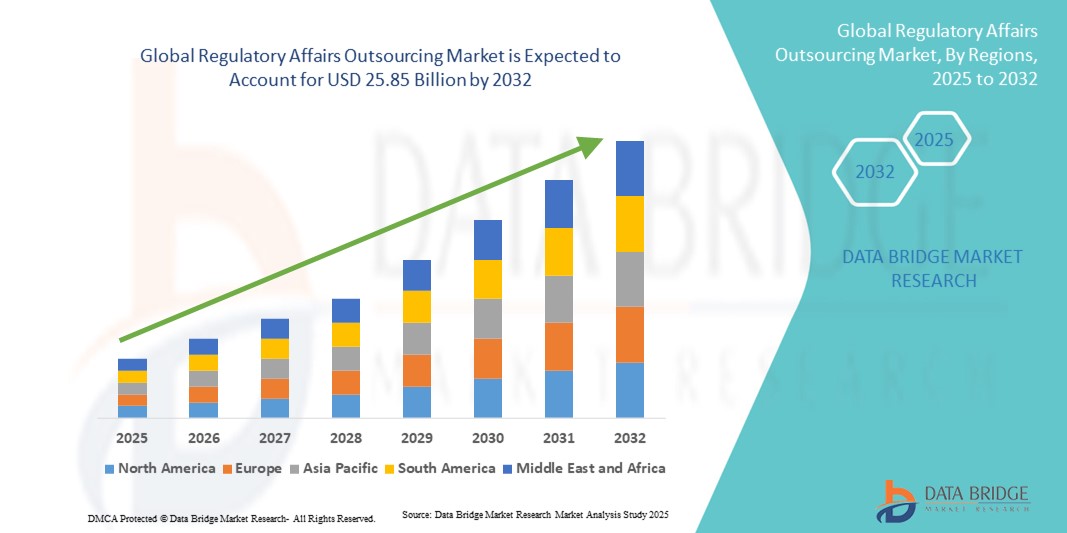
Global Regulatory Affairs Outsourcing Market
Taille du marché en milliards USD
TCAC :
% 
 USD
11.49 Billion
USD
25.85 Billion
2024
2032
USD
11.49 Billion
USD
25.85 Billion
2024
2032
| 2025 –2032 | |
| USD 11.49 Billion | |
| USD 25.85 Billion | |
|
|
|
|
Segments du marché mondial de l'externalisation des affaires réglementaires, par services (conseil réglementaire, représentation juridique, rédaction et publication réglementaires, enregistrement de produits, demandes d'essais cliniques et autres services), taille (petite, moyenne et grande), catégorie (médicaments, génériques, innovateurs, produits biologiques, biotechnologies, médicaments de thérapie innovante, dispositifs médicaux, thérapeutiques et diagnostiques), indication (oncologie, neurologie, cardiologie, immunologie et autres), stade (préclinique, clinique et PMA (autorisation de mise sur le marché)), utilisateur final (entreprises de dispositifs médicaux, sociétés pharmaceutiques et sociétés de biotechnologie) - Tendances et prévisions du secteur jusqu'en 2032
Taille du marché de l'externalisation des affaires réglementaires
- La taille du marché mondial de l'externalisation des affaires réglementaires était évaluée à 11,49 milliards USD en 2024 et devrait atteindre 25,85 milliards USD d'ici 2032 , à un TCAC de 10,66 % au cours de la période de prévision.
- La croissance du marché est largement alimentée par la complexité croissante des exigences réglementaires dans les secteurs pharmaceutique, biotechnologique et des dispositifs médicaux, ce qui incite les entreprises à rechercher des services d'externalisation spécialisés pour la gestion de la conformité.
- Par ailleurs, la demande croissante de soumissions réglementaires rentables, efficaces et rapides favorise l'adoption de solutions d'externalisation des affaires réglementaires. Ces facteurs convergents accélèrent l'adoption de ces services, stimulant ainsi considérablement la croissance du secteur à l'échelle mondiale.
Analyse du marché de l'externalisation des affaires réglementaires
- L'externalisation des affaires réglementaires, impliquant la délégation des tâches de conformité, de soumission et de documentation à des prestataires de services spécialisés, devient un élément essentiel pour les entreprises pharmaceutiques, biotechnologiques et de dispositifs médicaux qui souhaitent naviguer efficacement dans des réglementations mondiales complexes.
- La demande croissante d'expertise réglementaire, conjuguée à la complexité croissante des processus d'approbation dans différentes régions, favorise l'adoption de services d'externalisation des affaires réglementaires. Les entreprises exploitent ces services pour garantir un accès rapide au marché, réduire les risques de non-conformité et se concentrer sur leurs activités principales de recherche et développement.
- L'Amérique du Nord a dominé le marché de l'externalisation des affaires réglementaires, avec une part de chiffre d'affaires de 40,5 % en 2024, grâce à la présence de grandes entreprises pharmaceutiques et biotechnologiques, à la réglementation stricte de la FDA et au volume important d'essais cliniques nécessitant un soutien réglementaire spécialisé. Les États-Unis dominent le marché régional grâce à leur infrastructure solide, à leurs directives réglementaires exhaustives et à la forte demande de solutions d'externalisation expertes.
- L'Asie-Pacifique devrait connaître la croissance la plus rapide sur le marché de l'externalisation des affaires réglementaires au cours de la période de prévision, grâce à l'expansion de la production pharmaceutique, à la hausse des investissements dans le secteur de la santé et à la sensibilisation croissante à la conformité réglementaire dans des pays comme la Chine, l'Inde et le Japon. Des solutions d'externalisation rentables et la croissance des activités d'essais cliniques accélèrent encore la croissance du marché.
- Le segment des grandes entreprises a dominé le marché de l'externalisation des affaires réglementaires, avec une part de chiffre d'affaires de 45 % en 2024, grâce aux vastes activités mondiales des multinationales pharmaceutiques, biotechnologiques et des dispositifs médicaux. Les grandes entreprises externalisent souvent leurs fonctions réglementaires pour gérer d'importants volumes d'enregistrements de produits, maintenir la conformité dans plusieurs régions et optimiser leur efficacité opérationnelle.
Portée du rapport et segmentation du marché de l'externalisation des affaires réglementaires
|
Attributs |
Externalisation des affaires réglementaires : informations clés sur le marché |
|
Segments couverts |
|
|
Pays couverts |
Amérique du Nord
Europe
Asie-Pacifique
Moyen-Orient et Afrique
Amérique du Sud
|
|
Principaux acteurs du marché |
|
|
Opportunités de marché |
|
|
Ensembles d'informations de données à valeur ajoutée |
Outre les informations sur les scénarios de marché tels que la valeur marchande, le taux de croissance, la segmentation, la couverture géographique et les principaux acteurs, les rapports de marché organisés par Data Bridge Market Research comprennent également une analyse approfondie des experts, une analyse des prix, une analyse de la part de marque, une enquête auprès des consommateurs, une analyse démographique, une analyse de la chaîne d'approvisionnement, une analyse de la chaîne de valeur, un aperçu des matières premières/consommables, des critères de sélection des fournisseurs, une analyse PESTLE, une analyse Porter et un cadre réglementaire. |
Tendances du marché de l'externalisation des affaires réglementaires
Demande croissante d'expertise réglementaire spécialisée
- Une tendance significative et croissante sur le marché mondial de l'externalisation des affaires réglementaires est le recours croissant à des prestataires de services spécialisés pour la gestion des soumissions réglementaires complexes, de la documentation de conformité et des processus d'approbation. Cette tendance est motivée par la nécessité d'accéder rapidement au marché et de se conformer à l'évolution de la réglementation dans de multiples zones géographiques.
- Les entreprises pharmaceutiques, biotechnologiques et de dispositifs médicaux externalisent de plus en plus les tâches réglementaires pour rationaliser leurs opérations, réduire les risques de conformité et se concentrer davantage sur les activités de recherche et développement de base.
- Les principaux fournisseurs de services du marché élargissent leurs offres pour inclure un soutien réglementaire de bout en bout, y compris la préparation des dossiers, la gestion des soumissions, la surveillance post-commercialisation et la veille réglementaire, garantissant ainsi que les clients restent conformes aux exigences régionales et mondiales.
- La complexité croissante des réglementations, associée aux directives strictes des autorités telles que la FDA, l'EMA et la PMDA, stimule la demande de solutions d'externalisation qui offrent une expertise dans les stratégies réglementaires mondiales et des délais de soumission plus rapides.
- En outre, la croissance des activités d'essais cliniques et le nombre croissant d'approbations de produits en Amérique du Nord, en Europe et en Asie-Pacifique alimentent la croissance du marché, car les entreprises recherchent des services de soutien réglementaire rentables et fiables.
- Le marché de l'externalisation des affaires réglementaires connaît une expansion tant dans les grandes organisations pharmaceutiques que dans les petites et moyennes entreprises, soulignant son adoption généralisée et le rôle essentiel de l'expertise externalisée dans l'accélération du développement et de la commercialisation des produits.
Dynamique du marché de l'externalisation des affaires réglementaires
Conducteur
Besoin croissant en raison de la complexité croissante de la réglementation et de l'expansion mondiale
- La complexité croissante des exigences réglementaires dans les secteurs pharmaceutique, biotechnologique et des dispositifs médicaux, associée à l'expansion mondiale des marchés de la santé, constitue un facteur important de la demande accrue d'externalisation des affaires réglementaires.
- Par exemple, en avril 2024, une importante CRO a annoncé l'extension de ses services de conseil réglementaire pour inclure le suivi des soumissions et la surveillance de la conformité, basés sur l'IA, pour les marchés mondiaux. Ces stratégies, mises en œuvre par des entreprises clés, devraient stimuler la croissance du secteur de l'externalisation des affaires réglementaires au cours de la période de prévision.
- Alors que les entreprises pharmaceutiques et biotechnologiques sont confrontées à des normes de conformité plus strictes et à des mises à jour fréquentes des cadres réglementaires, l'externalisation donne accès à une expertise spécialisée pour l'enregistrement des produits, les demandes d'essais cliniques et l'autorisation post-commercialisation, offrant ainsi une alternative convaincante à la gestion interne.
- En outre, la tendance croissante aux lancements de produits à l'échelle mondiale et aux essais cliniques transfrontaliers fait de l'externalisation des affaires réglementaires une partie intégrante de la stratégie opérationnelle, permettant aux entreprises de naviguer efficacement dans divers environnements réglementaires et de garantir des approbations en temps opportun.
- La possibilité de faire appel à des professionnels de la réglementation expérimentés, la réduction de la charge de travail interne liée à la conformité et l'accès à des conseils actualisés sur l'évolution de la réglementation sont des facteurs clés qui favorisent l'externalisation des affaires réglementaires, tant au sein des grandes entreprises pharmaceutiques que des entreprises de biotechnologie émergentes. La tendance aux partenariats stratégiques et la disponibilité croissante d'options d'externalisation flexibles contribuent également à la croissance du marché.
Retenue/Défi
Préoccupations concernant la sécurité des données et les coûts élevés des services
- Les préoccupations concernant la confidentialité et la sécurité des données cliniques et réglementaires sensibles constituent un obstacle majeur à l'adoption généralisée de l'externalisation des affaires réglementaires. L'externalisation s'appuyant sur des prestataires de services externes et des plateformes numériques, elle présente un risque potentiel de violation de données ou d'accès non autorisé, suscitant des inquiétudes chez les entreprises quant à la conformité et à la protection de la propriété intellectuelle.
- Par exemple, les rapports sur les vulnérabilités en matière de cybersécurité dans les plateformes de gestion des données ont rendu certaines entreprises prudentes quant à l’externalisation des fonctions réglementaires.
- Répondre à ces préoccupations grâce à un chiffrement robuste, des protocoles d'authentification sécurisés et le respect des normes internationales de protection des données (par exemple, RGPD, HIPAA) est essentiel pour instaurer la confiance des clients. Des entreprises comme Parexel et Medpace mettent en avant leurs mesures avancées de sécurité des données et leurs cadres de conformité dans leurs offres de services afin de rassurer leurs clients potentiels.
- En outre, le coût relativement élevé des services complets d’externalisation réglementaire par rapport aux équipes internes peut constituer un obstacle pour les petites et moyennes entreprises, en particulier sur les marchés émergents.
- Bien que les frais de service deviennent progressivement plus compétitifs, la prime perçue pour l'externalisation d'une expertise réglementaire spécialisée peut encore entraver l'adoption, en particulier pour les entreprises disposant de budgets limités ou celles qui gèrent un petit portefeuille de produits.
- Surmonter ces défis grâce à des protocoles de sécurité des données améliorés, à la formation des clients sur les meilleures pratiques de conformité et au développement de solutions d'externalisation réglementaire rentables sera essentiel pour une croissance soutenue du marché.
Portée du marché de l'externalisation des affaires réglementaires
Le marché est segmenté en fonction des perspectives de services, de la taille, de la catégorie, de l’indication, de l’étape et de l’utilisateur final.
- Par Services Outlook
Sur la base des perspectives des services, le marché est segmenté en conseil réglementaire, représentation juridique, rédaction et publication réglementaires, enregistrement de produits, demandes d'essais cliniques et autres services. Le segment du conseil réglementaire a dominé le marché avec la plus grande part de chiffre d'affaires, soit 42,5 % en 2024. Cette domination est due au fait que les entreprises pharmaceutiques et biotechnologiques s'appuient de plus en plus sur l'expertise d'experts pour s'adapter aux cadres réglementaires mondiaux complexes. Le conseil réglementaire offre un soutien stratégique pour la préparation des dossiers, les soumissions réglementaires et la gestion de la conformité, ce qui garantit des approbations plus rapides et un risque de rejet réduit. La forte présence de ce segment est renforcée par le nombre croissant de produits en développement, le lancement de nouveaux médicaments et l'augmentation des investissements en R&D. Les multinationales privilégient souvent les services de conseil en raison de leur capacité à fournir une connaissance réglementaire multirégionale et des solutions sur mesure. La nécessité de maintenir la conformité dans un environnement réglementaire en constante évolution a renforcé la position de leader du conseil réglementaire.
Le segment des demandes d'essais cliniques devrait connaître le TCAC le plus rapide, soit 22,1 % entre 2025 et 2032, en raison de la complexité croissante des soumissions d'essais cliniques et de la rigueur des réglementations. L'externalisation des demandes d'essais cliniques permet aux entreprises de gérer efficacement les soumissions, de respecter les directives mondiales et de suivre les approbations dans plusieurs régions. La multiplication des essais en oncologie, neurologie et immunologie, conjuguée à l'adoption croissante des plateformes de soumission numériques, stimule la demande. Les entreprises privilégient l'externalisation pour minimiser les risques, améliorer leur efficacité et garantir l'exactitude des données. La croissance est également portée par les PME qui recherchent une expertise sans avoir à gérer de grandes équipes réglementaires internes, ce qui souligne le fort potentiel du segment.
- Par taille
Le marché est segmenté en petites, moyennes et grandes entreprises, selon leur taille. Le segment des grandes entreprises a dominé le marché avec une part de chiffre d'affaires de 45 % en 2024, portée par les vastes activités mondiales des multinationales pharmaceutiques, biotechnologiques et des dispositifs médicaux. Les grandes entreprises externalisent souvent leurs fonctions réglementaires pour gérer d'importants volumes d'enregistrements de produits, maintenir la conformité dans plusieurs régions et optimiser leur efficacité opérationnelle. Dotées de solides ressources financières et techniques, ces entreprises peuvent faire appel à des prestataires de services de premier plan, capables de gérer des tâches réglementaires complexes. Elles bénéficient également d'un risque réduit de retards réglementaires et peuvent se concentrer sur leurs priorités stratégiques et de R&D. La demande d'externalisation des affaires réglementaires dans les grandes entreprises continue de croître en raison de l'augmentation des pipelines, des multiples lancements de produits et de la rigueur des réglementations mondiales.
Le segment des petites entreprises devrait connaître le TCAC le plus rapide, soit 20,8 % entre 2025 et 2032, car les entreprises biotechnologiques émergentes et les start-ups pharmaceutiques ont de plus en plus recours à l'externalisation. Les petites entreprises manquent souvent d'équipes réglementaires internes importantes et privilégient une expertise externe pour l'enregistrement des produits, la conformité et les soumissions cliniques. La croissance de ce segment est soutenue par une meilleure connaissance des exigences réglementaires, l'augmentation du nombre d'essais cliniques et des solutions d'externalisation rentables. Cette tendance est particulièrement marquée dans les régions où se trouvent des pôles biotechnologiques émergents, où les connaissances réglementaires sont limitées en interne. L'externalisation permet aux petites entreprises d'accéder à des professionnels expérimentés et d'obtenir des approbations plus rapidement sans investissements opérationnels lourds.
- Par catégorie
Sur la base des catégories, le marché est segmenté en médicaments, génériques, innovateurs, produits biologiques, biotechnologies, ATMP, dispositifs médicaux, thérapeutiques et diagnostiques. Le segment des médicaments a dominé le marché avec la plus grande part de chiffre d'affaires (41,7 %) en 2024, en raison du nombre élevé de nouvelles entités chimiques et de la nécessité de soumettre des demandes réglementaires exhaustives. L'externalisation réglementaire dans ce segment permet aux entreprises de maintenir la conformité aux directives de la FDA, de l'EMA et de la PMDA tout en accélérant la mise sur le marché. Les entreprises bénéficient d'une gestion experte de la documentation, de stratégies de soumission mondiales et d'un suivi des approbations. Cette domination est renforcée par des investissements importants en R&D, d'importants portefeuilles de produits et un nombre croissant d'approbations à l'échelle mondiale. L'externalisation contribue à atténuer les risques d'erreurs de soumission et de retards réglementaires, faisant de ce segment un moteur clé de la croissance du marché.
Le segment des médicaments de thérapie innovante (MTI) devrait connaître le TCAC le plus rapide, soit 23,4 % entre 2025 et 2032, grâce à l'innovation dans les thérapies géniques et cellulaires. Les services d'externalisation réglementaire offrent une expertise spécialisée pour la documentation complexe, les demandes d'essais cliniques et la conformité post-commercialisation. La croissance des investissements en R&D, l'augmentation des autorisations et la complexité réglementaire des thérapies innovantes rendent le soutien externe essentiel. Les entreprises tirent parti de l'externalisation pour s'adapter efficacement aux réglementations multirégionales, garantissant ainsi des lancements de produits plus rapides et une conformité renforcée. L'adoption des MTI en oncologie, en immunologie et dans le traitement des maladies rares accélère encore la croissance de ce segment.
- Par indication
Sur la base des indications, le marché est segmenté en oncologie, neurologie, cardiologie, immunologie et autres. Le segment de l'oncologie a dominé avec la plus grande part de chiffre d'affaires (44,2 %) en 2024, grâce aux investissements mondiaux importants en R&D dans les thérapies contre le cancer et à l'augmentation du nombre d'approbations de médicaments oncologiques. L'externalisation réglementaire en oncologie aide les entreprises à gérer efficacement le volume des demandes d'autorisation, la complexité de la documentation et la conformité multi-pays. La prévalence croissante du cancer et l'innovation dans les thérapies ciblées ont stimulé la demande d'externalisation. Ce segment bénéficie d'un soutien gouvernemental important, de procédures d'approbation accélérées et d'essais cliniques à grande échelle, ce qui en fait l'indication la plus lucrative. L'externalisation permet des approbations plus rapides et une réduction des risques dans un marché de l'oncologie hautement réglementé et concurrentiel.
Le segment de l'immunologie devrait connaître le TCAC le plus rapide, soit 21,6 % entre 2025 et 2032, grâce au développement de nouvelles immunothérapies, vaccins et produits biologiques. L'externalisation réglementaire apporte une expertise en matière de soumissions d'essais cliniques, de documentation et de conformité réglementaire pour les thérapies émergentes. La sensibilisation croissante, l'augmentation des investissements dans la R&D en immunologie et l'introduction de produits biologiques innovants stimulent la croissance. Les entreprises exploitent l'externalisation pour surmonter les contraintes de ressources internes tout en garantissant l'efficacité réglementaire. La croissance rapide du segment est également soutenue par l'expansion des marchés mondiaux et la demande croissante de traitements immunologiques avancés.
- Par étape
En fonction du stade d'avancement, le marché est segmenté en phases préclinique, clinique et PMA (Post Market Authorization). Le segment clinique a dominé avec la plus grande part de chiffre d'affaires (43 %) en 2024, grâce au nombre élevé d'essais cliniques mondiaux et aux exigences strictes de conformité réglementaire. L'externalisation des activités de phase clinique permet aux entreprises de gérer efficacement les protocoles d'essai, les soumissions et les approbations dans toutes les régions. La forte demande d'essais en oncologie, neurologie et cardiologie stimule également la croissance. Les entreprises bénéficient d'un examen réglementaire plus rapide, d'une documentation précise et d'un accès à des professionnels expérimentés, ce qui réduit leur charge opérationnelle. La complexité et le volume des travaux réglementaires liés à la phase clinique continuent de faire de ce segment un moteur dominant du marché.
Le segment PMA (Post Market Authorization) devrait connaître le TCAC le plus rapide, soit 20,9 % entre 2025 et 2032, en raison des exigences croissantes en matière de surveillance post-commercialisation, de déclaration des effets indésirables et d'obligations de conformité continues pour les médicaments et les dispositifs médicaux. L'externalisation des activités liées à la PMA permet aux entreprises d'assurer efficacement le suivi de la sécurité, de mettre à jour la documentation et de se conformer efficacement à l'évolution de la réglementation. La croissance est également soutenue par l'augmentation des autorisations de mise sur le marché de produits biologiques, de dispositifs médicaux et de thérapies innovantes, ce qui rend l'externalisation de la PMA essentielle à une conformité durable.
- Par utilisateur final
En fonction de l'utilisateur final, le marché est segmenté en entreprises de dispositifs médicaux, entreprises pharmaceutiques et entreprises de biotechnologie. Le segment des entreprises pharmaceutiques a dominé le marché avec une part de chiffre d'affaires de 46 % en 2024, soutenue par un nombre élevé d'approbations de médicaments, des essais cliniques approfondis et des exigences réglementaires mondiales. L'externalisation permet aux entreprises pharmaceutiques de se concentrer sur leur cœur de métier, la R&D, tout en garantissant la conformité aux réglementations internationales. Les entreprises bénéficient d'une atténuation des risques, de coûts opérationnels réduits et de lancements de produits plus rapides. Cette domination est renforcée par des opérations mondiales à grande échelle et des pipelines multi-produits, faisant des entreprises pharmaceutiques les principaux utilisateurs de services d'externalisation réglementaire.
Le secteur des entreprises de biotechnologie devrait connaître le TCAC le plus rapide, soit 22,7 % entre 2025 et 2032, grâce aux innovations rapides dans les thérapies géniques, les produits biologiques et autres produits biotechnologiques. L'externalisation des fonctions réglementaires permet aux entreprises de biotechnologie de surmonter les contraintes de capacité internes et de gérer efficacement les demandes d'autorisation dans plusieurs pays. Cette croissance est également alimentée par l'augmentation des investissements dans la R&D biotechnologique, l'émergence de pôles biotechnologiques et une meilleure connaissance des meilleures pratiques réglementaires. Les entreprises de biotechnologie s'appuient sur des prestataires de services spécialisés pour accélérer les approbations et garantir la conformité dans un environnement hautement réglementé et dynamique.
Analyse régionale du marché de l'externalisation des affaires réglementaires
- L'Amérique du Nord a dominé le marché de l'externalisation des affaires réglementaires avec la plus grande part de revenus de 40,5 % en 2024, grâce à la demande croissante de services réglementaires spécialisés dans les secteurs pharmaceutique, biotechnologique et des dispositifs médicaux.
- L'infrastructure de santé mature de la région, la présence de grandes CRO mondiales et l'adoption précoce de stratégies réglementaires innovantes contribuent au leadership du marché
- En Amérique du Nord, les entreprises externalisent de plus en plus de services tels que le conseil réglementaire, l'enregistrement des produits et les demandes d'essais cliniques afin de garantir leur conformité aux réglementations strictes de la FDA et de Santé Canada. Une connaissance approfondie des complexités réglementaires, combinée à un soutien juridique et technique solide, renforce l'adoption de cette solution par les petites et grandes entreprises.
Aperçu du marché américain de l'externalisation des affaires réglementaires
Le marché américain de l'externalisation des affaires réglementaires a représenté la plus grande part de chiffre d'affaires en Amérique du Nord en 2024, avec 81 %, grâce au nombre croissant d'approbations de produits pharmaceutiques, biotechnologiques et de dispositifs médicaux nécessitant un soutien réglementaire spécialisé. Ce marché bénéficie de cadres réglementaires avancés, d'une forte présence de CRO et d'une forte demande de services tels que la rédaction réglementaire, la représentation juridique et la gestion des autorisations post-commercialisation. Les grandes, moyennes et petites entreprises en oncologie, neurologie, cardiologie, immunologie et autres domaines thérapeutiques ont de plus en plus recours à l'externalisation pour gérer efficacement les étapes réglementaires précliniques, cliniques et post-commercialisation.
Aperçu du marché européen de l'externalisation des affaires réglementaires
Le marché européen de l'externalisation des affaires réglementaires devrait connaître une croissance annuelle moyenne (TCAC) substantielle au cours de la période de prévision, principalement portée par la complexité des cadres réglementaires dans l'UE et l'importance croissante accordée à la conformité des thérapies innovantes telles que les produits biologiques, les médicaments de thérapie innovante (MTI) et les dispositifs médicaux. En Allemagne, en France et dans d'autres pays de l'UE, les entreprises externalisent leurs services réglementaires, notamment les demandes d'essais cliniques, l'enregistrement des produits et le conseil réglementaire, afin de maîtriser leurs coûts et de garantir des autorisations rapides. L'urbanisation croissante, l'intensification des activités de R&D et la présence de prestataires de services réglementaires spécialisés favorisent la croissance du marché pour les petites, moyennes et grandes entreprises.
Aperçu du marché britannique de l'externalisation des affaires réglementaires
Le marché britannique de l'externalisation des affaires réglementaires devrait connaître une croissance annuelle moyenne (TCAC) remarquable au cours de la période de prévision, stimulé par la demande croissante de services de conformité réglementaire de la part des entreprises pharmaceutiques et biotechnologiques. L'externalisation de services tels que la rédaction et la publication de réglementations, la gestion des demandes d'essais cliniques et l'enregistrement de produits aide les entreprises à s'y retrouver efficacement dans la réglementation de la MHRA. Le solide écosystème de santé, associé à des CRO bien établies et à une solide expertise en conseil réglementaire, soutient la croissance dans de nombreux domaines thérapeutiques, notamment l'oncologie, la cardiologie et l'immunologie.
Aperçu du marché allemand de l'externalisation des affaires réglementaires
Le marché allemand de l'externalisation des affaires réglementaires devrait connaître une croissance annuelle moyenne (TCAC) considérable au cours de la période de prévision, alimenté par une sensibilisation croissante à la conformité réglementaire, des réglementations européennes strictes et la nécessité d'une gestion rentable des processus précliniques, cliniques et d'autorisation post-commercialisation. Les entreprises pharmaceutiques, biotechnologiques et de dispositifs médicaux allemandes ont de plus en plus recours à des services d'externalisation tels que la représentation juridique, le conseil réglementaire et l'enregistrement des produits. La présence de CRO spécialisées et de normes sectorielles strictes favorise l'adoption de ces services par les petites, moyennes et grandes entreprises, couvrant diverses indications et domaines thérapeutiques.
Aperçu du marché de l'externalisation des affaires réglementaires en Asie-Pacifique
Le marché de l'externalisation des affaires réglementaires en Asie-Pacifique devrait connaître son taux de croissance annuel composé le plus élevé au cours de la période de prévision 2025-2032, porté par l'essor des secteurs pharmaceutique, biotechnologique et des dispositifs médicaux dans des pays comme la Chine, l'Inde et le Japon. Le développement des infrastructures de santé, les initiatives gouvernementales en faveur des essais cliniques et l'essor de la R&D stimulent l'adoption de services d'externalisation pour le conseil réglementaire, les demandes d'essais cliniques et la gestion post-autorisation de mise sur le marché. Les petites, moyennes et grandes entreprises font de plus en plus appel à ces services pour garantir leur conformité aux exigences réglementaires locales et internationales dans de nombreux domaines thérapeutiques.
Aperçu du marché japonais de l'externalisation des affaires réglementaires
Le marché japonais de l'externalisation des affaires réglementaires connaît un essor considérable grâce à l'avancée des secteurs de la santé et des biotechnologies, à des exigences réglementaires strictes et à la croissance des activités de R&D. Les entreprises externalisent des services tels que l'enregistrement des produits, la rédaction réglementaire et la gestion des essais cliniques pour s'y conformer efficacement aux réglementations PMDA. La croissance du marché est soutenue par une demande dans diverses indications telles que l'oncologie, la cardiologie et la neurologie, et l'adoption de cette approche touche les petites, moyennes et grandes entreprises pharmaceutiques, biotechnologiques et de dispositifs médicaux.
Aperçu du marché chinois de l'externalisation des affaires réglementaires
En 2024, le marché chinois de l'externalisation des affaires réglementaires représentait la plus grande part de chiffre d'affaires en Asie-Pacifique, grâce à l'essor des industries pharmaceutiques et biotechnologiques, à l'urbanisation rapide et à l'augmentation des dépenses de R&D. L'externalisation de services tels que le conseil réglementaire, les demandes d'essais cliniques, l'enregistrement des produits et la gestion des autorisations post-commercialisation est très demandée, permettant aux entreprises de se conformer efficacement aux réglementations NMPA. Les petites, moyennes et grandes entreprises du secteur des médicaments, des produits biologiques, des dispositifs médicaux et des médicaments de thérapie antimicrobienne (MTA) ont de plus en plus recours à l'externalisation réglementaire pour accélérer l'approbation des produits et leur mise sur le marché.
Part de marché de l'externalisation des affaires réglementaires
Le secteur de l’externalisation des affaires réglementaires est principalement dirigé par des entreprises bien établies, notamment :
- Accell Clinical Research, LLC (États-Unis)
- Genpact (États-Unis)
- CRITERIUM, INC. (États-Unis)
- Promedica International (États-Unis)
- WuXiAppTec (Chine)
- Medpace (États-Unis)
- PPD Inc. (États-Unis)
- Laboratoires Charles River (États-Unis)
- ICON plc (États-Unis)
- Parexel International (MA) Corporation (États-Unis)
- Freyr (États-Unis)
- Navitas Clinical Research, Inc. (États-Unis)
- Medelis, Inc. (États-Unis)
- Sciformix (États-Unis)
- Tech Tammina (États-Unis)
- Acorn Regulatory Consultancy Services Ltd. (Irlande)
- BIOMAPAS (Lituanie)
- PROFESSIONNELS DE LA RÉGLEMENTATION (Australie)
- CompareNetworks, Inc. (États-Unis)
Derniers développements sur le marché mondial de l'externalisation des affaires réglementaires
- En juillet 2025, l'Agence britannique de réglementation des médicaments et des produits de santé (MHRA) a annoncé qu'elle externaliserait environ 40 % de ses demandes d'autorisation de mise sur le marché de médicaments et de dispositifs médicaux à des agences réglementaires étrangères de confiance. Cette décision visait à préserver les ressources et à se concentrer sur des domaines innovants tels que l'intelligence artificielle dans les soins de santé et les thérapies innovantes. La « procédure de reconnaissance internationale » de la MHRA, introduite en avril 2024, a permis des approbations plus rapides, basées sur les décisions des autorités réglementaires de l'UE, des États-Unis ou de l'Australie.
- En février 2021, ICON plc a acquis PRA Health Sciences, Inc. dans le cadre d'une transaction en numéraire et en actions, évaluée à environ 12 milliards de dollars américains. Cette acquisition a renforcé l'offre de services médicaux de l'entreprise.
- En août 2021, le groupe ProPharma a acquis la société indienne iSafety Systems. Cette acquisition devrait renforcer la position du groupe ProPharma comme principal fournisseur mondial de conseil en réglementation et conformité, de pharmacovigilance, de services de recherche clinique et d'information médicale.
SKU-
Accédez en ligne au rapport sur le premier cloud mondial de veille économique
- Tableau de bord d'analyse de données interactif
- Tableau de bord d'analyse d'entreprise pour les opportunités à fort potentiel de croissance
- Accès d'analyste de recherche pour la personnalisation et les requêtes
- Analyse de la concurrence avec tableau de bord interactif
- Dernières actualités, mises à jour et analyse des tendances
- Exploitez la puissance de l'analyse comparative pour un suivi complet de la concurrence
Méthodologie de recherche
La collecte de données et l'analyse de l'année de base sont effectuées à l'aide de modules de collecte de données avec des échantillons de grande taille. L'étape consiste à obtenir des informations sur le marché ou des données connexes via diverses sources et stratégies. Elle comprend l'examen et la planification à l'avance de toutes les données acquises dans le passé. Elle englobe également l'examen des incohérences d'informations observées dans différentes sources d'informations. Les données de marché sont analysées et estimées à l'aide de modèles statistiques et cohérents de marché. De plus, l'analyse des parts de marché et l'analyse des tendances clés sont les principaux facteurs de succès du rapport de marché. Pour en savoir plus, veuillez demander un appel d'analyste ou déposer votre demande.
La méthodologie de recherche clé utilisée par l'équipe de recherche DBMR est la triangulation des données qui implique l'exploration de données, l'analyse de l'impact des variables de données sur le marché et la validation primaire (expert du secteur). Les modèles de données incluent la grille de positionnement des fournisseurs, l'analyse de la chronologie du marché, l'aperçu et le guide du marché, la grille de positionnement des entreprises, l'analyse des brevets, l'analyse des prix, l'analyse des parts de marché des entreprises, les normes de mesure, l'analyse globale par rapport à l'analyse régionale et des parts des fournisseurs. Pour en savoir plus sur la méthodologie de recherche, envoyez une demande pour parler à nos experts du secteur.
Personnalisation disponible
Data Bridge Market Research est un leader de la recherche formative avancée. Nous sommes fiers de fournir à nos clients existants et nouveaux des données et des analyses qui correspondent à leurs objectifs. Le rapport peut être personnalisé pour inclure une analyse des tendances des prix des marques cibles, une compréhension du marché pour d'autres pays (demandez la liste des pays), des données sur les résultats des essais cliniques, une revue de la littérature, une analyse du marché des produits remis à neuf et de la base de produits. L'analyse du marché des concurrents cibles peut être analysée à partir d'une analyse basée sur la technologie jusqu'à des stratégies de portefeuille de marché. Nous pouvons ajouter autant de concurrents que vous le souhaitez, dans le format et le style de données que vous recherchez. Notre équipe d'analystes peut également vous fournir des données sous forme de fichiers Excel bruts, de tableaux croisés dynamiques (Fact book) ou peut vous aider à créer des présentations à partir des ensembles de données disponibles dans le rapport.