Global Clinical Trial Management System Market
Taille du marché en milliards USD
TCAC :
% 
 USD
1.41 Billion
USD
3.87 Billion
2024
2032
USD
1.41 Billion
USD
3.87 Billion
2024
2032
| 2025 –2032 | |
| USD 1.41 Billion | |
| USD 3.87 Billion | |
|
|
|
|
Segmentation du marché mondial des systèmes de gestion des essais cliniques (CTMS), par type (entreprise et sur site), livraison (Web, Cloud et sur site), composant (logiciel et service), utilisateur final (entreprises pharmaceutiques et biotechnologiquesCRO et fabricants de dispositifs médicaux ) - Tendances et prévisions du secteur jusqu'en 2032
Taille du marché des systèmes de gestion des essais cliniques (CTMS)
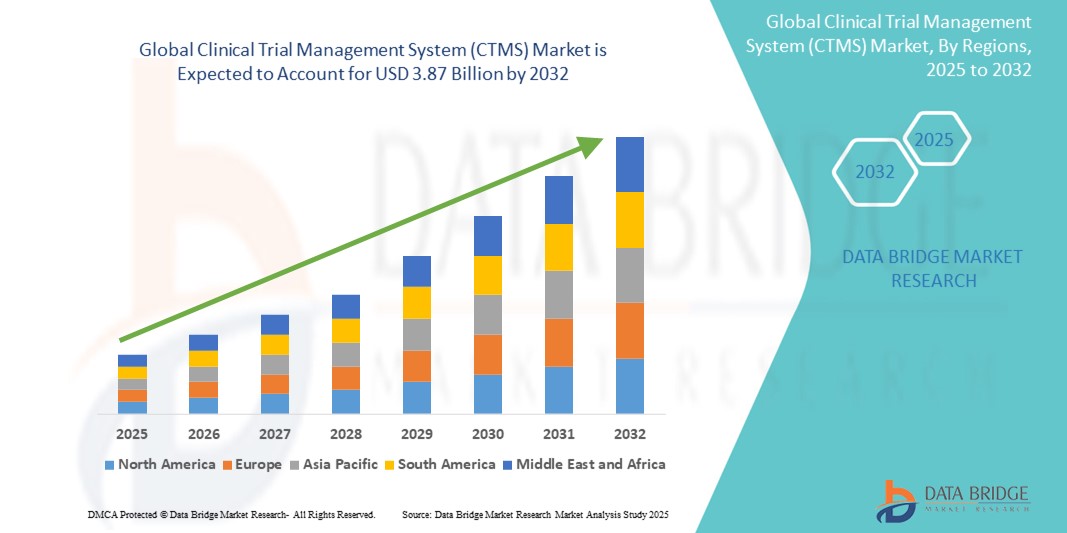
- La taille du marché mondial des systèmes de gestion des essais cliniques (CTMS) était évaluée à 1,41 milliard USD en 2024 et devrait atteindre 3,87 milliards USD d'ici 2032 , à un TCAC de 13,4 % au cours de la période de prévision.
- Cette croissance est tirée par des facteurs tels que l’augmentation des investissements en R&D, le volume croissant des essais cliniques et les avancées technologiques.
Analyse du marché des systèmes de gestion des essais cliniques (CTMS)
- Les systèmes de gestion des essais cliniques (SGC) sont des outils essentiels pour les industries pharmaceutique et biotechnologique. Ils offrent des solutions complètes pour la planification, le suivi et la gestion des essais cliniques. Ils jouent un rôle essentiel pour garantir la conformité réglementaire, améliorer l'exactitude des données et optimiser les opérations d'essai.
- La demande de solutions CTMS est fortement stimulée par l'augmentation du volume des essais cliniques, la hausse des investissements en R&D et la complexité croissante des études cliniques. L'intégration de technologies avancées, notamment l'IA, l'apprentissage automatique et le cloud computing, renforce encore l'efficacité et l'évolutivité des plateformes CTMS.
- L'Amérique du Nord devrait dominer le marché des systèmes de gestion des essais cliniques (CTMS), représentant environ 47,6 % de la part de marché mondiale, grâce à la présence de grandes sociétés pharmaceutiques et biotechnologiques, à une solide infrastructure de recherche clinique et à des réglementations gouvernementales favorables soutenant les essais cliniques.
- L'Asie-Pacifique devrait être la région connaissant la croissance la plus rapide sur le marché des systèmes de gestion des essais cliniques (CTMS), avec un TCAC de 12,8 %, grâce à l'augmentation de l'activité des essais cliniques, à l'expansion rapide des infrastructures de soins de santé et aux avantages en termes de coûts pour la conduite de recherches cliniques dans la région.
- Le segment web devrait dominer le marché avec une part de marché de 71,7 %, grâce à son évolutivité, sa flexibilité et sa rentabilité. Privilégiées pour la gestion des essais cliniques, les plateformes CTMS cloud offrent un accès en temps réel aux données des essais, une sécurité renforcée des données et des coûts d'infrastructure informatique réduits, favorisant ainsi une gestion efficace des essais.
Portée du rapport et segmentation du marché des systèmes de gestion des essais cliniques (CTMS)
|
Attributs |
Informations clés sur le marché des systèmes de gestion des essais cliniques (CTMS) |
|
Segments couverts |
|
|
Pays couverts |
Amérique du Nord
Europe
Asie-Pacifique
Moyen-Orient et Afrique
Amérique du Sud
|
|
Principaux acteurs du marché |
|
|
Opportunités de marché |
|
|
Ensembles d'informations de données à valeur ajoutée |
Outre les informations sur les scénarios de marché tels que la valeur marchande, le taux de croissance, la segmentation, la couverture géographique et les principaux acteurs, les rapports de marché organisés par Data Bridge Market Research comprennent également une analyse des importations et des exportations, un aperçu de la capacité de production, une analyse de la consommation de production, une analyse des tendances des prix, un scénario de changement climatique, une analyse de la chaîne d'approvisionnement, une analyse de la chaîne de valeur, un aperçu des matières premières/consommables, des critères de sélection des fournisseurs, une analyse PESTLE, une analyse Porter et un cadre réglementaire. |
Tendances du marché des systèmes de gestion des essais cliniques (CTMS)
« Intégration de l'IA et de l'analyse avancée dans CTMS »
- Une tendance significative dans l’évolution des systèmes de gestion des essais cliniques est l’intégration croissante de l’intelligence artificielle (IA), de l’apprentissage automatique (ML) et de l’analyse avancée.
- Ces technologies permettent l’analyse des données en temps réel, des informations prédictives et l’automatisation des processus, améliorant ainsi l’efficacité et la précision de la gestion des essais cliniques.
- Par exemple , les plateformes CTMS basées sur l'IA peuvent anticiper les difficultés de recrutement des patients, optimiser le choix des sites et identifier les retards potentiels, réduisant ainsi considérablement les délais et les coûts des essais. Cette fonctionnalité est particulièrement précieuse dans les essais multinationaux à grande échelle, où la rapidité de la prise de décision est essentielle.
- Ces avancées transforment les opérations d’essais cliniques, améliorent les résultats des patients et stimulent la demande de plateformes CTMS de nouvelle génération avec des analyses de données de pointe et une intégration de l’IA.
Dynamique du marché des systèmes de gestion des essais cliniques (CTMS)
Conducteur
« Demande croissante pour une gestion efficace des essais cliniques »
- La complexité croissante des essais cliniques, favorisée par l’essor de la médecine de précision, des thérapies personnalisées et des essais décentralisés, contribue de manière significative à la demande de systèmes robustes de gestion des essais cliniques.
- À mesure que les essais cliniques deviennent de plus en plus mondiaux et nécessitent davantage de données, le besoin d'accès aux données en temps réel, de flux de travail rationalisés et de conformité réglementaire devient essentiel pour les sponsors, les CRO et les instituts de recherche.
- Les plates-formes CTMS avancées offrent des solutions intégrées pour la gestion des sites, l'inscription des patients, la collecte de données et le suivi financier, améliorant ainsi l'efficacité des essais et réduisant les coûts opérationnels.
Par exemple,
- En janvier 2024, selon un article publié dans le Journal of Clinical Research, le marché mondial des essais cliniques devrait connaître une croissance significative, avec plus de 30 % des essais qui devraient adopter des modèles décentralisés d'ici 2028. Cette évolution stimule la demande de solutions CTMS avancées capables de gérer des conceptions d'essais complexes et la gestion des données à distance.
- En conséquence, le besoin de systèmes efficaces de gestion des essais cliniques devrait augmenter, soutenant la croissance du marché CTMS.
Opportunité
« Intégration de l'IA et de l'analyse avancée dans CTMS »
- Les plateformes CTMS basées sur l'IA peuvent améliorer l'efficacité des essais en automatisant les tâches de routine, en améliorant le recrutement des patients et en optimisant l'analyse des données, permettant ainsi une prise de décision plus précise et plus rapide.
- Ces plateformes exploitent des algorithmes d'apprentissage automatique pour prédire les retards des essais, optimiser la sélection des sites et réduire les taux d'abandon, réduisant ainsi considérablement les délais et les coûts des essais.
- De plus, les systèmes CTMS basés sur l'IA peuvent fournir des informations en temps réel sur les données des patients, permettant des conceptions d'essais plus personnalisées et adaptatives.
Par exemple,
- En mars 2025, selon un rapport de Clinical Research News, plusieurs grandes entreprises pharmaceutiques ont intégré l'IA à leurs plateformes CTMS, ce qui a permis d'accélérer jusqu'à 40 % le recrutement des patients et de réduire de 30 % le coût des essais cliniques. Ces avancées devraient transformer la gestion des essais cliniques et stimuler la demande de solutions CTMS basées sur l'IA.
- L'intégration de l'IA dans les systèmes CTMS peut également améliorer la précision des données, réduire les coûts opérationnels et améliorer les résultats globaux des essais, créant ainsi des opportunités de croissance significatives pour le marché
Retenue/Défi
« Coûts de mise en œuvre élevés et problèmes de sécurité des données »
- Le coût élevé de la mise en œuvre et de la maintenance des plateformes CTMS avancées peut constituer un obstacle important pour les petites et moyennes organisations de recherche clinique (CRO) et les entreprises de biotechnologie.
- Ces plateformes nécessitent souvent un investissement initial substantiel, notamment en matière de licences logicielles, de mises à niveau de l'infrastructure et de formation du personnel, ce qui peut être prohibitif pour les petites organisations.
- En outre, les préoccupations concernant la sécurité des données et la conformité réglementaire peuvent encore freiner l’adoption, car les essais cliniques génèrent des données sensibles sur les patients qui doivent être protégées contre les violations et les accès non autorisés.
Par exemple,
- En septembre 2024, un rapport du Data Protection Journal a souligné la menace croissante des cyberattaques dans le secteur de la santé, les données des essais cliniques devenant une cible privilégiée. Cela a incité de nombreuses organisations à investir massivement dans la cybersécurité, augmentant ainsi le coût global de la mise en œuvre du CTMS.
- Par conséquent, le coût élevé et les défis liés à la sécurité des données associés aux systèmes CTMS peuvent limiter leur adoption, en particulier parmi les petites organisations, ralentissant ainsi la croissance globale du marché.
Portée du marché des systèmes de gestion des essais cliniques (CTMS)
Le marché est segmenté en fonction du type, de la livraison, des composants et de l’utilisateur final.
|
Segmentation |
Sous-segmentation |
|
Par type |
|
|
Par livraison |
|
|
Par composants |
|
|
Par utilisateur final |
|
En 2025, le Web devrait dominer le marché avec une part de marché plus importante dans le segment de la livraison.
Le segment de la diffusion en ligne devrait dominer le marché des systèmes de gestion des essais cliniques (SGC) avec une part de marché de 71,7 % en 2025, grâce à son évolutivité, sa flexibilité et sa rentabilité. Privilégiées pour la gestion des essais cliniques, les plateformes SGC basées sur le cloud offrent un accès en temps réel aux données des essais, une sécurité renforcée des données et des coûts d'infrastructure informatique réduits, favorisant ainsi une gestion efficace des essais. La transition continue vers des essais décentralisés et le suivi à distance des patients contribue à la domination de ce segment, stimulant ainsi la croissance du marché.
L'entreprise devrait représenter la plus grande part au cours de la période de prévision sur le marché des types de produits.
En 2025, le segment des entreprises devrait dominer le marché des systèmes de gestion des essais cliniques (SGC) avec une part de marché de 65,4 %, grâce à sa capacité à gérer des essais cliniques complexes et multicentriques et à soutenir les opérations mondiales. Références pour la recherche clinique à grande échelle, les plateformes SGC d'entreprise offrent un accès aux données en temps réel, des analyses robustes et une collaboration fluide entre les acteurs des essais cliniques, améliorant ainsi l'efficacité et les résultats des essais. La demande croissante de solutions intégrées et évolutives contribue également à sa domination sur le marché.
Analyse régionale du marché des systèmes de gestion des essais cliniques (CTMS)
« L'Amérique du Nord détient la plus grande part du marché des systèmes de gestion des essais cliniques (CTMS) »
- L'Amérique du Nord devrait dominer le marché des systèmes de gestion des essais cliniques (CTMS), représentant 47,6 % de la part de marché mondiale, grâce à la présence de grandes sociétés pharmaceutiques et biotechnologiques, à une solide infrastructure de recherche clinique et à des réglementations gouvernementales favorables soutenant les essais cliniques.
- Les États-Unis détiennent une part importante de 35,3 % en raison du volume élevé d'essais cliniques, des investissements substantiels en R&D et de l'adoption précoce de technologies avancées de gestion des essais cliniques.
- L’écosystème de soins de santé bien établi de la région, sa vaste population de patients et son accent sur la médecine personnalisée contribuent également à son leadership sur le marché.
- De plus, la présence de professionnels qualifiés, d'une infrastructure informatique avancée et de cadres réglementaires solides renforcent encore le marché CTMS en Amérique du Nord.
« La région Asie-Pacifique devrait enregistrer le TCAC le plus élevé sur le marché des systèmes de gestion des essais cliniques (CTMS) »
- L'Asie-Pacifique devrait connaître le taux de croissance le plus élevé sur le marché des systèmes de gestion des essais cliniques (CTMS), avec un TCAC prévu d'environ 12,8 %, grâce à l'augmentation de l'activité des essais cliniques, à l'expansion rapide des infrastructures de soins de santé et aux avantages en termes de coûts pour la conduite de recherches cliniques dans la région.
- Des pays comme la Chine, l'Inde et la Corée du Sud émergent comme des marchés clés en raison de la croissance des industries pharmaceutiques et biotechnologiques et de l'augmentation du nombre de patients inscrits aux essais cliniques.
- La Chine est leader sur le marché régional avec un soutien gouvernemental important pour la recherche clinique, de larges populations de patients et des capacités de fabrication biopharmaceutique en expansion
- L'Inde devrait enregistrer le TCAC le plus élevé sur le marché CTMS, grâce à des opérations d'essais cliniques rentables, un nombre croissant d'organisations de recherche sous contrat (CRO) et des investissements étrangers croissants dans le secteur de la santé.
Part de marché des systèmes de gestion des essais cliniques (CTMS)
Le paysage concurrentiel du marché fournit des détails par concurrent. Il comprend la présentation de l'entreprise, ses données financières, son chiffre d'affaires, son potentiel de marché, ses investissements en recherche et développement, ses nouvelles initiatives commerciales, sa présence mondiale, ses sites et installations de production, ses capacités de production, ses forces et faiblesses, le lancement de nouveaux produits, leur ampleur et leur portée, ainsi que la domination de ses applications. Les données ci-dessus ne concernent que les activités des entreprises par rapport à leur marché.
Les principaux leaders du marché opérant sur le marché sont :
- Advarra (États-Unis)
- ICON plc (Irlande)
- Merative (États-Unis)
- DSG, Inc. (États-Unis)
- ArisGlobal (États-Unis)
- Clario (États-Unis)
- Oracle (États-Unis)
- Medidata (États-Unis)
- Fountayn (États-Unis)
- MedNet (États-Unis)
- IQVIA Inc. (États-Unis)
- SimpleTrials (États-Unis)
- Calyx Global Inc. (États-Unis)
- RealTime Software Solutions, LLC (États-Unis)
- LabCorp (États-Unis)
- Veeva Systems (États-Unis)
- Wipro (Inde)
- PHARMASEAL (Royaume-Uni)
Derniers développements sur le marché mondial des systèmes de gestion des essais cliniques (CTMS)
- En février 2025, Medidata Solutions, fournisseur leader de technologies pour les essais cliniques, a annoncé le lancement de son nouveau système de gestion des essais cliniques basé sur l'IA, conçu pour améliorer l'intégration des données et l'analyse en temps réel. Ce système offre des capacités de suivi des essais améliorées, des évaluations des risques automatisées et des flux de travail simplifiés pour la conformité réglementaire, visant à accélérer le développement des médicaments et à améliorer l'efficacité des essais.
- En novembre 2024, Oracle Corporation a dévoilé la dernière version de sa plateforme CTMS, dotée de fonctionnalités cloud améliorées, notamment des outils avancés de recrutement de patients, la prise en charge de la surveillance à distance et des modules de consentement électronique intégrés. Ces innovations visent à soutenir les essais cliniques décentralisés et hybrides, en améliorant l'engagement des participants et la précision des données.
- En octobre 2024, IQVIA Inc. a lancé sa solution CTMS nouvelle génération intégrant des algorithmes d'apprentissage automatique pour prédire les risques liés aux essais et optimiser l'allocation des ressources. La plateforme fournit également des tableaux de bord en temps réel et des rapports personnalisables pour optimiser la prise de décision des organismes de recherche clinique (CRO) et des promoteurs.
- En août 2024, Clario a annoncé l'extension de son offre CTMS avec des modules intégrés de saisie électronique des données (SED) et de résultats rapportés par les patients (RTP). Ce système unifié vise à simplifier la gestion des données, à améliorer la conformité et à optimiser la conception des essais cliniques centrés sur le patient. La plateforme mise à jour vise à améliorer l'efficacité opérationnelle et la préparation réglementaire.
SKU-
Accédez en ligne au rapport sur le premier cloud mondial de veille économique
- Tableau de bord d'analyse de données interactif
- Tableau de bord d'analyse d'entreprise pour les opportunités à fort potentiel de croissance
- Accès d'analyste de recherche pour la personnalisation et les requêtes
- Analyse de la concurrence avec tableau de bord interactif
- Dernières actualités, mises à jour et analyse des tendances
- Exploitez la puissance de l'analyse comparative pour un suivi complet de la concurrence
Méthodologie de recherche
La collecte de données et l'analyse de l'année de base sont effectuées à l'aide de modules de collecte de données avec des échantillons de grande taille. L'étape consiste à obtenir des informations sur le marché ou des données connexes via diverses sources et stratégies. Elle comprend l'examen et la planification à l'avance de toutes les données acquises dans le passé. Elle englobe également l'examen des incohérences d'informations observées dans différentes sources d'informations. Les données de marché sont analysées et estimées à l'aide de modèles statistiques et cohérents de marché. De plus, l'analyse des parts de marché et l'analyse des tendances clés sont les principaux facteurs de succès du rapport de marché. Pour en savoir plus, veuillez demander un appel d'analyste ou déposer votre demande.
La méthodologie de recherche clé utilisée par l'équipe de recherche DBMR est la triangulation des données qui implique l'exploration de données, l'analyse de l'impact des variables de données sur le marché et la validation primaire (expert du secteur). Les modèles de données incluent la grille de positionnement des fournisseurs, l'analyse de la chronologie du marché, l'aperçu et le guide du marché, la grille de positionnement des entreprises, l'analyse des brevets, l'analyse des prix, l'analyse des parts de marché des entreprises, les normes de mesure, l'analyse globale par rapport à l'analyse régionale et des parts des fournisseurs. Pour en savoir plus sur la méthodologie de recherche, envoyez une demande pour parler à nos experts du secteur.
Personnalisation disponible
Data Bridge Market Research est un leader de la recherche formative avancée. Nous sommes fiers de fournir à nos clients existants et nouveaux des données et des analyses qui correspondent à leurs objectifs. Le rapport peut être personnalisé pour inclure une analyse des tendances des prix des marques cibles, une compréhension du marché pour d'autres pays (demandez la liste des pays), des données sur les résultats des essais cliniques, une revue de la littérature, une analyse du marché des produits remis à neuf et de la base de produits. L'analyse du marché des concurrents cibles peut être analysée à partir d'une analyse basée sur la technologie jusqu'à des stratégies de portefeuille de marché. Nous pouvons ajouter autant de concurrents que vous le souhaitez, dans le format et le style de données que vous recherchez. Notre équipe d'analystes peut également vous fournir des données sous forme de fichiers Excel bruts, de tableaux croisés dynamiques (Fact book) ou peut vous aider à créer des présentations à partir des ensembles de données disponibles dans le rapport.