Middle East And Africa Electronic Clinical Outcome Assessment Market
Marktgröße in Milliarden USD
CAGR :
% 
 USD
57.02 million
USD
144.23 million
2022
2030
USD
57.02 million
USD
144.23 million
2022
2030
| 2023 –2030 | |
| USD 57.02 million | |
| USD 144.23 million | |
|
|
|
Markt für elektronische klinische Ergebnisbeurteilungen (eCOA) im Nahen Osten und in Afrika, nach Produkt (Lösungen vor Ort, Cloud-basierte Lösungen und webbasierte Lösungen), Ansatz (Clinician Reported Outcome Assessment (CLINRO), Patient Reported Outcome Assessment (PRO), Observer Reported Outcome Assessment (OBSRO) und Performance Outcome Assessment (PERFO)), Endnutzer (gewerbliche Dienstleister, Krankenhäuser und Transplantationszentren, Forschungslabore und akademische Einrichtungen), Plattform (Auftragsforschungsinstitute, Pharma- und Biopharmaunternehmen, Hersteller medizinischer Geräte, Krankenhäuser und klinische Labore, Beratungsdienstleistungsunternehmen, Forschung und Wissenschaft und andere) – Branchentrends und Prognose bis 2030.
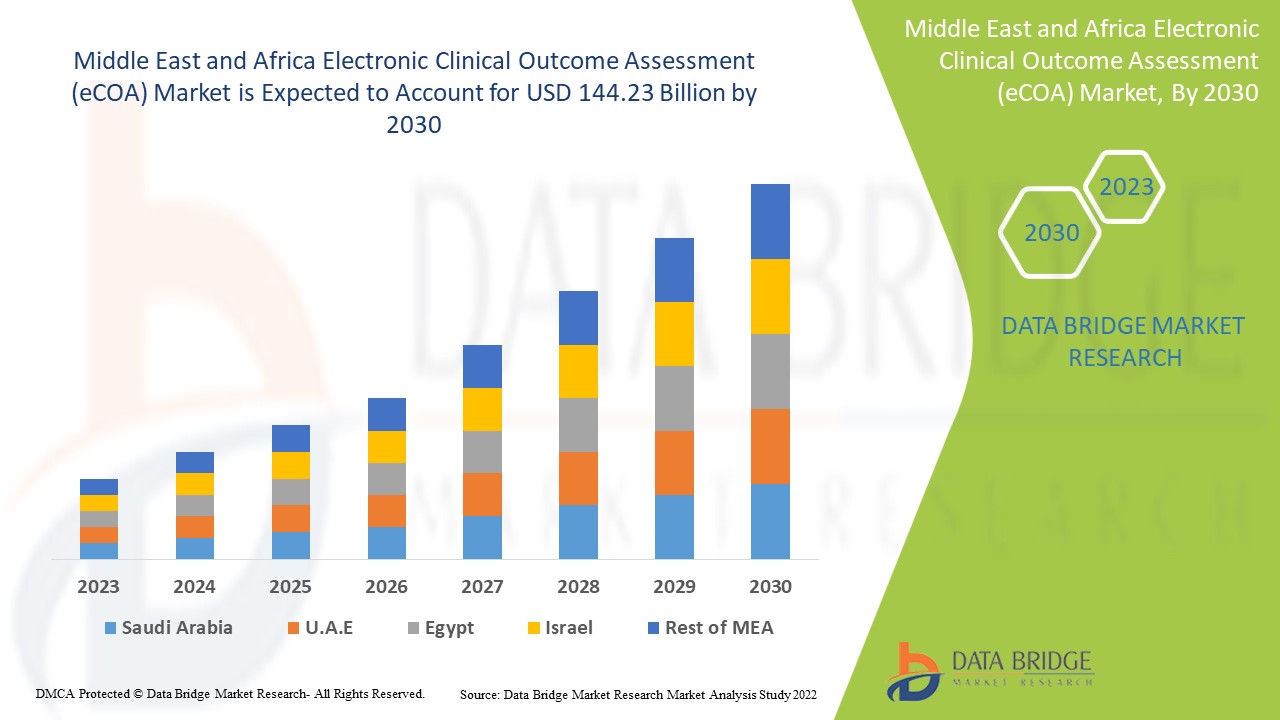
Marktanalyse und -größe für elektronische klinische Ergebnisbeurteilungen (eCOA) im Nahen Osten und in Afrika
Die Notwendigkeit, die Compliance zu verbessern, klinische Informationen effektiv zu erfassen und zu verwalten, Kosten zu senken und die F&E-Aktivitäten zu steigern, dürfte das Marktwachstum vorantreiben. Kayentis, ein französisches Unternehmen, das auf Lösungen zur elektronischen klinischen Ergebnisbewertung (eCOA) spezialisiert ist, wird im Dezember 2020 eine Finanzierung von rund 8,3 Millionen USD erhalten. Dies unterstützte seine Ziele der regionalen Expansion und Produktentwicklung.
Data Bridge Market Research analysiert, dass der Markt für elektronische klinische Ergebnisbewertungen (eCOA), der im Jahr 2022 57,02 Milliarden USD betrug, bis 2030 voraussichtlich 144,23 Milliarden USD erreichen wird, bei einer CAGR von 12,30 % während des Prognosezeitraums 2023 bis 2030. Zusätzlich zu den Einblicken in Marktszenarien wie Marktwert, Wachstumsrate, Segmentierung, geografische Abdeckung und wichtige Akteure enthalten die von Data Bridge Market Research kuratierten Marktberichte auch eingehende Expertenanalysen, Patientenepidemiologie, Pipeline-Analysen, Preisanalysen und regulatorische Rahmenbedingungen.
Marktumfang und -segmentierung für elektronische klinische Ergebnisbeurteilungen (eCOA) im Nahen Osten und in Afrika
|
Berichtsmetrik |
Details |
|
Prognosezeitraum |
2023 bis 2030 |
|
Basisjahr |
2022 |
|
Historische Jahre |
2021 (Anpassbar auf 2015 – 2020) |
|
Quantitative Einheiten |
Umsatz in Mrd. USD, Volumen in Einheiten, Preise in USD |
|
Abgedeckte Segmente |
Produkt (On-Premise-Lösungen, Cloud-basierte Lösungen und webbasierte Lösungen), Ansatz (Clinician Reported Outcome Assessment (CLINRO), Patient Reported Outcome Assessment (PRO), Observer Reported Outcome Assessment (OBSRO) und Performance Outcome Assessment (PERFO)), Endbenutzer (kommerzielle Dienstleister, Krankenhäuser und Transplantationszentren, Forschungslabore und akademische Einrichtungen), Plattform (Auftragsforschungsinstitute, Pharma- und Biopharmaunternehmen, Hersteller medizinischer Geräte, Krankenhäuser und klinische Labore, Beratungsdienstleistungsunternehmen, Forschung und Wissenschaft und andere) |
|
Abgedeckte Länder |
Saudi-Arabien, Vereinigte Arabische Emirate, Südafrika, Ägypten, Israel, Rest des Nahen Ostens und Afrikas (MEA) als Teil des Nahen Ostens und Afrikas (MEA) |
|
Abgedeckte Marktteilnehmer |
IBM Corporation (USA), IQVIA (USA), Medidata Solutions, Inc. (USA), Clario (USA), ArisGlobal (USA), Signant Health (USA), TransPerfect (USA), Cloudbyz (USA), Climedo Health GmbH (Deutschland), ClinCapture (USA), Oracle Corporation (USA), Paraxel International Corporation (USA), eClinical Solutions LLC (USA), OmniComm Systems, Inc. (USA), CRF Health (USA), European Round Table (USA) |
|
Marktchancen |
|
Marktdefinition
Elektronische klinische Ergebnisbewertungen werden verwendet, um den Zustand eines Patienten sowie die Folgen und den Verlauf einer Krankheit zu bestimmen (eCOA). Elektronische klinische Ergebnisbewertungen bieten Echtzeittransparenz, die die Einhaltung von Protokollen, die Sicherheit und Teilnahme der Patienten sowie die Reduzierung des Studienrisikos unterstützt.
Marktdynamik für elektronische klinische Ergebnisbeurteilungen (eCOA) im Nahen Osten und in Afrika
Treiber
- Steigende Belastung für Pharmahersteller
Um die Gesamtkosten zu senken, verlassen sich neue Techniken zur Medikamentenentwicklung zunehmend auf die elektronische Datenerfassung statt auf papierbasierte Verfahren. Die Datenerfassung mithilfe elektronischer Plattformen zur klinischen Ergebnisbewertung verbessert die Datenqualität, harmonisiert die Datenerfassungspraktiken und bietet den Benutzern einen erheblichen Mehrwert, beispielsweise durch Datenanalyse. Elektronische Datenerfassungs- und -analysedienste beseitigen die Nachteile papierbasierter Aufzeichnungen und erhöhen gleichzeitig die Compliance der Patienten. Sie senken außerdem die Kosten für die Standortüberwachung und eliminieren das Risiko von Datenschwankungen. Diese Lösungen bieten rationalisierte Informationen, die durch strukturierte Datenerfassung zur Verbesserung der Datenqualität beitragen. Die oben genannten Vorteile der Verwendung elektronischer klinischer Ergebnisbewertungen werden voraussichtlich die Produktnachfrage in den kommenden Jahren steigern.
- Anstieg klinischer Ergebnisbeurteilungen
Klinische Ergebnisbewertungen (COAs) werden daher immer häufiger verwendet, um die Wirksamkeit verschiedener Therapien für chronische Krankheiten zu beurteilen. Diese waren häufig von entscheidender Bedeutung für die behördliche Zulassung von Arzneimitteln. Das Hinzufügen zahlreicher Dienste wird ebenfalls zum Wachstum beitragen. So startete Signant Health im Juni 2021 ein neuartiges Beschleunigungsprogramm, das die Zeitpläne für die Studieneinrichtung um 50 % oder mehr verkürzt, ohne die Qualität der klinischen Daten zu beeinträchtigen. Die zunehmende Einführung neuartiger Programme, die Unternehmen bei der Bewertung klinischer Studien zugute kommen, dürfte daher die Nachfrage nach elektronischen Lösungen zur klinischen Ergebnisbewertung erhöhen und so das Marktwachstum ankurbeln.
Gelegenheiten
- Steigende Nachfrage nach elektronischen Lösungen zur klinischen Ergebnisbewertung
Laut einer Studie, die 2020 in der American Chemical Society Pharmacology and Translational Science veröffentlicht wurde, wurden mithilfe einer kombinierten virtuellen und experimentellen Screening-Strategie neue potenzielle COVID-19-Therapeutika identifiziert und aus einer Bibliothek von fast 4.000 zugelassenen Medikamenten ausgewählt, wobei Hydroxychloroquin (HCQ) als Referenzmedikament diente. Zuclopenthixol, Nebivolol und Amodiaquin wurden als potenzielle Kandidaten für klinische Studien für die frühen Stadien der SARS-CoV-2-Infektion vorgeschlagen, und Remdesivir- und Favipiravir-Therapeutika wurden als potenzielle Adjuvantien bei der COVID-19-Behandlung vorgeschlagen. Die Nachfrage nach elektronischen Lösungen zur klinischen Ergebnisbewertung wird voraussichtlich steigen, da die Zahl der klinischen Studien infolge der Umwidmung mehrerer Medikamente zunimmt.
Einschränkungen/Herausforderungen
- Hohe Implementierungskosten
Datenschutzprobleme und hohe Implementierungskosten schränken die Expansion des Marktes ein. Darüber hinaus dürften im Prognosezeitraum 2023–2030 fehlende günstige Erstattungsszenarien in Entwicklungsländern, hohe Zölle auf medizinische Geräte und ein Mangel an ausreichender Infrastruktur in Ländern mit niedrigem und mittlerem Einkommen den Markt vor Herausforderungen stellen.
Dieser Marktbericht zur elektronischen klinischen Ergebnisbewertung (eCOA) enthält Einzelheiten zu neuen Entwicklungen, Handelsvorschriften, Import-Export-Analysen, Produktionsanalysen, Wertschöpfungskettenoptimierungen, Marktanteilen, Auswirkungen inländischer und lokaler Marktteilnehmer, analysiert Chancen in Bezug auf neue Einnahmequellen, Änderungen der Marktvorschriften, strategische Marktwachstumsanalysen, Marktgröße, Kategoriemarktwachstum, Anwendungsnischen und -dominanz, Produktzulassungen, Produkteinführungen, geografische Expansionen und technologische Innovationen auf dem Markt. Um weitere Informationen zum Markt für elektronische klinische Ergebnisbewertung (eCOA) zu erhalten, wenden Sie sich an Data Bridge Market Research, um einen Analystenbericht zu erhalten. Unser Team hilft Ihnen dabei, eine fundierte Marktentscheidung zu treffen, um Marktwachstum zu erzielen.
Auswirkungen von COVID-19 auf den Markt für elektronische klinische Ergebnisbewertung (eCOA)
Die COVID-19-Pandemie erschwerte die Durchführung und Verwaltung klinischer Studien im Jahr 2020. Um diese Probleme anzugehen und die Kontinuität klinischer Forschungsaktivitäten sicherzustellen, setzten Marktteilnehmer eine Reihe von Initiativen um, darunter den Einsatz von eClinical-Technologien. Infolge der Pandemie wurden klinische Studien digitalisiert. Viele Sponsoren, Biopharmaunternehmen, Medizinproduktehersteller und Auftragsforschungsinstitute (CROs) haben begonnen, eClinical-Systeme zu verwenden, um Daten kostengünstig und aus der Ferne zu sammeln, zu verwalten und aussagekräftige Erkenntnisse daraus abzuleiten. Mithilfe der elektronischen klinischen Ergebnisbewertung können Patientendaten aus der Ferne erfasst werden.
Jüngste Entwicklung
• Im Jahr 2020 erweiterte Oracle sein Cloud-System auf Australien (Melbourne), Japan (Osaka), Saudi-Arabien (Jeddah), die Niederlande (Amsterdam) und Kanada (Montreal). Die Marktexpansion dürfte von der gestiegenen Bekanntheit der Cloud-basierten Anwendungen bei den Verbrauchern profitieren.
• Im Jahr 2020 ging ArisGlobal eine Partnerschaft mit Soterius, Inc. ein, um sein Produktangebot durch die Aufnahme von LifeSphere Medical Information und LifeSphere MultiVigilance in seinen serviceorientierten Technologie-Stack zu erweitern.
Marktumfang für elektronische klinische Ergebnisbeurteilungen (eCOA) im Nahen Osten und in Afrika
Der Markt für elektronische klinische Ergebnisbewertungen (eCOA) ist nach Produkt, Liefermodus, Ansatz, Plattform und Endbenutzer segmentiert. Das Wachstum dieser Segmente hilft Ihnen bei der Analyse schwacher Wachstumssegmente in den Branchen und bietet den Benutzern einen wertvollen Marktüberblick und Markteinblicke, die ihnen bei der strategischen Entscheidungsfindung zur Identifizierung der wichtigsten Marktanwendungen helfen.
Produkt
- On-Premise-Lösungen
- Cloudbasierte Lösungen
- Webbasierte Lösungen
Liefermodus
- Webgehostet
- Cloudbasiert
Ansatz
- Vom Patienten berichtetes Ergebnis (PRO)
- Vom Arzt berichtetes Ergebnis (CLINRO)
- Vom Beobachter gemeldetes Ergebnis (OBSRO)
- Leistungsergebnis (PERFO)
Plattform
- Auftragsforschungsinstitute
- Pharmazeutische und biopharmazeutische Unternehmen
- Hersteller medizinischer Geräte
- Krankenhäuser und klinische Labore
- Beratungsdienstleistungsunternehmen
- Forschung und Lehre
- Sonstiges
Endbenutzer
- Pharmazeutische und biopharmazeutische Unternehmen
- Auftragsforschungsinstitute
- Andere Endbenutzer
Regionale Analyse/Einblicke zum Markt für elektronische klinische Ergebnisbeurteilungen (eCOA)
Der Markt für elektronische klinische Ergebnisbeurteilungen (eCOA) wird analysiert und es werden Einblicke in die Marktgröße und Trends nach Land, Produkt, Bereitstellungsmodus, Ansatz, Plattform und Endbenutzer wie oben angegeben bereitgestellt.
Die im Marktbericht zur elektronischen klinischen Ergebnisbewertung (eCOA) abgedeckten Länder sind Saudi-Arabien, die Vereinigten Arabischen Emirate, Südafrika, Ägypten, Israel und der Rest des Nahen Ostens und Afrikas (MEA) als Teil des Nahen Ostens und Afrikas (MEA).
Der Länderabschnitt des Berichts enthält auch Angaben zu einzelnen marktbeeinflussenden Faktoren und Änderungen der Regulierung auf dem Inlandsmarkt, die sich auf die aktuellen und zukünftigen Trends des Marktes auswirken. Datenpunkte wie Downstream- und Upstream-Wertschöpfungskettenanalysen, technische Trends und Porters Fünf-Kräfte-Analyse sowie Fallstudien sind einige der Anhaltspunkte, die zur Prognose des Marktszenarios für einzelne Länder verwendet werden. Bei der Bereitstellung von Prognoseanalysen der Länderdaten werden auch die Präsenz und Verfügbarkeit globaler Marken und ihre Herausforderungen aufgrund großer oder geringer Konkurrenz durch lokale und inländische Marken sowie die Auswirkungen inländischer Zölle und Handelsrouten berücksichtigt.
Wachstum der Gesundheitsinfrastruktur, installierte Basis und Durchdringung mit neuen Technologien
Der Markt für elektronische klinische Ergebnisbewertungen (eCOA) bietet Ihnen außerdem detaillierte Marktanalysen für jedes Land, das Wachstum der Gesundheitsausgaben für Investitionsgüter, die installierte Basis verschiedener Arten von Produkten für den Markt für elektronische klinische Ergebnisbewertungen (eCOA), die Auswirkungen der Technologie anhand von Lebenslinienkurven und Änderungen der regulatorischen Szenarien im Gesundheitswesen und deren Auswirkungen auf den Markt für elektronische klinische Ergebnisbewertungen (eCOA). Die Daten sind für den historischen Zeitraum 2011–2021 verfügbar.
Wettbewerbsumfeld und Analyse der Marktanteile für elektronische klinische Ergebnisbewertung (eCOA)
Die Wettbewerbslandschaft des Marktes für elektronische klinische Ergebnisbewertungen (eCOA) liefert Details nach Wettbewerbern. Die enthaltenen Details sind Unternehmensübersicht, Unternehmensfinanzen, erzielter Umsatz, Marktpotenzial, Investitionen in Forschung und Entwicklung, neue Marktinitiativen, globale Präsenz, Produktionsstandorte und -anlagen, Produktionskapazitäten, Stärken und Schwächen des Unternehmens, Produkteinführung, Produktbreite und -umfang, Anwendungsdominanz. Die oben angegebenen Datenpunkte beziehen sich nur auf den Fokus der Unternehmen in Bezug auf den Markt für elektronische klinische Ergebnisbewertungen (eCOA).
Zu den wichtigsten Akteuren auf dem Markt für elektronische klinische Ergebnisbewertungen (eCOA) zählen:
- IBM Corporation (USA)
- IQVIA (USA)
- Medidata Solutions, Inc. (USA)
- Clario (USA)
- ArisGlobal (USA)
- Signant Health (USA)
- TransPerfect (USA)
- Cloudbyz (USA)
- Climedo Health GmbH (Deutschland)
- ClinCapture (USA)
- Oracle Corporation (USA)
- Paraxel International Corporation (USA)
- eClinical Solutions LLC (USA)
- OmniComm Systems, Inc. (USA)
- CRF Health (USA)
- Europäischer Runder Tisch (USA)
SKU-
Erhalten Sie Online-Zugriff auf den Bericht zur weltweit ersten Market Intelligence Cloud
- Interaktives Datenanalyse-Dashboard
- Unternehmensanalyse-Dashboard für Chancen mit hohem Wachstumspotenzial
- Zugriff für Research-Analysten für Anpassungen und Abfragen
- Konkurrenzanalyse mit interaktivem Dashboard
- Aktuelle Nachrichten, Updates und Trendanalyse
- Nutzen Sie die Leistungsfähigkeit der Benchmark-Analyse für eine umfassende Konkurrenzverfolgung
Forschungsmethodik
Die Datenerfassung und Basisjahresanalyse werden mithilfe von Datenerfassungsmodulen mit großen Stichprobengrößen durchgeführt. Die Phase umfasst das Erhalten von Marktinformationen oder verwandten Daten aus verschiedenen Quellen und Strategien. Sie umfasst die Prüfung und Planung aller aus der Vergangenheit im Voraus erfassten Daten. Sie umfasst auch die Prüfung von Informationsinkonsistenzen, die in verschiedenen Informationsquellen auftreten. Die Marktdaten werden mithilfe von marktstatistischen und kohärenten Modellen analysiert und geschätzt. Darüber hinaus sind Marktanteilsanalyse und Schlüsseltrendanalyse die wichtigsten Erfolgsfaktoren im Marktbericht. Um mehr zu erfahren, fordern Sie bitte einen Analystenanruf an oder geben Sie Ihre Anfrage ein.
Die wichtigste Forschungsmethodik, die vom DBMR-Forschungsteam verwendet wird, ist die Datentriangulation, die Data Mining, die Analyse der Auswirkungen von Datenvariablen auf den Markt und die primäre (Branchenexperten-)Validierung umfasst. Zu den Datenmodellen gehören ein Lieferantenpositionierungsraster, eine Marktzeitlinienanalyse, ein Marktüberblick und -leitfaden, ein Firmenpositionierungsraster, eine Patentanalyse, eine Preisanalyse, eine Firmenmarktanteilsanalyse, Messstandards, eine globale versus eine regionale und Lieferantenanteilsanalyse. Um mehr über die Forschungsmethodik zu erfahren, senden Sie eine Anfrage an unsere Branchenexperten.
Anpassung möglich
Data Bridge Market Research ist ein führendes Unternehmen in der fortgeschrittenen formativen Forschung. Wir sind stolz darauf, unseren bestehenden und neuen Kunden Daten und Analysen zu bieten, die zu ihren Zielen passen. Der Bericht kann angepasst werden, um Preistrendanalysen von Zielmarken, Marktverständnis für zusätzliche Länder (fordern Sie die Länderliste an), Daten zu klinischen Studienergebnissen, Literaturübersicht, Analysen des Marktes für aufgearbeitete Produkte und Produktbasis einzuschließen. Marktanalysen von Zielkonkurrenten können von technologiebasierten Analysen bis hin zu Marktportfoliostrategien analysiert werden. Wir können so viele Wettbewerber hinzufügen, wie Sie Daten in dem von Ihnen gewünschten Format und Datenstil benötigen. Unser Analystenteam kann Ihnen auch Daten in groben Excel-Rohdateien und Pivot-Tabellen (Fact Book) bereitstellen oder Sie bei der Erstellung von Präsentationen aus den im Bericht verfügbaren Datensätzen unterstützen.













