Markt für generische Injektionsmittel in Indien und Europa, nach therapeutischer Anwendung (Onkologie, Herz-Kreislauf-Erkrankungen, Infektionskrankheiten , Schmerzbehandlung, Stoffwechselstörungen (Diabetes) und immunologische Erkrankungen), Biosimilar-Arzneimittel (Semaglutid, Ibutidlidfumarat, Evolocumab, Alirocumab, Anidulafungin, Dulaglutid, Lixisenatid, Exenatid, Liraglutid und Adalimumab), Endverbraucher (Direktvertriebshändler, Pharmagroßhändler, Drogerien, Apotheken, Einkaufsgemeinschaften (GPOs) und andere), Vertriebskanäle (Pharmagroßhändler, Vertragshersteller, Apothekenketten, Einkaufsgemeinschaften (GPOs) und andere) – Branchentrends und Prognose bis 2035.
Marktanalyse und Größe für generische Injektionsmittel in Indien und Europa
Generische Injektionspräparate sind kostengünstiger als Markenpräparate und bieten eine attraktive Lösung für Gesundheitssysteme, die Kosten senken möchten, ohne Kompromisse bei der Qualität einzugehen. Dies treibt das Marktwachstum an. Der Anstieg des Marktwachstums durch eine stärkere Betonung der Auftragsforschungsproduktion dürfte Chancen für Marktwachstum schaffen.
Data Bridge Market Research analysiert, dass der Markt für generische Injektionsmittel in Indien und Europa im Prognosezeitraum von 2024 bis 2035 mit einer durchschnittlichen jährlichen Wachstumsrate von 9,0 % wächst und von 43.499,40 Millionen USD im Jahr 2023 auf 119.063,77 Millionen USD im Jahr 2031 ansteigen dürfte. Die zunehmende Häufigkeit chronischer Krankheiten und ein Anstieg bei der Entwicklung und Produktion generischer Injektionsmittel dürften das Marktwachstum vorantreiben.
|
Berichtsmetrik |
Details |
|
Prognosezeitraum |
2024 bis 2035 |
|
Basisjahr |
2023 |
|
Historisches Jahr |
2022 (Anpassbar 2016–2021) |
|
Quantitative Einheiten |
Umsatz in Mio. USD |
|
Abgedeckte Segmente |
Therapeutische Anwendung (Onkologie, Herz-Kreislauf-Erkrankungen, Infektionskrankheiten, Schmerzbehandlung, Stoffwechselstörungen (Diabetes) und immunologische Störungen), Biosimilar-Medikamente (Semaglutid, Ibutidlidfumarat, Evolocumab, Alirocumab, Anidulafungin, Dulaglutid, Lixisenatid, Exenatid, Liraglutid und Adalimumab), Endverbraucher (Direktvertriebshändler, Pharmagroßhändler, Drogerien, Apotheken, Einkaufsgemeinschaften (GPOs) und andere), Vertriebskanal (Pharmagroßhändler, Vertragshersteller, Apothekenketten, Einkaufsgemeinschaften (GPOs) und andere) |
|
Abgedecktes Land/Region |
Indien und Europa |
|
Abgedeckte Marktteilnehmer |
Cipla Inc., Dr. Reddy's Laboratories Ltd, Sanofi, Viatris Inc., Fresenius Kabi AG, Sandoz Group AG, GLENMARK PHARMACEUTICALS LTD, Gland Pharma Limited, Par Pharmaceutical und Sun Pharmaceutical Industries Ltd., unter anderem |
Marktdefinition
Der Begriff „generisches Injektionsmittel“ beschreibt die Verabreichung von Arzneimitteln durch Injektion mithilfe von Generika. Diese Verabreichungsmethode wird bevorzugt, da sie eine genaue Dosierung ermöglicht und als Ersatz dient, wenn eine orale Verabreichung nicht möglich oder nicht so wirksam ist. Die Verabreichung von generischen Injektionsmedikamenten ist für die Gesundheitsversorgung von wesentlicher Bedeutung, da sie preisgünstige Ersatzmittel bietet, ohne die therapeutischen Anforderungen zu beeinträchtigen.
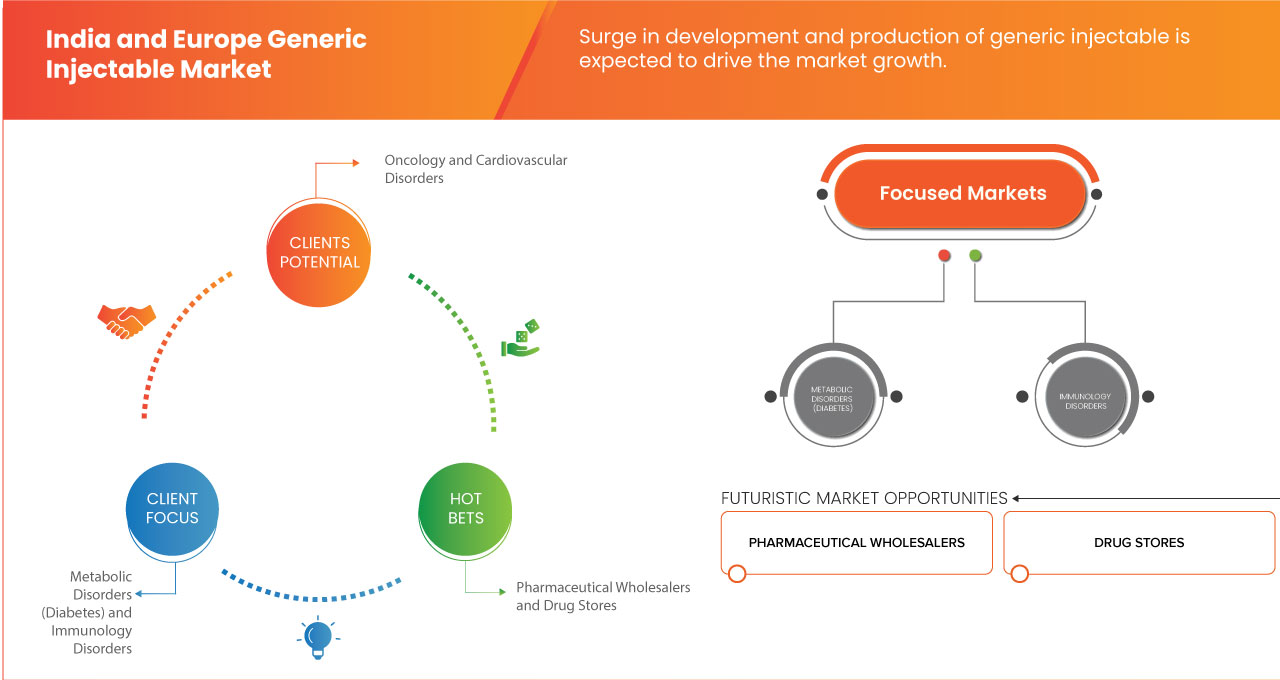
Marktdynamik für generische Injektionsmittel in Indien und Europa
In diesem Abschnitt geht es um das Verständnis der Markttreiber, Vorteile, Chancen, Einschränkungen und Herausforderungen. All dies wird im Folgenden ausführlich erläutert:
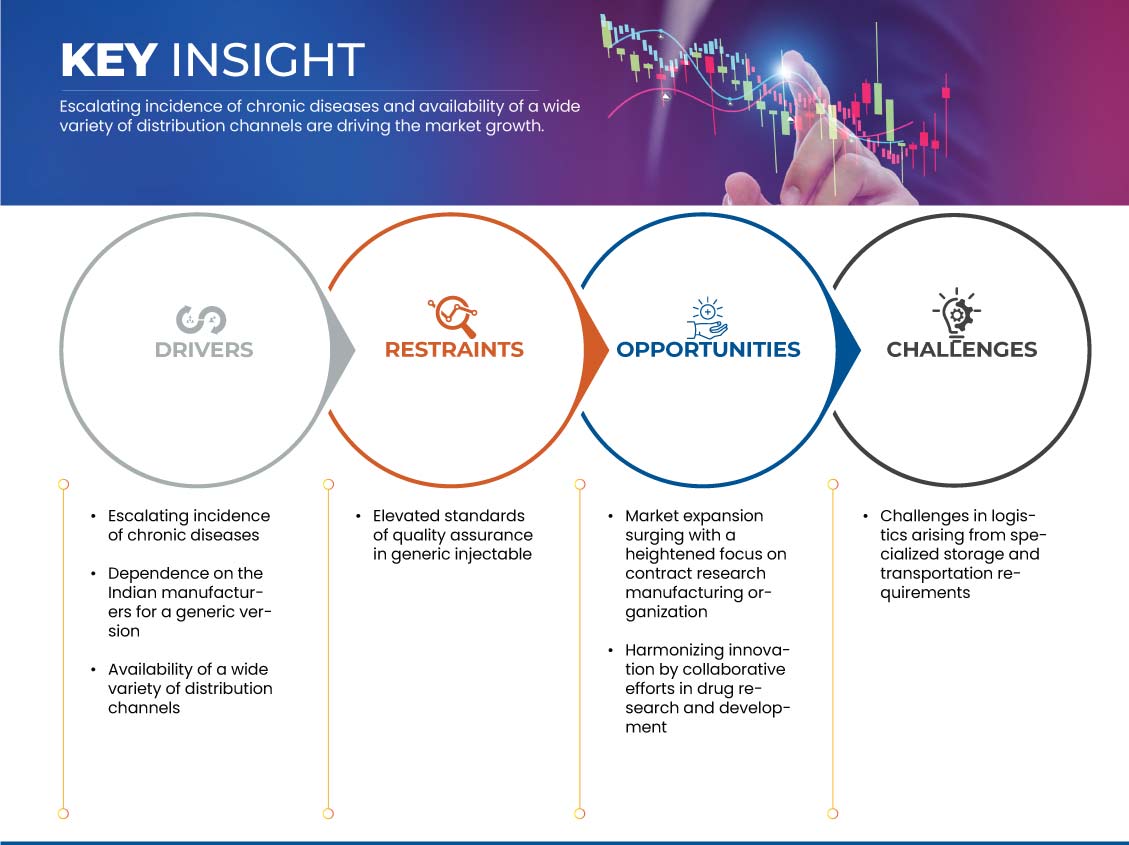
Treiber
- Anstieg bei der Entwicklung und Produktion von generischen injizierbaren
Der Markt erlebt einen bemerkenswerten Aufschwung aufgrund der zunehmenden Entwicklung und Produktion von generischen Injektionspräparaten. Dieser Aufschwung wird durch mehrere Faktoren vorangetrieben, darunter die zunehmende Betonung der Kosteneffizienz im Gesundheitswesen.
Generische Injektionsmittel sind wirtschaftlicher als ihre Markengegenstücke und stellen daher eine attraktive Lösung für Gesundheitssysteme dar, die Kosten senken möchten, ohne Kompromisse bei der Qualität einzugehen.
Der Ablauf der Patente für verschiedene Marken-Injektionsmedikamente hat weitere Möglichkeiten für generische Alternativen eröffnet, einen gesunden Wettbewerb gefördert und die Auswahlmöglichkeiten für Gesundheitsdienstleister erweitert. Regulatorische Unterstützung und günstige Rahmenbedingungen in Europa spielen eine entscheidende Rolle bei der Förderung der Zulassung und Markteinführung von Generika-Injektionsmedikamenten. Darüber hinaus trägt die steigende Nachfrage nach Biosimilars, insbesondere nach generischen Versionen komplexer biologischer Injektionsmedikamente, erheblich zur wachsenden Landschaft der Entwicklung von Generika-Injektionsmedikamenten bei.
- Zunahme chronischer Erkrankungen
Dieser Anstieg chronischer Krankheiten hat eine beispiellose Nachfrage nach gezielten und effizienten therapeutischen Interventionen geschaffen. Injektionssysteme haben sich als unverzichtbare Werkzeuge erwiesen, um die Komplexität dieser anhaltenden Gesundheitsprobleme zu bewältigen. Die inhärente Natur chronischer Krankheiten erfordert oft eine präzise Dosierungskontrolle und kontinuierliche Medikamentenverabreichung, Bereiche, in denen Injektionssysteme hervorragend sind. Der Markt gewinnt an Bedeutung, indem er Lösungen anbietet, die zu verbesserten Behandlungsergebnissen, verbessertem Patientenmanagement und erhöhter therapeutischer Wirksamkeit führen, da Gesundheitssysteme weltweit mit der zunehmenden Belastung durch chronische Krankheiten zu kämpfen haben.
Zusammenfassend lässt sich sagen, dass die Richtung des Marktes eng mit seiner Fähigkeit verknüpft ist, die komplexen Anforderungen an die Gesundheitsversorgung zu erfüllen, die sich aus der zunehmenden Verbreitung chronischer Krankheiten ergeben. Der Markt festigt seine zentrale Rolle als
Gelegenheit
- Steigendes Marktwachstum durch verstärkte Betonung der Auftragsforschungsfertigung
Auftragsforschungs- und -herstellungsorganisationen (CRMOs) erfreuen sich bei Pharmaunternehmen, insbesondere bei solchen, die Generika entwickeln, zunehmender Beliebtheit. Auftragshersteller nutzen spezialisiertes Fachwissen, verbessern Verfahren und steigern die Produktion von Generika. Durch die Nutzung von CRMOs zur Abwicklung der Produktion können sich Pharmaunternehmen auf ihre Kernkompetenzen konzentrieren, zu denen Marketing, Forschung und Einhaltung gesetzlicher Vorschriften gehören. Der Pharmasektor verändert sich und mit ihm steigt der Bedarf an Effizienz, Wirtschaftlichkeit und Flexibilität bei der Arzneimittelentdeckung und -produktion. CRMOs oder Auftragsforschungs- und -herstellungsorganisationen sind unverzichtbar, um Generikaherstellern dabei zu helfen, diese Erwartungen zu erfüllen, da sie spezialisierte Dienstleistungen anbieten. Pharmaunternehmen lagern aufgrund eingeschränkter gesetzlicher Anforderungen, der zunehmenden Komplexität der Arzneimittelforschungsverfahren und der Notwendigkeit innovativer Fertigungstechnologien verschiedene Phasen ihrer Betriebsabläufe aus.
Einschränkungen/Herausforderungen
- Sicherstellung und Aufrechterhaltung hoher Qualitätsstandards
Die strengen Qualitätskontrollprozesse bei der Herstellung injizierbarer Medikamente erfordern in jeder Phase akribische Aufmerksamkeit für Details. Die Einhaltung dieser Standards erfordert erhebliche Investitionen in Technologie, Infrastruktur und Fachpersonal, was zu höheren Produktionskosten führen kann. Darüber hinaus können die strengen Compliance-Anforderungen auch die Markteinführungszeit neuer injizierbarer Medikamente verlängern. Trotz dieser Herausforderungen ist die Verpflichtung zur Aufrechterhaltung hoher Qualität unerlässlich, um die Patientensicherheit zu gewährleisten und die Integrität der Gesundheitspraktiken aufrechtzuerhalten.
Trotz der Herausforderungen, die sich durch Einschränkungen bei der Qualitätssicherung ergeben, ist dies ein zentraler Aspekt, der das unermüdliche Engagement der Branche unterstreicht, sichere und wirksame injizierbare Medikamente bereitzustellen. Dieses Engagement spielt eine grundlegende Rolle bei der Sicherung des Vertrauens und des Wohlbefindens der Patienten weltweit.
- Logistik aufgrund spezieller Lager- und Transportanforderungen
Generika werden häufig von mehreren Herstellern hergestellt, was zu unterschiedlichen Rezepturen und Verpackungen führt. Obwohl Generika in verschiedenen Rezepturen erhältlich sind, können sie bei Lagerung und Transport anfälliger für Feuchtigkeits- und Temperaturschwankungen sein. Das Problem ergibt sich aus der Möglichkeit, dass einige Generika, insbesondere solche mit besonderen Stabilitätsanforderungen, möglicherweise spezielle Lagerbedingungen erfordern, um ihre Wirksamkeit und Sicherheit zu bewahren.
Bestimmte komplexe Rezepturen und Generika können empfindlich auf Temperaturschwankungen und Lichteinwirkung reagieren. Die Unversehrtheit dieser Medikamente kann durch unsachgemäße Lagerung beeinträchtigt werden, was zu einer verminderten therapeutischen Wirksamkeit oder sogar zu Sicherheitsproblemen bei der Verabreichung führen kann. Darüber hinaus sind Großhändler und Distributoren nur zwei der zahlreichen Zwischenhändler, die häufig an den weltweiten Vertriebsnetzen für Generika beteiligt sind. Ungünstige Lagerbedingungen stellen in jeder Phase der Lieferkette ein Risiko dar. Dies wird besonders wichtig in Gebieten mit weniger entwickelter Infrastruktur oder ungleichmäßiger Temperaturregelung beim Transport.
Jüngste Entwicklungen
- Im Januar 2024 haben Sun Pharmaceutical Industries Limited und Taro Pharmaceutical Industries Ltd. offiziell eine endgültige Fusionsvereinbarung geschlossen. Im Rahmen dieser Vereinbarung wird Sun Pharma als Mehrheitsaktionär von Taro alle ausstehenden Stammaktien von Taro erwerben, mit Ausnahme derjenigen, die bereits von Sun Pharma oder seinen Tochtergesellschaften gehalten werden. Der Erwerb erfolgt zu einem Barpreis von 43,00 USD pro Aktie ohne Zinsen. Diese Fusion soll ein robusteres und wettbewerbsfähigeres Unternehmen schaffen und potenzielle Vorteile wie eine erhöhte Marktpräsenz, betriebliche Effizienz und erweiterte Kapazitäten für Sun Pharma und Taro Pharmaceutical Industries Ltd. mit sich bringen.
- Im November 2023 führte Fresenius Kabi Tyenne, sein Biosimilar von Tocilizumab, das auf RoActemra (Tocilizumab) verweist, in der Europäischen Union ein. Tyenne ist das erste Tocilizumab-Biosimilar in Europa zur Behandlung verschiedener entzündlicher und immunologischer Erkrankungen. Es erweitert seine Produktpalette
- Im August 2023 erhielt Aurobindo Pharma von der US-amerikanischen Food and Drug Administration (USFDA) die endgültige Genehmigung für die Herstellung und Vermarktung von Vancomycin Hydrochloride for Injection USP in Einzeldosisfläschchen mit Stärken von 1,25 g/Fläschchen und 1,5 g/Fläschchen. Diese Formulierungen sind bioäquivalent und therapeutisch gleichwertig mit dem Referenzarzneimittel (RLD), Vancomycin Hydrochloride for Injection USP, hergestellt von Mylan Laboratories Ltd.
- Im Juni 2023 kündigte Dr. Reddy's Laboratories Ltd. die Eröffnung seiner neuen, dedizierten Abteilung „RGenX“ an und damit seinen Eintritt in den indischen kommerziellen Generikamarkt. Dr. Reddy glaubt, dass dies den Patienten erschwinglichere und bessere Zugangsmöglichkeiten zu einer größeren Produktauswahl bieten wird. Das neue Unternehmen wird das Ziel des Unternehmens voranbringen, bis 2030 mehr als 1,5 Milliarden Patienten zu versorgen. Dies hat dem Unternehmen geholfen, sein Geschäft mit der Produktverfügbarkeit zu erweitern
- Im Dezember 2023 führte Hikma Pharmaceuticals PLC die Phenylephrin-HCl-Injektion USP ein, die in den Dosierungen 500 mcg/5 ml und 1.000 mcg/10 ml erhältlich ist. Dieses Produkt ist jetzt in den Vereinigten Staaten in gebrauchsfertigen Fläschchen erhältlich. Es soll den Blutdruck bei Erwachsenen erhöhen, die an klinisch signifikanter Hypotonie leiden, die hauptsächlich durch eine Gefäßerweiterung während der Anästhesie verursacht wird. Dies half dem Unternehmen, seinen Markt zu erweitern.
Marktumfang für generische Injektionsmittel in Indien und Europa
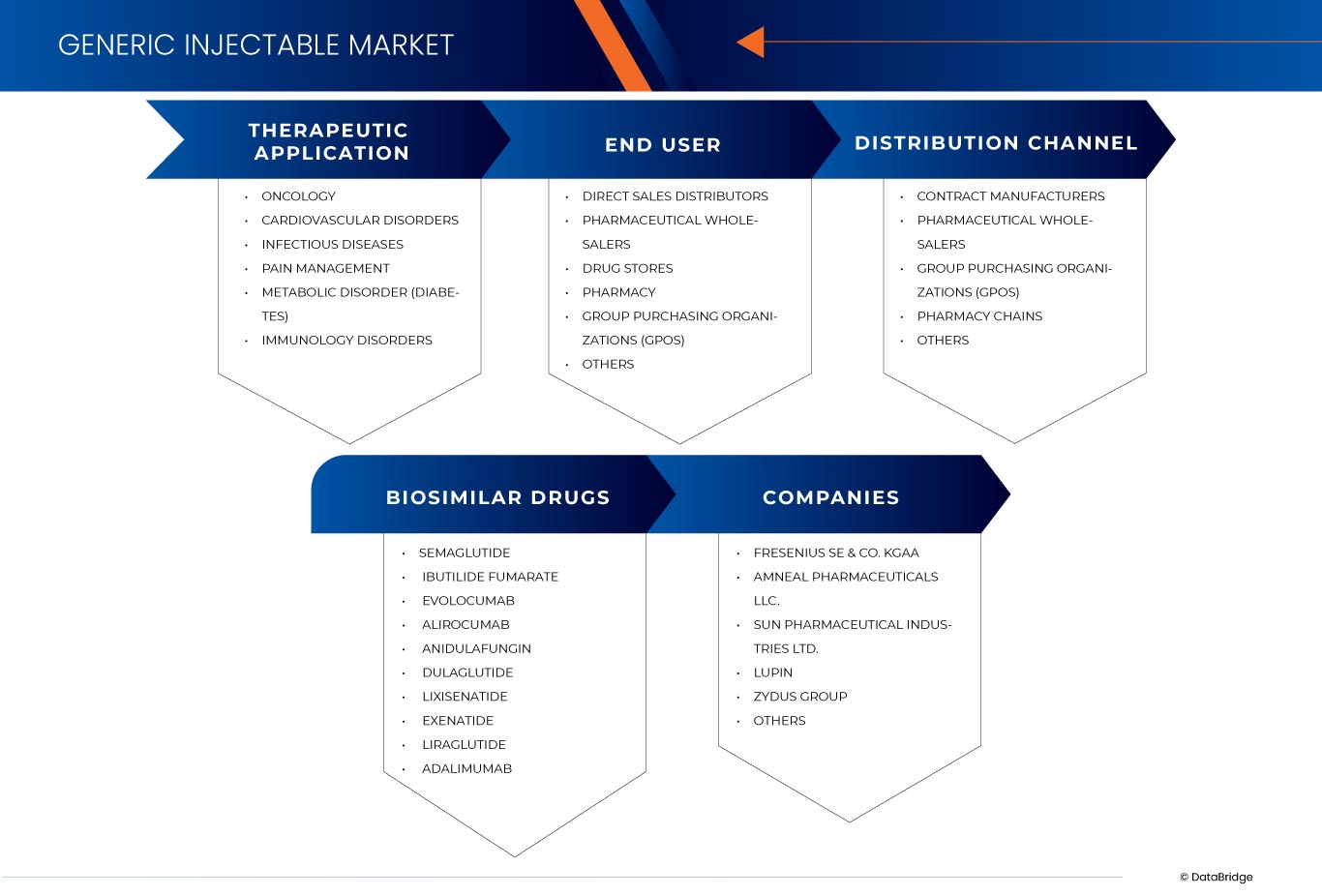
Der indische und europäische Markt für generische Injektionspräparate ist in drei wichtige Segmente unterteilt, die auf therapeutischer Anwendung, Endverbraucher, Biosimilar-Medikamenten und Vertriebskanälen basieren. Das Wachstum dieser Segmente hilft Ihnen bei der Analyse schwacher Wachstumssegmente in den Branchen und bietet den Benutzern einen wertvollen Marktüberblick und Markteinblicke, die ihnen bei der strategischen Entscheidungsfindung zur Identifizierung der wichtigsten Marktanwendungen helfen.
Therapeutische Anwendung
- Onkologie
- Herz-Kreislauf-Erkrankungen
- Infektionskrankheiten
- Schmerztherapie
- Stoffwechselstörung (Diabetes)
- Immunologische Störungen
Auf der Grundlage der therapeutischen Anwendung ist der Markt in Onkologie, Herz-Kreislauf-Erkrankungen, Infektionskrankheiten, Schmerzbehandlung, Stoffwechselstörungen (Diabetes) und immunologische Erkrankungen segmentiert.
Biosimilar-Medikamente
- Semaglutid
- Ibutidlidfumarat
- Evolocumab
- Alirocumab
- Anidulafungin
- Exenatid
- Lixisenatid
- Dulaglutid
- Adalimumab
Auf der Grundlage von Biosimilar-Arzneimitteln ist der Markt in Semaglutid, Ibutilidfumarat, Evolocumab, Alirocumab, Anidulafungin, Exenatid, Lixisenatid, Dulaglutid und Adalimumab segmentiert.
Endbenutzer
- Direktvertriebshändler
- Pharmazeutische Großhändler
- Drogerien
- Apotheke
- Einkaufsgemeinschaften (GPOs)
- Sonstiges
Auf der Grundlage des Endverbrauchers ist der Markt in Direktvertriebshändler, Pharmagroßhändler, Drogerien, Apotheken, Einkaufsgemeinschaften (GPOs) und andere segmentiert.
Vertriebskanal
- Pharmazeutische Großhändler
- Auftragshersteller
- Apothekenketten
- Einkaufsgemeinschaften (GPOs)
- Sonstiges
Auf der Grundlage der Vertriebskanäle ist der Markt in Pharmagroßhändler, Auftragshersteller, Apothekenketten, Group Purchasing Organizations (GPOs) und andere segmentiert.
Regionale Analyse/Einblicke zum Markt für generische Injektionsmittel in Indien und Europa
Der indische und europäische Markt für generische Injektionsmittel wird analysiert und es werden Erkenntnisse und Trends zur Marktgröße nach therapeutischer Anwendung, Endverbraucher, Biosimilar-Medikamenten und Vertriebskanälen bereitgestellt.
Die in diesem Marktbericht abgedeckten Länder/Regionen sind Indien und Europa.
Es wird erwartet, dass Europa den Markt für injizierbare Generika in Indien und Europa dominieren wird, da in der Region technologische Fortschritte bei injizierbaren Generikamolekülen erzielt werden.
Der Länderabschnitt des Berichts enthält auch einzelne marktbeeinflussende Faktoren und Änderungen der Marktregulierung, die sich auf die aktuellen und zukünftigen Trends des Marktes auswirken. Datenpunkte wie die Analyse der nachgelagerten und vorgelagerten Wertschöpfungskette, technische Trends, Porters Fünf-Kräfte-Analyse und Fallstudien sind einige der Hinweise, die zur Prognose des Marktszenarios für einzelne Länder verwendet werden. Bei der Bereitstellung einer Prognoseanalyse der Länderdaten werden auch die Präsenz und Verfügbarkeit regionaler/nationaler Marken und ihre Herausforderungen aufgrund großer oder geringer Konkurrenz durch lokale und inländische Marken, die Auswirkungen inländischer Zölle und Handelsrouten berücksichtigt.
Markt für generische Injektionsmittel in Indien und Europa: Wettbewerbslandschaft und Marktanteilsanalyse
Die Wettbewerbslandschaft des indischen und europäischen Marktes für generische injizierbare Arzneimittel liefert Einzelheiten zu den einzelnen Wettbewerbern. Die enthaltenen Einzelheiten umfassen Unternehmensübersicht, Unternehmensfinanzen, erzielten Umsatz, Marktpotenzial, Investitionen in Forschung und Entwicklung, neue Marktinitiativen, regionale Präsenz, Produktionsstandorte und -anlagen, Produktionskapazitäten, Stärken und Schwächen des Unternehmens, Produkteinführung, Produktbreite und -umfang, Anwendungsdominanz. Die oben angegebenen Datenpunkte beziehen sich nur auf den Fokus der Unternehmen auf den Markt.
Zu den wichtigsten Akteuren auf dem indischen und europäischen Markt für generische Injektionspräparate zählen unter anderem Cipla Inc., Dr. Reddy's Laboratories Ltd, Sanofi, Viatris Inc., Fresenius Kabi AG, Sandoz Group AG, GLENMARK PHARMACEUTICALS LTD, Gland Pharma Limited, Par Pharmaceutical und Sun Pharmaceutical Industries Ltd.
SKU-
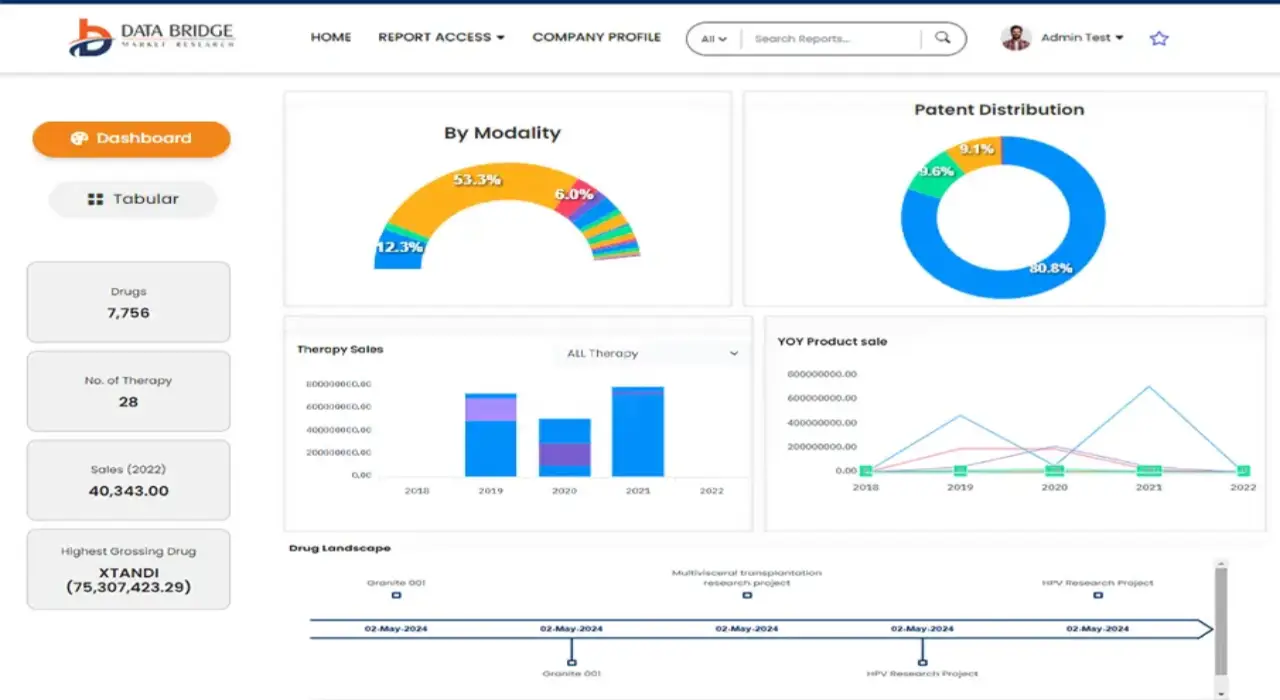
Erhalten Sie Online-Zugriff auf den Bericht zur weltweit ersten Market Intelligence Cloud
- Interaktives Datenanalyse-Dashboard
- Unternehmensanalyse-Dashboard für Chancen mit hohem Wachstumspotenzial
- Zugriff für Research-Analysten für Anpassungen und Abfragen
- Konkurrenzanalyse mit interaktivem Dashboard
- Aktuelle Nachrichten, Updates und Trendanalyse
- Nutzen Sie die Leistungsfähigkeit der Benchmark-Analyse für eine umfassende Konkurrenzverfolgung
Inhaltsverzeichnis
1 INTRODUCTION
1.1 OBJECTIVES OF THE STUDY
1.2 MARKET DEFINITION
1.3 OVERVIEW OF INDIA AND EUROPE GENERIC INJECTABLE MARKET
1.4 LIMITATIONS
1.5 MARKETS COVERED
2 MARKET SEGMENTATION
2.1 MARKETS COVERED
2.2 YEARS CONSIDERED FOR THE STUDY
2.3 CURRENCY AND PRICING
2.4 DBMR TRIPOD DATA VALIDATION MODEL
2.5 INDIA MULTIVARIATE MODELLING
2.6 TYPE LIFELINE CURVE
2.7 PRIMARY INTERVIEWS WITH KEY OPINION LEADERS
2.8 VENDOR SHARE ANALYSIS
2.9 SECONDARY SOURCES
2.1 ASSUMPTIONS
3 EXECUTIVE SUMMARY
4 PREMIUM INSIGHTS
4.1 PESTAL ANALYSIS
4.1.1 EUROPE
4.1.2 INDIA
4.2 PORTER FIVE FORCED
4.2.1 EUROPE
4.2.2 INDIA
4.3 EPIDEMIOLOGY
5 EUROPE GENERIC INJECATBLE MARKET OVERVIEW
5.1 DRIVERS
5.1.1 SURGE IN DEVELOPMENT AND PRODUCTION OF GENERIC INJECTABLE
5.1.2 PIONEERING PROGRESS FUELED BY TECHNOLOGICAL ADVANCEMENTS IN DRUG MOLECULES
5.1.3 SURGE OF GENERIC INJECTABLE MARKET AMIDST THE ESCALATING PREVALENCE OF CHRONIC DISEASES
5.2 RESTRAINTS
5.2.1 ENSURING AND MAINTAINING HIGH-QUALITY STANDARDS
5.2.2 ENSURING THE QUALIFICATION AND ETHICAL STANDARDS OF A CONTRACT MANUFACTURING ORGANIZATION (CMO)
5.2.3 NAVIGATING MARKET CHALLENGES IN THE DEVELOPMENT COSTS OF GENERIC INJECTABLE
5.3 OPPORTUNITIES
5.3.1 ASCENDANCE OF MARKET GROWTH THROUGH INCREASED EMPHASIS ON CONTRACT RESEARCH MANUFACTURING
5.3.2 SYNERGIZING INNOVATION THROUGH COLLABORATIVE DRUG RESEARCH AND DEVELOPMENT
5.3.3 EXPANSION IN MARKET GROWTH FUELED BY RISING PREFERENCE FOR GENERIC DRUGS OVER NOVEL ALTERNATIVES
5.3.4 EXPANDING HORIZONS PROPELLED BY GROWING PIPELINE OF INNOVATIVE PRODUCTS
5.4 CHALLENGES
5.4.1 LOGISTICAL CHALLENGES DUE TO SPECIALIZED STORAGE AND TRANSPORTATION NEEDS
6 INDIA GENERIC INJECATBLE MARKET OVERVIEW
6.1 DRIVERS
6.1.1 ESCALATING INCIDENCE OF CHRONIC DISEASES
6.1.2 DEPENDENCE ON THE INDIAN MANUFACTURERS FOR GENERIC VERSION
6.1.3 AVAILABILITY OF A WIDE VARIETY OF DISTRIBUTION CHANNELS
6.2 RESTRAINTS
6.2.1 ELEVATED STANDARDS OF QUALITY ASSURANCE IN GENERIC INJECTABLE
6.3 OPPORTUNITIES
6.3.1 MARKET EXPANSION SURGING WITH A HEIGHTENED FOCUS ON CONTRACT RESEARCH MANUFACTURING ORGANIZATION
6.3.2 HARMONIZING INNOVATION BY COLLABORATIVE EFFORTS IN DRUG RESEARCH AND DEVELOPMENT
6.3.3 MARKET GROWTH EXPANDS DUE TO INCREASING FAVOR FOR GENERIC DRUGS INSTEAD OF NOVEL ALTERNATIVES
6.3.4 GOVERNMENT DRIVE AND ADVOCACY FOR GENERIC MEDICATIONS
6.4 CHALLENGES
6.4.1 CHALLENGES IN LOGISTICS ARISING FROM SPECIALIZED STORAGE AND TRANSPORTATION REQUIREMENTS
7 INDIA & EUROPE INJECTABLE DRUG DELIVERY MARKET, BY THERAPEUTIC APPLICATION
7.1 OVERVIEW
7.2 ONCOLOGY
7.3 CARDIOVASCULAR DISORDERS
7.4 INFECTIOUS DISEASES
7.5 PAIN MANAGEMENT
7.6 METABOLIC DISORDERS (DIABETES)
7.7 IMMUNOLOGY DISORDERS
8 INDIA & EUROPE INJECTABLE DRUG DELIVERY MARKET, BY BIOSIMILAR DRUGS
8.1 OVERVIEW
8.2 SEMAGLUTIDE
8.3 IBUTILIDE FUMARATE
8.4 EVOLOCUMAB
8.5 ALIROCUMAB
8.6 ANIDULAFUNGIN
8.7 DULAGLUTIDE
8.8 LIXISENATIDE
8.9 EXENATIDE
8.1 LIRAGLUTIDE
8.11 ADALIMUMAB
9 INDIA & EUROPE INJECTABLE DRUG DELIVERY MARKET, BY END USER
9.1 OVERVIEW
9.2 DIRECT SALES DISTRIBUTORS
9.3 PHARMACEUTICAL WHOLESALERS
9.4 DRUG STORES
9.5 PHARMACY
9.6 GROUP PURCHASING ORGANIZATIONS (GPOS)
9.7 OTHERS
10 INDIA & EUROPE INJECTABLE DRUG DELIVERY MARKET, BY DISTRIBUTION CHANNEL
10.1 OVERVIEW
10.2 CONTRACT MANUFACTURERS
10.3 PHARMACEUTICAL WHOLESALERS
10.4 PHARMACY CHAINS
10.5 GROUP PURCHASING ORGANIZATIONS (GPOS)
10.6 OTHERS
11 INDIA AND EUROPE GENERIC INJECTABLE MARKET: COMPANY LANDSCAPE
11.1 COMPANY SHARE ANALYSIS: EUROPE
11.2 COMPANY SHARE ANALYSIS: INDIA
12 SWOT ANALYSIS
12.1 CONTRACT MANUFACTURERS
12.2 MANUFACTURERS
12.3 DISTRIBUTORS
13 COMPANY PROFILE (CONTRACT MANUFACTURERS)
13.1 BOEHRINGER INGELHEIM INTERNATIONAL GMBH
13.1.1 COMPANY SNAPSHOT
13.1.2 PRODUCT PORTFOLIO
13.1.3 RECENT DEVELOPMENT
13.2 CARDINAL HEALTH
13.2.1 COMPANY SNAPSHOT
13.2.2 REVENUE ANALYSIS
13.2.3 PRODUCT PORTFOLIO
13.2.4 RECENT DEVELOPMENT
13.3 DIVI'S LABORATORIES LIMITED.
13.3.1 COMPANY SNAPSHOT
13.3.2 REVENUE ANALYSIS
13.3.3 PRODUCT PORTFOLIO
13.3.4 RECENT DEVELOPMENT
13.4 DR. REDDY’S LABORATORIES LTD
13.4.1 COMPANY SNAPSHOT
13.4.2 REVENUE ANALYSIS
13.4.3 PRODUCT PORTFOLIO
13.4.4 RECENT DEVELOPMENT
13.5 FAREVA
13.5.1 COMPANY SNAPSHOT
13.5.2 PRODUCT PORTFOLIO
13.5.3 RECENT DEVELOPMENT
13.6 HIKMA PHARMACEUTICALS PLC
13.6.1 COMPANY SNAPSHOT
13.6.2 REVENUE ANALYSIS
13.6.3 PRODUCT PORTFOLIO
13.6.4 RECENT DEVELOPMENTS
13.7 INNOVEXIA LIFESCIENCES PVT LTD
13.7.1 COMPANY SNAPSHOT
13.7.2 PRODUCT PORTFOLIO
13.7.3 RECENT DEVELOPMENT
13.8 MEDLOCK HEALTHCARE
13.8.1 COMPANY SNAPSHOT
13.8.2 PRODUCT PORTFOLIO
13.8.3 RECENT DEVELOPMENT
13.9 RECIPHARM AB.
13.9.1 COMPANY SNAPSHOT
13.9.2 PRODUCT PORTFOLIO
13.9.3 RECENT DEVELOPMENT
13.1 SWISSCHEM
13.10.1 COMPANY SNAPSHOT
13.10.2 PRODUCT PORTFOLIO
13.10.3 RECENT DEVELOPMENT
13.11 TEVA PHARMACEUTICAL INDUSTRIES LTD
13.11.1 COMPANY SNAPSHOT
13.11.2 REVENUE ANALYSIS
13.11.3 PRODUCT PORTFOLIO
13.11.4 RECENT DEVELOPMENT
13.12 VENUS PHARMA GMBH.
13.12.1 COMPANY SNAPSHOT
13.12.2 PRODUCT PORTFOLIO
13.12.3 RECENT DEVELOPMENT
13.13 ZYDUS GROUP
13.13.1 COMPANY SNAPSHOT
13.13.2 REVENUE ANALYSIS
13.13.3 PRODUCT PORTFOLIO
13.13.4 RECENT DEVELOPMENT
14 COMPANY PROFILES (DISTRIBUTORS)
14.1 AAH PHARMACEUTICALS LTD
14.1.1 COMPANY SNAPSHOT
14.1.2 PRODUCT DESCRIPTION
14.1.3 RECENT DEVELOPMENT
14.2 HENRY SCHEIN, INC.
14.2.1 COMPANY SNAPSHOT
14.2.2 REVENUE ANALYSIS
14.2.3 PRODUCT PORTFOLIO
14.2.4 RECENT DEVELOPMENT
14.3 MAWDSLEYS – BROOKS & CO. LTD.
14.3.1 COMPANY SNAPSHOT
14.3.2 PRODUCT DESCRIPTION
14.3.3 RECENT DEVELOPMENT
14.4 MEDLINE INDUSTRIES, LP.
14.4.1 COMPANY SNAPSHOT
14.4.2 PRODUCT PORTFOLIO
14.4.3 RECENT DEVELOPMENT
15 COMPANY PROFILES (GENERIC MANUFACTURERS)
15.1 FRESENIUS SE & CO. KGAA
15.1.1 COMPANY SNAPSHOT
15.1.2 REVENUE ANALYSIS
15.1.3 PRODUCT PORTFOLIO
15.1.4 RECENT DEVELOPMENT
15.2 AMNEAL PHARMACEUTICALS LLC
15.2.1 COMPANY SNAPSHOT
15.2.2 REVENUE ANALYSIS
15.2.3 PRODUCT PORTFOLIO
15.2.4 RECENT DEVELOPMENT
15.3 SUN PHARMACEUTICAL INDUSTRIES LTD.
15.3.1 COMPANY SNAPSHOT
15.3.2 REVENUE ANALYSIS
15.3.3 PRODUCT PORTFOLIO
15.3.4 RECENT DEVELOPMENT
15.4 LUPIN.
15.4.1 COMPANY SNAPSHOT
15.4.2 REVENUE ANALYSIS
15.4.3 PRODUCT PORTFOLIO
15.4.4 RECENT DEVELOPMENT
15.5 ZYDUS GROUP
15.5.1 COMPANY SNAPSHOT
15.5.2 REVENUE ANALYSIS
15.5.3 PRODUCT PORTFOLIO
15.5.4 RECENT DEVELOPMENT
15.6 AUROBINDO PHARMA.
15.6.1 COMPANY SNAPSHOT
15.6.2 REVENUE ANALYSIS
15.6.3 PRODUCT PORTFOLIO
15.6.4 RECENT DEVELOPMENTS
15.7 CIPLA INC.
15.7.1 COMPANY SNAPSHOT
15.7.2 REVENUE ANALYSIS
15.7.3 PRODUCT PORTFOLIO
15.7.4 RECENT DEVELOPMENTS
15.8 CONCORD BIOTECH.
15.8.1 COMPANY SNAPSHOT
15.8.2 REVENUE ANALYSIS
15.8.3 PRODUCT PORTFOLIO
15.8.4 RECENT DEVELOPMENT
15.9 DR. REDDY’S LABORATORIES LTD
15.9.1 COMPANY SNAPSHOT
15.9.2 REVENUE ANALYSIS
15.9.3 PRODUCT PORTFOLIO
15.9.4 RECENT DEVELOPMENT
15.1 GLAND PHARMA LIMITED
15.10.1 COMPANY SNAPSHOT
15.10.2 SOURCE: COMPANY WEBSITE, ANNUAL REPORTS, AND SEC FILING
15.10.3 REVENUE ANALYSIS
15.10.4 PRODUCT PORTFOLIO
15.10.5 RECENT DEVELOPMENT
15.11 GLENMARK PHARMACEUTICALS LTD
15.11.1 COMPANY SNAPSHOT
15.11.2 REVENUE ANALYSIS
15.11.3 PRODUCT PORTFOLIO
15.11.4 RECENT DEVELOPMENT
15.12 HIKMA PHARMACEUTICALS PLC
15.12.1 COMPANY SNAPSHOT
15.12.2 REVENUE ANALYSIS
15.12.3 PRODUCT PORTFOLIO
15.12.4 RECENT DEVELOPMENTS
15.13 INTAS PHARMACEUTICALS LTD.
15.13.1 COMPANY SNAPSHOT
15.13.2 PRODUCT PORTFOLIO
15.13.3 RECENT DEVELOPMENT
15.14 PAR PHARMACEUTICAL.
15.14.1 COMPANY SNAPSHOT
15.14.2 PRODUCT PORTFOLIO
15.14.3 RECENT DEVELOPMENT
15.15 SANDOZ GROUP AG
15.15.1 COMPANY SNAPSHOT
15.15.2 REVENUE ANALYSIS
15.15.3 PRODUCT PORTFOLIO
15.15.4 RECENT DEVELOPMENT
15.16 SANOFI
15.16.1 COMPANY SNAPSHOT
15.16.2 REVENUE ANALYSIS
15.16.3 PRODUCT PORTFOLIO
15.16.4 RECENT DEVELOPMENT
15.17 VIATRIS INC.
15.17.1 COMPANY SNAPSHOT
15.17.2 REVENUE ANALYSIS
15.17.3 PRODUCT PORTFOLIO
15.17.4 RECENT DEVELOPMENT
16 QUESTIONNAIRE
17 RELATED REPORTS
18 REFERENCES
Tabellenverzeichnis
TABLE 1 INDIA GENERIC INJECTABLE MARKET, BY THERAPEUTIC APPLICATION, 2022-2035 (USD MILLION)
TABLE 2 EUROPE GENERIC INJECTABLE MARKET, BY THERAPEUTIC APPLICATION, 2022-2035 (USD MILLION)
TABLE 3 EUROPE ONCOLOGY IN GENERIC INJECTABLE MARKET, BY DRUGS, 2022-2035 (USD MILLION)
TABLE 4 EUROPE ONCOLOGY IN GENERIC INJECTABLE MARKET, BY DRUGS, 2022-2035 (USD MILLION)
TABLE 5 EUROPE CARDIOVASCULAR DISORDERS IN GENERIC INJECTABLE MARKET, BY DRUGS, 2022-2035 (USD MILLION)
TABLE 6 INDIA CARDIOVASCULAR DISORDERS IN GENERIC INJECTABLE MARKET, BY DRUGS, 2022-2035 (USD MILLION)
TABLE 7 EUROPE INFECTIOUS DISEASES IN GENERIC INJECTABLE MARKET, BY DRUGS, 2022-2035 (USD MILLION)
TABLE 8 INDIA INFECTIOUS DISEASES IN GENERIC INJECTABLE MARKET, BY DRUGS, 2022-2035 (USD MILLION)
TABLE 9 EUROPE PAIN MANAGEMENT IN GENERIC INJECTABLE MARKET, BY DRUGS, 2022-2035 (USD MILLION)
TABLE 10 INDIA PAIN MANAGEMENT IN GENERIC INJECTABLE MARKET, BY DRUGS, 2022-2035 (USD MILLION)
TABLE 11 EUROPE METABOLIC DISORDERS (DIABETES) IN GENERIC INJECTABLE MARKET, BY DRUGS, 2022-2035 (USD MILLION)
TABLE 12 INDIA METABOLIC DISORDERS (DIABETES) IN GENERIC INJECTABLE MARKET, BY DRUGS, 2022-2035 (USD MILLION)
TABLE 13 EUROPE IMMUNOLOGY IN GENERIC INJECTABLE MARKET, BY DRUGS, 2022-2035 (USD MILLION)
TABLE 14 INDIA IMMUNOLOGY IN GENERIC INJECTABLE MARKET, BY DRUGS, 2022-2035 (USD MILLION)
TABLE 15 EUROPE GENERIC INJECTABLE MARKET, BY BIOSIMILAR DRUGS, 2022-2035 (USD MILLION)
TABLE 16 INDIA GENERIC INJECTABLE MARKET, BY BIOSIMILAR DRUGS, 2022-2035 (USD MILLION)
TABLE 17 EUROPE GENERIC INJECTABLE MARKET, BY END USER, 2022-2035 (USD MILLION)
TABLE 18 INDIA GENERIC INJECTABLE MARKET, BY END USER, 2022-2035 (USD MILLION)
TABLE 19 EUROPE GENERIC INJECTABLE MARKET, BY END USER, 2022-2035 (USD MILLION)
TABLE 20 INDIA GENERIC INJECTABLE MARKET, BY END USER, 2022-2035 (USD MILLION)
TABLE 21 EUROPE GENERIC INJECTABLE MARKET, BY DISTRIBUTION CHANNEL, 2022-2035 (USD MILLION)
TABLE 22 INDIA GENERIC INJECTABLE MARKET, BY DISTRIBUTION CHANNEL, 2022-2035 (USD MILLION)
Abbildungsverzeichnis
FIGURE 1 INDIA AND EUROPE GENERIC INJECTABLE MARKET: SEGMENTATION
FIGURE 2 INDIA AND EUROPE GENERIC INJECTABLE MARKET: DATA TRIANGULATION
FIGURE 3 INDIA GENERIC INJECTABLE MARKET: DROC ANALYSIS
FIGURE 4 EUROPE GENERIC INJECTABLE MARKET: DROC ANALYSIS
FIGURE 5 INDIA GENERIC INJECTABLE MARKET: REGIONAL VS COUNTRY MARKET ANALYSIS
FIGURE 6 EUROPE GENERIC INJECTABLE MARKET: REGIONAL VS COUNTRY MARKET ANALYSIS
FIGURE 7 INDIA AND EUROPE GENERIC INJECTABLE MARKET: COMPANY RESEARCH ANALYSIS
FIGURE 8 EUROPE MULTIVARIATE MODELLING
FIGURE 9 INDIA AND EUROPE GENERIC INJECTABLE MARKET: INTERVIEW DEMOGRAPHICS
FIGURE 10 INDIA AND EUROPE GENERIC INJECTABLE MARKET: VENDOR SHARE ANALYSIS
FIGURE 11 INDIA AND EUROPE GENERIC INJECTABLE MARKET: SEGMENTATION
FIGURE 12 ESCALATING INCIDENCE OF CHRONIC DISEASES AND SURGE IN THE DEVELOPMENT AND PRODUCTION OF GENERIC INJECTABLE IS DRIVING THE GROWTH OF THE INDIA GENERIC INJECTABLE MARKET IN THE FORECAST PERIOD OF 2024 TO 2035
FIGURE 13 SURGE IN DEVELOPMENT AND PRODUCTION OF GENERIC INJECTABLE DRUGS IS EXPECTED TO DRIVE THE EUROPEAN GENERIC INJECTABLE MARKET IN THE FORECAST PERIOD OF 2024 TO 2035
FIGURE 14 ONCOLOGY SEGMENT IS EXPECTED TO ACCOUNT FOR THE LARGEST SHARE OF THE INDIA GENERIC INJECTABLE MARKET IN 2024 AND 2035
FIGURE 15 ONCOLOGY SEGMENT IS EXPECTED TO ACCOUNT FOR THE LARGEST SHARE OF THE EUROPE GENERIC INJECTABLE MARKET IN 2024 AND 2035
FIGURE 16 DRIVERS, RESTRAINTS, OPPORTUNITIES, AND CHALLENGES OF EUROPE GENERIC INJECATBLE MARKET
FIGURE 17 DRIVERS, RESTRAINTS, OPPORTUNITIES AND CHALLENGES OF INDIA GENERIC INJECATBLE MARKET
FIGURE 18 EUROPE GENERIC INJECTABLE MARKET: BY THERAPEUTIC APPLICATION, 2023
FIGURE 19 EUROPE GENERIC INJECTABLE MARKET: BY THERAPEUTIC APPLICATION, 2024-2035 (USD MILLION)
FIGURE 20 EUROPE GENERIC INJECTABLE MARKET: BY THERAPEUTIC APPLICATION, CAGR (2024-2035)
FIGURE 21 EUROPE GENERIC INJECTABLE MARKET: BY THERAPEUTIC APPLICATION, LIFELINE CURVE
FIGURE 22 INDIA GENERIC INJECTABLE MARKET: BY THERAPEUTIC APPLICATION, 2023
FIGURE 23 INDIA GENERIC INJECTABLE MARKET: BY THERAPEUTIC APPLICATION, 2024-2035 (USD MILLION)
FIGURE 24 INDIA GENERIC INJECTABLE MARKET: BY THERAPEUTIC APPLICATION, CAGR (2024-2035)
FIGURE 25 INDIA GENERIC INJECTABLE MARKET: BY THERAPEUTIC APPLICATION, LIFELINE CURVE
FIGURE 26 EUROPE GENERIC INJECTABLE MARKET: BY BIOSIMILAR DRUGS, 2023
FIGURE 27 EUROPE GENERIC INJECTABLE MARKET: BY BIOSIMILAR DRUGS, 2024-2035 (USD MILLION)
FIGURE 28 INDIA GENERIC INJECTABLE MARKET: BY BIOSIMILAR DRUGS, 2023
FIGURE 29 INDIA GENERIC INJECTABLE MARKET: BY BIOSIMILAR DRUGS, 2024-2035 (USD MILLION)
FIGURE 30 EUROPE GENERIC INJECTABLE MARKET: BY END USER, 2023
FIGURE 31 EUROPE GENERIC INJECTABLE MARKET: BY END USER, 2024-2035 (USD MILLION)
FIGURE 32 EUROPE GENERIC INJECTABLE MARKET: BY END USER, CAGR (2024-2035)
FIGURE 33 EUROPE GENERIC INJECTABLE MARKET: BY END USER, LIFELINE CURVE
FIGURE 34 INDIA GENERIC INJECTABLE MARKET: BY END USER, 2023
FIGURE 35 INDIA GENERIC INJECTABLE MARKET: BY END USER, 2024-2035 (USD MILLION)
FIGURE 36 INDIA GENERIC INJECTABLE MARKET: BY END USER, CAGR (2024-2035)
FIGURE 37 INDIA GENERIC INJECTABLE MARKET: BY END USER, LIFELINE CURVE
FIGURE 38 EUROPE GENERIC INJECTABLE MARKET: BY DISTRIBUTION CHANNEL, 2023
FIGURE 39 EUROPE GENERIC INJECTABLE MARKET: BY DISTRIBUTION CHANNEL, 2024-2035 (USD MILLION)
FIGURE 40 EUROPE GENERIC INJECTABLE MARKET: BY DISTRIBUTION CHANNEL, CAGR (2024-2035)
FIGURE 41 EUROPE GENERIC INJECTABLE MARKET: BY DISTRIBUTION CHANNEL, LIFELINE CURVE
FIGURE 42 INDIA GENERIC INJECTABLE MARKET: BY DISTRIBUTION CHANNEL, 2023
FIGURE 43 INDIA GENERIC INJECTABLE MARKET: BY DISTRIBUTION CHANNEL, 2024-2035 (USD MILLION)
FIGURE 44 INDIA GENERIC INJECTABLE MARKET: BY DISTRIBUTION CHANNEL, CAGR (2024-2035)
FIGURE 45 INDIA GENERIC INJECTABLE MARKET: BY DISTRIBUTION CHANNEL, LIFELINE CURVE
FIGURE 46 EUROPE GENERIC INJECTABLE MARKET: COMPANY SHARE 2023 (%)
FIGURE 47 INDIA GENERIC INJECTABLE MARKET: COMPANY SHARE 2023 (%)
Forschungsmethodik
Die Datenerfassung und Basisjahresanalyse werden mithilfe von Datenerfassungsmodulen mit großen Stichprobengrößen durchgeführt. Die Phase umfasst das Erhalten von Marktinformationen oder verwandten Daten aus verschiedenen Quellen und Strategien. Sie umfasst die Prüfung und Planung aller aus der Vergangenheit im Voraus erfassten Daten. Sie umfasst auch die Prüfung von Informationsinkonsistenzen, die in verschiedenen Informationsquellen auftreten. Die Marktdaten werden mithilfe von marktstatistischen und kohärenten Modellen analysiert und geschätzt. Darüber hinaus sind Marktanteilsanalyse und Schlüsseltrendanalyse die wichtigsten Erfolgsfaktoren im Marktbericht. Um mehr zu erfahren, fordern Sie bitte einen Analystenanruf an oder geben Sie Ihre Anfrage ein.
Die wichtigste Forschungsmethodik, die vom DBMR-Forschungsteam verwendet wird, ist die Datentriangulation, die Data Mining, die Analyse der Auswirkungen von Datenvariablen auf den Markt und die primäre (Branchenexperten-)Validierung umfasst. Zu den Datenmodellen gehören ein Lieferantenpositionierungsraster, eine Marktzeitlinienanalyse, ein Marktüberblick und -leitfaden, ein Firmenpositionierungsraster, eine Patentanalyse, eine Preisanalyse, eine Firmenmarktanteilsanalyse, Messstandards, eine globale versus eine regionale und Lieferantenanteilsanalyse. Um mehr über die Forschungsmethodik zu erfahren, senden Sie eine Anfrage an unsere Branchenexperten.
Anpassung möglich
Data Bridge Market Research ist ein führendes Unternehmen in der fortgeschrittenen formativen Forschung. Wir sind stolz darauf, unseren bestehenden und neuen Kunden Daten und Analysen zu bieten, die zu ihren Zielen passen. Der Bericht kann angepasst werden, um Preistrendanalysen von Zielmarken, Marktverständnis für zusätzliche Länder (fordern Sie die Länderliste an), Daten zu klinischen Studienergebnissen, Literaturübersicht, Analysen des Marktes für aufgearbeitete Produkte und Produktbasis einzuschließen. Marktanalysen von Zielkonkurrenten können von technologiebasierten Analysen bis hin zu Marktportfoliostrategien analysiert werden. Wir können so viele Wettbewerber hinzufügen, wie Sie Daten in dem von Ihnen gewünschten Format und Datenstil benötigen. Unser Analystenteam kann Ihnen auch Daten in groben Excel-Rohdateien und Pivot-Tabellen (Fact Book) bereitstellen oder Sie bei der Erstellung von Präsentationen aus den im Bericht verfügbaren Datensätzen unterstützen.