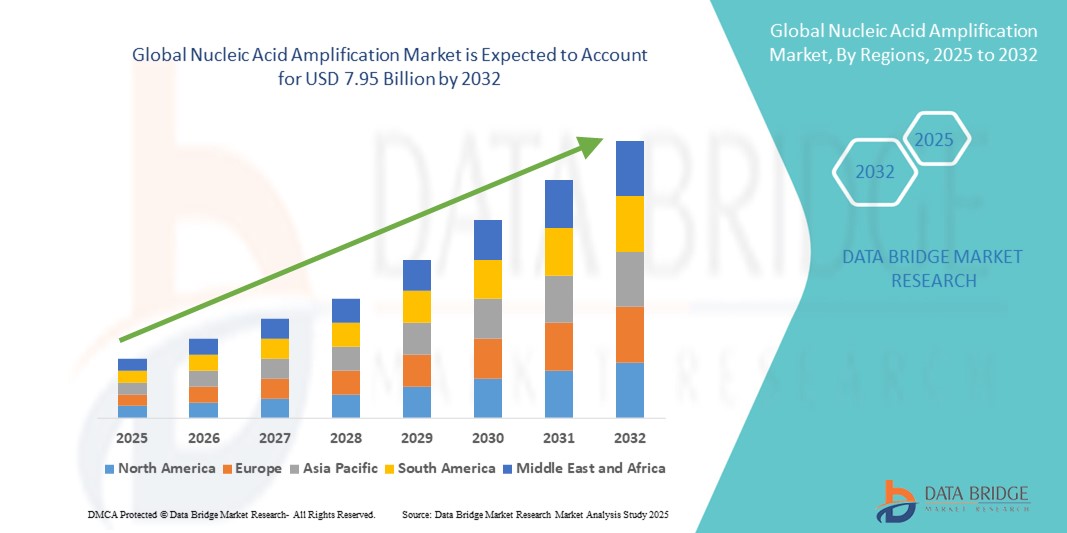
Global Nucleic Acid Amplification Market
Marktgröße in Milliarden USD
CAGR :
% 
 USD
3.90 Billion
USD
7.95 Billion
2024
2032
USD
3.90 Billion
USD
7.95 Billion
2024
2032
| 2025 –2032 | |
| USD 3.90 Billion | |
| USD 7.95 Billion | |
|
|
|
|
Globale Marktsegmentierung für Nukleinsäureamplifikation nach Anwendung (Infektionskrankheiten, Krebs, personalisierte Medizin und Genetik), Technik (Zielamplifikation, Sondenamplifikation und Signalamplifikation) – Branchentrends und Prognose bis 2032
Nukleinsäureamplifikation Marktgröße
- Der globale Markt für Nukleinsäureamplifikation wird im Jahr 2024 auf 3,90 Milliarden US-Dollar geschätzt und soll bis 2032 7,95 Milliarden US-Dollar erreichen , bei einer CAGR von 9,30 % im Prognosezeitraum.
- Das Marktwachstum wird vor allem durch die steigende Nachfrage nach schnellen, sensiblen und präzisen molekulardiagnostischen Techniken in den Bereichen Gesundheitswesen, Forschung und Forensik vorangetrieben.
- Darüber hinaus treiben Fortschritte in der Amplifikationstechnologie, die steigende Prävalenz von Infektionskrankheiten und die zunehmende Anwendung in der personalisierten Medizin die weltweite Akzeptanz voran. Diese Faktoren beschleunigen gemeinsam die Integration von Nukleinsäureamplifikationsmethoden und treiben damit die Expansion des Marktes deutlich voran.
Marktanalyse für Nukleinsäureamplifikation
- Technologien zur Nukleinsäureamplifikation ermöglichen eine schnelle und präzise Erkennung von genetischem Material und werden zu unverzichtbaren Werkzeugen in der Molekulardiagnostik, bei Tests auf Infektionskrankheiten und in der genetischen Forschung im klinischen und Laborumfeld.
- Die wachsende Nachfrage ist vor allem auf die zunehmende Verbreitung von Infektionskrankheiten, Fortschritte bei Amplifikationstechniken wie PCR und isothermischer Amplifikation sowie die zunehmende Nutzung der Molekulardiagnostik für die personalisierte Medizin und Krebserkennung zurückzuführen.
- Nordamerika dominierte den Markt für Nukleinsäureamplifikation mit dem größten Umsatzanteil von 39,4 % im Jahr 2024, unterstützt durch eine fortschrittliche Gesundheitsinfrastruktur, hohe F&E-Investitionen und die Präsenz wichtiger Akteure, die Innovationen bei diagnostischen Tests und Plattformen entwickeln.
- Der asiatisch-pazifische Raum dürfte im Prognosezeitraum aufgrund des verbesserten Zugangs zur Gesundheitsversorgung, der zunehmenden Belastung durch Infektionskrankheiten und der zunehmenden staatlichen Initiativen zur Förderung der Molekulardiagnostik die am schnellsten wachsende Region im Markt für Nukleinsäureamplifikation sein.
- Das Segment Infektionskrankheiten dominierte den Markt für Nukleinsäureamplifikation mit einem Marktanteil von 52,5 % im Jahr 2024, getrieben durch die dringende Nachfrage nach schneller Krankheitserregererkennung und Ausbruchsmanagement im klinischen Umfeld
Berichtsumfang und Marktsegmentierung für Nukleinsäureamplifikation
|
Eigenschaften |
Wichtige Markteinblicke zur Nukleinsäureamplifikation |
|
Abgedeckte Segmente |
|
|
Abgedeckte Länder |
Nordamerika
Europa
Asien-Pazifik
Naher Osten und Afrika
Südamerika
|
|
Wichtige Marktteilnehmer |
|
|
Marktchancen |
|
|
Wertschöpfungsdaten-Infosets |
Zusätzlich zu den Einblicken in Marktszenarien wie Marktwert, Wachstumsrate, Segmentierung, geografische Abdeckung und wichtige Akteure enthalten die von Data Bridge Market Research kuratierten Marktberichte auch ausführliche Expertenanalysen, Preisanalysen, Markenanteilsanalysen, Verbraucherumfragen, demografische Analysen, Lieferkettenanalysen, Wertschöpfungskettenanalysen, eine Übersicht über Rohstoffe/Verbrauchsmaterialien, Kriterien für die Lieferantenauswahl, PESTLE-Analysen, Porter-Analysen und regulatorische Rahmenbedingungen. |
Markttrends im Bereich Nukleinsäureamplifikation
Fortschritte bei Schnell- und Point-of-Care-Testtechnologien
- Ein wichtiger und sich beschleunigender Trend auf dem globalen Markt für Nukleinsäureamplifikation ist die Entwicklung und Einführung schneller, tragbarer Point-of-Care- Diagnosegeräte (POC), die zeitnahe Ergebnisse außerhalb traditioneller Laborumgebungen liefern.
- Plattformen wie GeneXpert von Cepheid und ID NOW von Abbott ermöglichen beispielsweise die schnelle Erkennung von Infektionserregern wie COVID-19 und Grippe und verbessern so die Patientenergebnisse durch schnellere klinische Entscheidungen.
- Innovationen bei isothermen Verstärkungstechniken wie LAMP (Loop-mediated Isothermal Amplification) ermöglichen eine Verstärkung ohne komplexe thermische Zyklen und machen Geräte für dezentrale Tests und Umgebungen mit begrenzten Ressourcen zugänglicher.
- Die Integration mit digitalen Gesundheitsplattformen und Cloud-basierten Datenmanagementsystemen verbessert die Ergebnisberichterstattung, die Fernüberwachung und die Möglichkeiten zur epidemiologischen Überwachung
- Dieser Trend verändert die Molekulardiagnostik, indem er dezentrale Tests ermöglicht, die Durchlaufzeiten verkürzt und die Zugänglichkeit sowohl in entwickelten als auch in aufstrebenden Märkten verbessert.
- Unternehmen wie BioFire Diagnostics und Qiagen entwickeln aktiv tragbare Lösungen zur Nukleinsäureamplifikation mit Multiplex-Testfunktionen und benutzerfreundlichen Schnittstellen und decken damit die wachsende Nachfrage nach schneller Vor-Ort-Diagnostik im Gesundheits- und öffentlichen Gesundheitssektor ab.
Marktdynamik für Nukleinsäureamplifikation
Treiber
Steigende Nachfrage aufgrund zunehmender Infektionskrankheiten und personalisierter Medizin
- Die weltweit steigende Prävalenz von Infektionskrankheiten, einschließlich neu auftretender Virusausbrüche und antibiotikaresistenter bakterieller Infektionen, ist ein wichtiger Treiber für Nukleinsäureamplifikationstechnologien, die einen empfindlichen und spezifischen Nachweis von Krankheitserregern ermöglichen.
- So erweiterte Roche Diagnostics im Jahr 2024 sein Portfolio an molekularen Tests um neue Tests zur Erkennung von Infektionserregern, die eine schnellere Identifizierung und Behandlung von Krankheiten ermöglichen.
- Die zunehmende Verbreitung personalisierter Medizin und genetischer Tests für Krebs und seltene Krankheiten treibt die Nachfrage nach präzisen Nukleinsäureamplifikationsmethoden weiter voran, die gezielte Therapien und Diagnostik unterstützen.
- Steigende Investitionen in die Gesundheitsinfrastruktur, insbesondere in Entwicklungsländern, und staatliche Initiativen zur Verbesserung der Diagnosemöglichkeiten tragen zum Marktwachstum bei
- Der Bedarf an schneller, genauer und kostengünstiger Molekulardiagnostik in klinischen, wissenschaftlichen und forensischen Anwendungen treibt die Expansion des Marktes weiter voran.
Einschränkung/Herausforderung
Technische Komplexität und regulatorische Hürden
- Die Komplexität der Nukleinsäureamplifikationstechnologien und die strengen regulatorischen Anforderungen für die Zulassung diagnostischer Tests stellen Herausforderungen für das Marktwachstum und die Produktvermarktung dar
- Hohe Kosten für moderne Geräte, Reagenzien und Fachpersonal können die Akzeptanz insbesondere in ressourcenarmen Umgebungen einschränken
- So kam es beispielsweise im Jahr 2023 bei einem führenden Diagnostikunternehmen zu Verzögerungen bei der FDA-Zulassung eines neuartigen PCR-basierten Tests aufgrund strenger Validierungsanforderungen, was sich auf den Zeitplan für die Markteinführung auswirkte.
- Darüber hinaus erfordern Probleme im Zusammenhang mit Kontaminationsrisiken, Assay-Empfindlichkeit und Reproduzierbarkeit eine kontinuierliche Qualitätskontrolle und Validierung, was den Betriebsaufwand für Labore erhöht.
- Die Bewältigung dieser Herausforderungen durch technologische Vereinfachung, Kostensenkung, optimierte Regulierungswege und eine robuste Qualitätssicherung wird für eine breitere Marktdurchdringung und nachhaltiges Wachstum von entscheidender Bedeutung sein.
Marktumfang der Nukleinsäureamplifikation
Der Markt ist nach Anwendung und Technik segmentiert.
- Nach Typ
Der Markt für Nukleinsäureamplifikation ist nach Anwendungsgebieten in die Bereiche Infektionskrankheiten, Krebs, personalisierte Medizin und Gentests unterteilt. Das Segment Infektionskrankheiten dominierte den Markt mit dem größten Umsatzanteil von 52,5 % im Jahr 2024, getrieben durch den dringenden Bedarf an schneller und präziser Erregererkennung in der klinischen Diagnostik und im Ausbruchsmanagement. Die weltweit hohe Prävalenz von Infektionskrankheiten und anhaltende Virusausbrüche sind Schlüsselfaktoren für die starke Nachfrage in diesem Segment.
Der Krebssektor dürfte zwischen 2025 und 2032 die höchste durchschnittliche jährliche Wachstumsrate verzeichnen, unterstützt durch die zunehmende Nutzung molekularer Diagnostik zur Krebsfrüherkennung, Mutationsanalyse und Therapieüberwachung. Auch die personalisierte Medizin wächst rasant, da der Fokus zunehmend auf gezielten Behandlungen auf Basis genetischer Profile liegt. Genetische Tests werden stetig ausgebaut, angetrieben durch Anwendungen im Screening und in der Erforschung von Erbkrankheiten.
- Nach Technik
Basierend auf der Technologie ist der Markt für Nukleinsäureamplifikation in Zielamplifikation, Sondenamplifikation und Signalamplifikation unterteilt. Das Segment Zielamplifikation dominierte den Markt mit einem Umsatzanteil von etwa 57 % im Jahr 2024, hauptsächlich aufgrund der weit verbreiteten Verwendung von PCR und verwandten Methoden, die spezifische DNA- oder RNA-Sequenzen für eine sensitive und spezifische Detektion amplifizieren.
Das Segment der Sondenamplifikation dürfte zwischen 2025 und 2032 die höchste durchschnittliche jährliche Wachstumsrate (CAGR) verzeichnen, da es die Detektionsspezifität durch die Amplifikation des Sondensignals anstelle der Zielsequenz verbessert. Dies ist insbesondere bei diagnostischen Anwendungen mit hohen Genauigkeitsanforderungen von Nutzen. Die Signalamplifikation dürfte aufgrund ihrer Fähigkeit, die Assay-Sensitivität zu verbessern, ohne die Zielnukleinsäure selbst zu amplifizieren, eine zunehmende Verbreitung erfahren. Dies ist insbesondere bei komplexen Probenmatrizen und Multiplex-Tests von Vorteil.
Regionale Analyse des Nukleinsäureamplifikationsmarktes
- Nordamerika dominierte den Markt für Nukleinsäureamplifikation mit dem größten Umsatzanteil von 39,4 % im Jahr 2024, unterstützt durch eine fortschrittliche Gesundheitsinfrastruktur, hohe F&E-Investitionen und die Präsenz wichtiger Akteure, die Innovationen bei diagnostischen Tests und Plattformen entwickeln.
- Gesundheitsdienstleister und Forschungseinrichtungen in der Region legen Wert auf eine schnelle und präzise Diagnostik von Infektionskrankheiten, Krebs und genetischen Störungen, unterstützt durch umfangreiche F&E-Aktivitäten und die Präsenz wichtiger Branchenakteure
- Der gut etablierte regulatorische Rahmen der Region und die zunehmende Betonung der personalisierten Medizin beschleunigen die Einführung von Nukleinsäureamplifikationstests weiter und machen Nordamerika zu einem führenden Markt für innovative molekulardiagnostische Lösungen sowohl im klinischen als auch im Forschungsumfeld.
Markteinblick in die Nukleinsäureamplifikation in den USA
Der US-Markt für Nukleinsäureamplifikation erzielte 2024 mit 39 % den größten Umsatzanteil in Nordamerika. Dies ist auf die schnelle Einführung fortschrittlicher molekulardiagnostischer Technologien und die steigende Nachfrage nach schnellen und präzisen Tests auf Infektionskrankheiten zurückzuführen. Der zunehmende Einsatz von Point-of-Care-Plattformen sowie erhöhte Investitionen in Forschung und Entwicklung im Gesundheitswesen und in die digitale Integration treiben das Marktwachstum weiter voran. Darüber hinaus verbessert die Integration von Nukleinsäureamplifikationstests mit KI-gestützter Datenanalyse und elektronischen Patientenakten die diagnostische Effizienz und die Ergebnisse erheblich.
Einblicke in den europäischen Markt für Nukleinsäureamplifikation
Der europäische Markt für Nukleinsäureamplifikation wird im Prognosezeitraum voraussichtlich stetig wachsen. Dies ist auf strenge regulatorische Standards, die zunehmende Verbreitung von Infektionskrankheiten und die steigende Nachfrage nach Krebsfrüherkennung und genetischen Tests zurückzuführen. Länder wie Deutschland und Großbritannien verzeichnen ein starkes Marktwachstum, das durch steigende staatliche Förderung der Molekulardiagnostik und die zunehmende Digitalisierung des Gesundheitswesens unterstützt wird. Die Region legt Wert auf hochwertige Diagnostik und personalisierte Medizin, was die Einführung von Nukleinsäureamplifikationstechnologien in klinischen und Forschungseinrichtungen fördert.
Markteinblick in die Nukleinsäureamplifikation in Großbritannien
Der britische Markt für Nukleinsäureamplifikation wird im Prognosezeitraum voraussichtlich mit einer bemerkenswerten jährlichen Wachstumsrate wachsen, unterstützt durch steigende Investitionen in die Genomforschung und die zunehmende Implementierung der Präzisionsmedizin. Öffentliche Gesundheitsinitiativen zur Bekämpfung von Infektionskrankheiten und zur Krebsvorsorge treiben die Nachfrage nach Nukleinsäureamplifikationstests an. Der robuste Biotechnologiesektor des Landes und die starke Gesundheitsinfrastruktur stimulieren das Wachstum zusätzlich, wobei die Point-of-Care-Molekulardiagnostik in Krankenhäusern und Kliniken zunehmend integriert wird.
Markteinblick in die Nukleinsäureamplifikation in Deutschland
Der deutsche Markt für Nukleinsäureamplifikation wird voraussichtlich deutlich wachsen, angetrieben durch den starken Fokus auf Innovationen im Gesundheitswesen und die digitale Transformation. Deutschland legt Wert auf Früherkennung von Krankheiten und präventive Gesundheitsfürsorge und fördert den Einsatz fortschrittlicher Nukleinsäureamplifikationstechnologien. Strenge Datenschutz- und Sicherheitsvorschriften führen zudem zu einer Nachfrage nach sicheren und zuverlässigen Diagnoselösungen. Die Integration mit automatisierten Laborsystemen und intelligenten Datenmanagementplattformen gewinnt in deutschen klinischen Laboren zunehmend an Bedeutung.
Markteinblicke zur Nukleinsäureamplifikation im asiatisch-pazifischen Raum
Der Markt für Nukleinsäureamplifikation im asiatisch-pazifischen Raum wird zwischen 2025 und 2032 voraussichtlich mit einer durchschnittlichen jährlichen Wachstumsrate von rund 22 % wachsen. Dies ist auf steigende Gesundheitsausgaben, eine zunehmende Belastung durch Infektionskrankheiten und die zunehmende Nutzung der Molekulardiagnostik in Ländern wie China, Indien und Japan zurückzuführen. Regierungsinitiativen zur Förderung der digitalen Gesundheitsversorgung, das wachsende Bewusstsein für personalisierte Medizin und der Ausbau der biotechnologischen Infrastruktur beschleunigen das Marktwachstum. Darüber hinaus profitiert die Region von der lokalen Herstellung von Reagenzien und Instrumenten, was die Erschwinglichkeit und Zugänglichkeit von Lösungen zur Nukleinsäureamplifikation verbessert.
Einblicke in den japanischen Markt für Nukleinsäureamplifikation
Das Wachstum des japanischen Marktes für Nukleinsäureamplifikation wird durch das fortschrittliche Gesundheitssystem des Landes, die alternde Bevölkerung und den starken Fokus auf technologische Innovation unterstützt. Die steigende Prävalenz chronischer Krankheiten und der zunehmende Einsatz molekularer Diagnostik bei Krebs und genetischen Erkrankungen steigern die Nachfrage. Die Integration der Nukleinsäureamplifikation in IoT- und KI-gesteuerte Gesundheitsüberwachungssysteme verbessert zudem die Effizienz und Genauigkeit der Diagnostik in Japan.
Markteinblick in die Nukleinsäureamplifikation in Indien
Der indische Markt für Nukleinsäureamplifikation erzielte 2024 den größten Umsatzanteil im asiatisch-pazifischen Raum. Dies ist auf die rasante Urbanisierung, den Ausbau der Gesundheitsinfrastruktur und den zunehmenden staatlichen Fokus auf die Bekämpfung von Infektionskrankheiten zurückzuführen. Die wachsende Mittelschicht und das steigende Bewusstsein für molekulare Diagnostik fördern die Akzeptanz im öffentlichen und privaten Gesundheitssektor. Der Bedarf an erschwinglichen Diagnoselösungen und die wachsenden inländischen Produktionskapazitäten beschleunigen das Marktwachstum in Indien weiter.
Marktanteile der Nukleinsäureamplifikation
Die Nukleinsäureamplifikationsbranche wird hauptsächlich von etablierten Unternehmen angeführt, darunter:
- Siemens (Deutschland)
- Hologic, Inc. (USA)
- Shenzhen Mindray Bio-Medical Electronics Co., Ltd. (China)
- Abbott (USA)
- BD (USA)
- F. Hoffmann-La Roche Ltd (Schweiz)
- Thermo Fisher Scientific Inc. (USA)
- Koninklijke Philips NV (Niederlande)
- NeuroLogica Corp. (USA)
- Shimadzu Medical (India) pvt. Ltd. (Japan)
- General Electric (USA)
- Quest Diagnostics Incorporated (USA)
- Sysmex India Pvt. Ltd. (Japan)
- Hitachi, Ltd. (Japan)
- Canon Inc. (Japan)
- FUJIFILM Holdings Corporation (Großbritannien)
- Illumina, Inc. (USA)
- Danaher Corporation (USA)
- Bio-Rad Laboratories, Inc. (USA)
- Novartis AG (Schweiz)
- Seegene Inc. (Südkorea)
Was sind die jüngsten Entwicklungen auf dem globalen Markt für Nukleinsäureamplifikation?
- Im Juni 2025 veröffentlichte bioMérieux SA einen automatisierten Nukleinsäureamplifikationstest zum Nachweis von Mykoplasmen in Zell- und Gentherapieprodukten. Dieser Test bietet eine interne Hochdurchsatzlösung auf Basis isothermer Technologie und liefert Ergebnisse in etwa einer Stunde mit minimalem technischen Aufwand.
- Im Mai 2025 unterzeichnete QIAGEN NV eine endgültige Vereinbarung zur Übernahme von Genoox, Ltd. für 80 Millionen US-Dollar (davon 70 Millionen US-Dollar in bar plus bis zu 10 Millionen US-Dollar an bedingten Zahlungen) mit dem Ziel, sein Angebot in den Bereichen klinische Genomik und Molekulardiagnostik zu erweitern.
- Im Mai 2025 demonstrierte eine neu veröffentlichte Studie einen Reverse-Transkriptase-Rekombinase-Polymerase-Amplifikationstest (RT-RPA) in Verbindung mit einer Lateral-Flow-Detektionsplattform (LFD) für den schnellen, sensitiven und spezifischen Nachweis des Dengue-Virus Serotyp 2 (DENV2). Der Test erreicht eine Nachweisgrenze von etwa 50 Kopien pro Reaktion, zeigt keine Kreuzreaktivität mit anderen gängigen Krankheitserregern und funktioniert zuverlässig unter variablen Umgebungsbedingungen.
- Im April 2025 veröffentlichten Forscher eine PCR-basierte Open-Source-Point-of-Care-Plattform, die eine 100-prozentige Sensitivität und über 98-prozentige Spezifität bei der Erkennung von Atemwegs- und HPV-Viren bietet. ROC-AUC-Werte über 0,98 machen sie zu einer hochpräzisen und kostengünstigen Alternative für die dezentrale Diagnostik.
- Im April 2025 führte Meridian Bioscience, Inc. neue Enzymstabilisierungsdienste für die Molekulardiagnostik ein, die qPCR, isotherme Amplifikation und NGS umfassen – entwickelt, um die Reagenzienstabilität zu verbessern, Formate bei Umgebungstemperatur zu ermöglichen, Arbeitsabläufe zu optimieren und Kosten zu senken
SKU-
Erhalten Sie Online-Zugriff auf den Bericht zur weltweit ersten Market Intelligence Cloud
- Interaktives Datenanalyse-Dashboard
- Unternehmensanalyse-Dashboard für Chancen mit hohem Wachstumspotenzial
- Zugriff für Research-Analysten für Anpassungen und Abfragen
- Konkurrenzanalyse mit interaktivem Dashboard
- Aktuelle Nachrichten, Updates und Trendanalyse
- Nutzen Sie die Leistungsfähigkeit der Benchmark-Analyse für eine umfassende Konkurrenzverfolgung
Forschungsmethodik
Die Datenerfassung und Basisjahresanalyse werden mithilfe von Datenerfassungsmodulen mit großen Stichprobengrößen durchgeführt. Die Phase umfasst das Erhalten von Marktinformationen oder verwandten Daten aus verschiedenen Quellen und Strategien. Sie umfasst die Prüfung und Planung aller aus der Vergangenheit im Voraus erfassten Daten. Sie umfasst auch die Prüfung von Informationsinkonsistenzen, die in verschiedenen Informationsquellen auftreten. Die Marktdaten werden mithilfe von marktstatistischen und kohärenten Modellen analysiert und geschätzt. Darüber hinaus sind Marktanteilsanalyse und Schlüsseltrendanalyse die wichtigsten Erfolgsfaktoren im Marktbericht. Um mehr zu erfahren, fordern Sie bitte einen Analystenanruf an oder geben Sie Ihre Anfrage ein.
Die wichtigste Forschungsmethodik, die vom DBMR-Forschungsteam verwendet wird, ist die Datentriangulation, die Data Mining, die Analyse der Auswirkungen von Datenvariablen auf den Markt und die primäre (Branchenexperten-)Validierung umfasst. Zu den Datenmodellen gehören ein Lieferantenpositionierungsraster, eine Marktzeitlinienanalyse, ein Marktüberblick und -leitfaden, ein Firmenpositionierungsraster, eine Patentanalyse, eine Preisanalyse, eine Firmenmarktanteilsanalyse, Messstandards, eine globale versus eine regionale und Lieferantenanteilsanalyse. Um mehr über die Forschungsmethodik zu erfahren, senden Sie eine Anfrage an unsere Branchenexperten.
Anpassung möglich
Data Bridge Market Research ist ein führendes Unternehmen in der fortgeschrittenen formativen Forschung. Wir sind stolz darauf, unseren bestehenden und neuen Kunden Daten und Analysen zu bieten, die zu ihren Zielen passen. Der Bericht kann angepasst werden, um Preistrendanalysen von Zielmarken, Marktverständnis für zusätzliche Länder (fordern Sie die Länderliste an), Daten zu klinischen Studienergebnissen, Literaturübersicht, Analysen des Marktes für aufgearbeitete Produkte und Produktbasis einzuschließen. Marktanalysen von Zielkonkurrenten können von technologiebasierten Analysen bis hin zu Marktportfoliostrategien analysiert werden. Wir können so viele Wettbewerber hinzufügen, wie Sie Daten in dem von Ihnen gewünschten Format und Datenstil benötigen. Unser Analystenteam kann Ihnen auch Daten in groben Excel-Rohdateien und Pivot-Tabellen (Fact Book) bereitstellen oder Sie bei der Erstellung von Präsentationen aus den im Bericht verfügbaren Datensätzen unterstützen.