Global Electronic Trial Master File Etmf Systems Market
Marktgröße in Milliarden USD
CAGR :
% 
 USD
1.84 Billion
USD
4.85 Billion
2024
2032
USD
1.84 Billion
USD
4.85 Billion
2024
2032
| 2025 –2032 | |
| USD 1.84 Billion | |
| USD 4.85 Billion | |
|
|
|
|
Marktsegmentierung globaler Systeme für elektronische Studienmasterdateien (eTMF) nach Komponenten (Dienstleistungen und Software), Bereitstellungsmodus (Cloud-basiertes eTMF und On-Premise-eTMF), Endnutzer (Pharma- und Biotechnologieunternehmen, CROs und andere) – Branchentrends und Prognose bis 2032
Marktgröße für elektronische Prozessmasterfile-Systeme (eTMF)
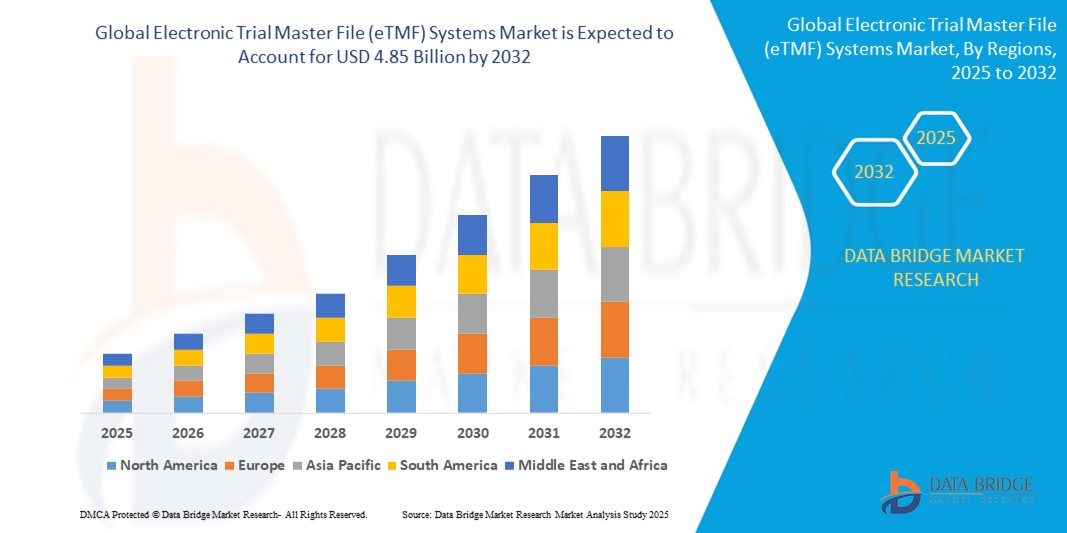
- Der globale Markt für elektronische Prozessaktenverwaltungssysteme (eTMF) hatte im Jahr 2024 einen Wert von 1,84 Milliarden US-Dollar und wird voraussichtlich bis 2032 auf 4,85 Milliarden US-Dollar anwachsen , was einer durchschnittlichen jährlichen Wachstumsrate (CAGR) von 12,90 % im Prognosezeitraum entspricht.
- Das Marktwachstum wird maßgeblich durch die steigende Nachfrage nach zentralisiertem Datenmanagement für klinische Studien, die Einhaltung regulatorischer Vorgaben und die zunehmende Nutzung digitaler Plattformen in der klinischen Forschung im pharmazeutischen und biotechnologischen Sektor angetrieben.
- Die weltweit steigende Anzahl klinischer Studien, insbesondere in Schwellenländern, und der Bedarf an Echtzeitzugriff auf Studiendokumente beschleunigen die Einführung von elektronischen Studienmasterfile-Systemen (eTMF) bei Sponsoren und Auftragsforschungsinstituten zusätzlich.
Marktanalyse für elektronische Prozessmasterfile-Systeme (eTMF)
- Der Markt für elektronische Masterdateisysteme für klinische Studien verzeichnet ein stetiges Wachstum, da Pharma- und Biotechnologieunternehmen zunehmend digitale Lösungen für das klinische Dokumentenmanagement einsetzen.
- Die zunehmende Anzahl klinischer Studien und der Bedarf an effizienten Prozessen zur Einhaltung regulatorischer Vorgaben veranlassen Organisationen dazu, von papierbasierten Systemen auf cloudbasierte Plattformen umzusteigen.
- Nordamerika dominierte 2024 mit einem Umsatzanteil von 49,5 % den Markt für elektronische Studienmasterfiles (eTMF). Gründe hierfür waren die hohe Konzentration von Pharma- und Biotechnologieunternehmen, erhebliche Investitionen in Forschung und Entwicklung, eine gut ausgebaute IT-Infrastruktur im Gesundheitswesen sowie die wachsende Zahl komplexer klinischer Studien, die eine effiziente Dokumentation und die Einhaltung der Compliance-Vorgaben erfordern.
- Die Region Asien-Pazifik dürfte die höchste Wachstumsrate auf dem globalen Markt für elektronische Prozessmasterfile-Systeme (eTMF) verzeichnen. Treiber dieser Entwicklung sind die zunehmende Urbanisierung, steigende verfügbare Einkommen, technologische Fortschritte in Ländern wie China, Japan und Indien sowie eine wachsende Neigung zu Smart Homes, die durch staatliche Digitalisierungsinitiativen unterstützt wird.
- Das Segment „Dienstleistungen“ erzielte 2024 den größten Marktanteil, da es wesentliche Leistungen über den gesamten Systemlebenszyklus hinweg anbietet, darunter Implementierung, Schulung, technischer Support und Datenmigration.
Berichtsumfang und Marktsegmentierung für elektronische Prozessmasterfile-Systeme (eTMF)
|
Attribute |
Elektronische Prozessmasterfile-Systeme (eTMF): Wichtigste Markteinblicke |
|
Abgedeckte Segmente |
|
|
Abgedeckte Länder |
Nordamerika
Europa
Asien-Pazifik
Naher Osten und Afrika
Südamerika
|
|
Wichtige Marktteilnehmer |
|
|
Marktchancen |
|
|
Mehrwertdaten-Infosets |
Zusätzlich zu Einblicken in Marktszenarien wie Marktwert, Wachstumsrate, Segmentierung, geografische Abdeckung und Hauptakteure enthalten die von Data Bridge Market Research erstellten Marktberichte auch eingehende Expertenanalysen, geografisch dargestellte Unternehmensproduktion und -kapazität, Netzwerkstrukturen von Vertriebspartnern und Partnern, detaillierte und aktualisierte Preistrendanalysen sowie Defizitanalysen der Lieferkette und der Nachfrage. |
Markttrends für elektronische Prozessmasterfile-Systeme (eTMF)
„Integration von künstlicher Intelligenz zur Workflow-Automatisierung“
- Künstliche Intelligenz wird zunehmend in elektronische Prozessaktenverwaltungssysteme integriert, um wiederkehrende Aufgaben wie die Dokumentenklassifizierung und Metadatenverschlagwortung zu automatisieren.
- Dieser Trend verbessert die Effizienz und reduziert manuelle Fehler, sodass sich Fachkräfte in der klinischen Forschung stärker auf strategische und Compliance-bezogene Aufgaben konzentrieren können.
- So können KI-gestützte Plattformen beispielsweise klinische Studiendokumente automatisch indexieren und fehlende Dateien kennzeichnen, wodurch eine höhere Genauigkeit und regulatorische Konformität gewährleistet wird.
- Unternehmen wie Veeva Systems und Phlexglobal setzen KI-Funktionen ein, um eTMF-Prozesse zu optimieren und Echtzeit-Einblicke in den Studienstatus zu gewinnen.
- Angesichts der zunehmenden Mengen klinischer Daten wird die Integration von KI unerlässlich, um die Entscheidungsfindung zu verbessern und den Lebenszyklus klinischer Studien zu beschleunigen.
Marktdynamik von Systemen für elektronische Prozessakten (eTMF)
Treiber
„Verlagerung hin zur Digitalisierung im klinischen Studienmanagement“
- Der Trend zur Digitalisierung treibt die Einführung elektronischer Masterdateisysteme für klinische Studien voran, da diese immer komplexer werden und ein effizienteres Dokumentenmanagement erfordern.
- Diese Systeme ermöglichen den zentralen Zugriff auf Prozessdokumente und damit einen schnelleren Abruf, die Zusammenarbeit in Echtzeit und eine verbesserte Versionskontrolle über alle Teams hinweg.
- Beispielsweise haben große Pharmaunternehmen wie Pfizer digitale Plattformen für das Studienmanagement eingeführt, um die Dokumentation zu optimieren und die Einhaltung regulatorischer Vorgaben sicherzustellen.
- Digitale Systeme tragen dazu bei, Risiken im Zusammenhang mit manuellen Fehlern, verloren gegangenen Dokumenten und verspäteten Einreichungen zu reduzieren und letztendlich die Qualität und die Einhaltung der Fristen von Gerichtsverfahren zu verbessern.
- Fernzugriff und sichere Cloud-Speicherfunktionen machen diese Systeme unverzichtbar für Organisationen, die ihre betriebliche Effizienz steigern und globale regulatorische Standards erfüllen wollen.
Zurückhaltung/Herausforderung
„Bedenken hinsichtlich Datensicherheit und Compliance“
- Bedenken hinsichtlich Datensicherheit und Einhaltung regulatorischer Bestimmungen stellen weiterhin große Hindernisse für die Einführung elektronischer Masterdateisysteme für klinische Studien in der gesamten klinischen Forschungsbranche dar.
- Daten aus klinischen Studien sind hochsensibel, und jede Datenschutzverletzung kann schwerwiegende Folgen haben, wie z. B. Verzögerungen der Studie, rechtliche Konsequenzen und eine Schädigung der Glaubwürdigkeit der Organisation.
- Beispielsweise führte ein gemeldeter Datenverstoß bei einer europäischen Organisation für klinische Forschung zu behördlichen Untersuchungen und Verzögerungen im Studienablauf, was die damit verbundenen Risiken unterstreicht.
- Die Einhaltung sich ständig weiterentwickelnder internationaler Vorschriften wie der Datenschutz-Grundverordnung und des Health Insurance Portability and Accountability Act (HIPAA) erfordert ständige Aktualisierungen und regionsspezifische Protokolle.
- Kleine und mittlere Unternehmen stehen oft vor der Herausforderung, die notwendige Cybersicherheitsinfrastruktur und -expertise aufzubringen, was ihre Fähigkeit einschränkt, vollständig auf cloudbasierte eTMF-Plattformen umzusteigen.
Marktübersicht für elektronische Prozessmasteraktensysteme (eTMF)
Der Markt ist segmentiert nach Komponente, Lieferart und Endnutzer.
- Nach Komponente
Basierend auf den Komponenten ist der Markt für eTMF-Systeme in Dienstleistungen und Software unterteilt. Das Segment Dienstleistungen erzielte 2024 den größten Marktanteil, da es wesentliche Leistungen über den gesamten Systemlebenszyklus hinweg anbietet, darunter Implementierung, Schulung, technischer Support und Datenmigration.
Im Softwaresegment wird von 2025 bis 2032 voraussichtlich die höchste Wachstumsrate erwartet, da Unternehmen zunehmend auf dedizierte eTMF-Plattformen für die zentrale Dokumentenverwaltung und die Einhaltung gesetzlicher Vorschriften setzen.
- Nach Lieferart
Basierend auf dem Bereitstellungsmodus ist der Markt für eTMF-Systeme in Cloud-basierte und On-Premise-eTMF-Systeme unterteilt. Das Segment der Cloud-basierten eTMF-Systeme erzielte 2024 den größten Marktanteil, was auf verbesserte Zugänglichkeit, Flexibilität, Kosteneffizienz und Skalierbarkeit zurückzuführen ist.
Das Segment der On-Premise-eTMF-Lösungen dürfte von 2025 bis 2032 die schnellste Wachstumsrate aufweisen und bleibt relevant für Organisationen, die der vollständigen Kontrolle über Datensicherheit und Infrastruktur Priorität einräumen, oft aufgrund spezifischer regulatorischer oder interner IT-Richtlinien.
- Vom Endbenutzer
Basierend auf den Endnutzern ist der Markt für eTMF-Systeme in Pharma- und Biotechnologieunternehmen, CROs und Sonstige unterteilt. Das Segment der Pharma- und Biotechnologieunternehmen hielt 2024 den größten Marktanteil, bedingt durch zunehmend komplexe klinische Studien, die Globalisierung und strenge regulatorische Anforderungen.
Bei Auftragsforschungsinstituten (CROs) wird von 2025 bis 2032 das schnellste Wachstum erwartet, da sie zunehmend eTMF-Systeme nutzen, um diverse Studien für verschiedene Sponsoren effizient zu verwalten.
Regionale Marktanalyse für elektronische Prozessmasterfile-Systeme (eTMF)
- Nordamerika dominierte 2024 mit einem Umsatzanteil von 49,5 % den Markt für elektronische Studienmasterfiles (eTMF). Gründe hierfür waren die hohe Konzentration von Pharma- und Biotechnologieunternehmen, erhebliche Investitionen in Forschung und Entwicklung, eine gut ausgebaute IT-Infrastruktur im Gesundheitswesen sowie die wachsende Zahl komplexer klinischer Studien, die eine effiziente Dokumentation und die Einhaltung der Compliance-Vorgaben erfordern.
- Strenge regulatorische Rahmenbedingungen und der Fokus auf Datenintegrität treiben die Entwicklung robuster und konformer eTMF-Lösungen voran, um die Anforderungen der FDA und anderer Gesundheitsbehörden zu erfüllen.
- Die hohe Akzeptanz fortschrittlicher Cloud-basierter Technologien und Initiativen zur digitalen Transformation in klinischen Forschungsorganisationen beschleunigt die Implementierung und Nutzung des eTMF-Systems zusätzlich.
Markteinblicke in US-amerikanische Systeme für elektronische Prozessakten (eTMF)
Der US-amerikanische Markt für eTMF-Systeme erzielte 2024 mit 81 % den größten Umsatzanteil in Nordamerika. Treiber dieses Wachstums waren strenge regulatorische Anforderungen, die zunehmende Komplexität und das wachsende Volumen klinischer Studiendaten sowie der starke Fokus auf die Auditbereitschaft. Die breite Akzeptanz cloudbasierter Lösungen und die staatliche Förderung von Forschung und Entwicklung im Gesundheitswesen treiben das Marktwachstum zusätzlich an.
Markteinblicke für elektronische Prozessmasterfile-Systeme (eTMF) in Europa
Für den europäischen Markt wird von 2025 bis 2032 das schnellste Wachstum prognostiziert. Treiber dieser Entwicklung sind die steigende Nachfrage nach Cloud-Lösungen, der Bedarf an verbessertem Datenaustausch und Zusammenarbeit zwischen den Akteuren sowie sich wandelnde regulatorische Vorgaben. Die Region profitiert zudem von einem starken Fokus auf Innovation und digitale Transformation im Bereich der Biowissenschaften.
Markteinblicke in britische Systeme für elektronische Prozessmasterakten (eTMF)
Der britische Markt für eTMF-Systeme wird voraussichtlich von 2025 bis 2032 das schnellste Wachstum verzeichnen. Treiber dieser Entwicklung ist die steigende Anzahl klinischer Studien, insbesondere der zunehmende Fokus auf dezentrale und virtuelle Studien. Die starke pharmazeutische Industrie des Landes und ein proaktiver Ansatz bei digitalen Gesundheitsinitiativen tragen zum Marktwachstum bei.
Markteinblicke in Deutschland: Elektronische Prozessmasterfile-Systeme (eTMF)
Der deutsche Markt für eTMF-Systeme wird voraussichtlich von 2025 bis 2032 das schnellste Wachstum verzeichnen. Treiber dieses Wachstums sind das steigende Bewusstsein für digitale Sicherheit, die hohen Anforderungen an die Einhaltung regulatorischer Vorgaben und die Nachfrage nach technologisch fortschrittlichen Lösungen im hochentwickelten Pharmasektor. Deutschlands Innovationsorientierung und die starke industrielle Basis fördern die Einführung von eTMF zusätzlich.
Markteinblicke für elektronische Prozessmasterfile-Systeme (eTMF) im asiatisch-pazifischen Raum
Der Markt für eTMF-Systeme im asiatisch-pazifischen Raum wird voraussichtlich von 2025 bis 2032 das schnellste Wachstum verzeichnen. Treiber dieser Entwicklung sind die zunehmende Urbanisierung, steigende verfügbare Einkommen und bedeutende technologische Fortschritte in Ländern wie China, Japan und Indien. Die wachsende Hinwendung der Region zu intelligenten klinischen Abläufen, unterstützt durch staatliche Initiativen zur Förderung der Digitalisierung, trägt zur steigenden Verbreitung von eTMF-Systemen bei.
Markteinblicke in japanische Systeme für elektronische Prozessmasterakten (eTMF).
Der japanische Markt für eTMF-Systeme wird aufgrund der hochtechnologischen Kultur des Landes, der rasanten Urbanisierung und des zunehmenden Fokus auf Datenintegrität und regulatorische Konformität voraussichtlich von 2025 bis 2032 das schnellste Wachstum verzeichnen. Sicherheit und Effizienz spielen dabei eine zentrale Rolle. Die steigende Anzahl klinischer Studien und die Integration von eTMF in andere digitale klinische Lösungen treiben die Marktakzeptanz voran.
Markteinblicke für chinesische Systeme zur elektronischen Prozessmasterakte (eTMF).
Der chinesische Markt für elektronische Myokardfibromatose-Systeme (eTMF) erzielte 2024 den größten Marktanteil im asiatisch-pazifischen Raum. Dies ist auf die wachsende Mittelschicht, die rasante Urbanisierung und die hohe Technologieakzeptanz im Gesundheitswesen zurückzuführen. China ist ein bedeutendes Zentrum für klinische Forschung. Starke inländische Hersteller und die staatliche Förderung der digitalen Transformation treiben die Verbreitung von eTMF in Privathaushalten, Unternehmen und Forschungseinrichtungen voran.
Marktanteil von Systemen für elektronische Prozessmasterakten (eTMF)
Die Branche der elektronischen Prozessaktensysteme (eTMF) wird hauptsächlich von etablierten Unternehmen angeführt, darunter:
- IQVIA Inc. (USA)
- Labcorp Arzneimittelentwicklung (USA)
- TransPerfect (USA)
- Oracle (USA)
- Phlexglobal (USA)
- SureClinical Inc. (USA)
- Aurea, Inc. (USA)
- Veeva Systems (USA)
- MasterControl Solutions, Inc. (USA)
- Clinevo Technologies (Indien)
- Mayo-Stiftung für medizinische Ausbildung und Forschung (MFMER) (USA)
- Montrium Inc. (USA)
- NCGD Inc. (USA)
- PharmaVigilance (USA)
Neueste Entwicklungen auf dem globalen Markt für elektronische Prozessmasterfile-Systeme (eTMF)
- Im Februar 2023 kooperierte Vial mit Egnyte, um die Egnyte eTMF-Lösung in seine Plattform zu integrieren. Ziel ist es, die Dokumenten- und Datenverarbeitung zu optimieren, die Einhaltung von 21 CFR Part 11 sicherzustellen und die Auditbereitschaft von Life-Science-Unternehmen zu stärken, um letztendlich die Effizienz und die Einhaltung regulatorischer Vorgaben in klinischen Studien zu verbessern.
- Im September 2022 startete Montrium von Experten geleitete TMF-Services und Schulungen. Diese Initiative soll die klinischen Abläufe und TMF-Teams während des gesamten klinischen Entwicklungsprozesses stärken und wichtige Unterstützung und Kenntnisse bereitstellen, um das Studienmanagement und die Datenintegrität im Markt zu optimieren.
- Im Juni 2022 brachte Anju Software Inc. eTMF Master auf den Markt, eine neue cloudbasierte eTMF-Software. Diese Lösung erleichtert die Zusammenarbeit zwischen Sponsoren, CROs und Studienzentren für ein effizientes und sicheres Management von Inhalten klinischer Studien unter Einhaltung regulatorischer Standards. Dadurch werden Arbeitsabläufe beschleunigt und die Compliance in der klinischen Forschung insgesamt verbessert.
- Im April 2021 kündigte Phlexglobal seine Lösung für die TMF-Qualitätsprüfung an. Das Angebot richtet sich an Pharmaunternehmen, insbesondere an globale Marktführer, und unterstützt sie bei der Bewertung und Minimierung regulatorischer Risiken bei Fusionen und Übernahmen. Dadurch wird die Inspektionsbereitschaft deutlich verbessert und die Datenqualität im gesamten Markt sichergestellt.
SKU-
Erhalten Sie Online-Zugriff auf den Bericht zur weltweit ersten Market Intelligence Cloud
- Interaktives Datenanalyse-Dashboard
- Unternehmensanalyse-Dashboard für Chancen mit hohem Wachstumspotenzial
- Zugriff für Research-Analysten für Anpassungen und Abfragen
- Konkurrenzanalyse mit interaktivem Dashboard
- Aktuelle Nachrichten, Updates und Trendanalyse
- Nutzen Sie die Leistungsfähigkeit der Benchmark-Analyse für eine umfassende Konkurrenzverfolgung
Inhaltsverzeichnis
1 INTRODUCTION
1.1 OBJECTIVES OF THE STUDY
1.2 MARKET DEFINITION
1.3 OVERVIEW OF GLOBAL ELECTRONIC TRIAL MASTER FILE (ETMF) SYSTEMS MARKET
1.4 CURRENCY AND PRICING
1.5 LIMITATION
1.6 MARKETS COVERED
2 MARKET SEGMENTATION
2.1 KEY TAKEAWAYS
2.2 ARRIVING AT THE GLOBAL ELECTRONIC TRIAL MASTER FILE (ETMF) SYSTEMS MARKET
2.2.1 VENDOR POSITIONING GRID
2.2.2 TECHNOLOGY LIFE LINE CURVE
2.2.3 MARKET GUIDE
2.2.4 COMAPANY MARKET SHARE ANALYSIS
2.2.5 MULTIVARIATE MODELLING
2.2.6 TOP TO BOTTOM ANALYSIS
2.2.7 STANDARDS OF MEASUREMENT
2.2.8 DATA POINTS FROM KEY PRIMARY INTERVIEWS
2.2.9 DATA POINTS FROM KEY SECONDARY DATABASES
2.3 GLOBAL ELECTRONIC TRIAL MASTER FILE (ETMF) SYSTEMS MARKET: RESEARCH SNAPSHOT
2.4 ASSUMPTIONS
3 MARKET OVERVIEW
3.1 DRIVERS
3.2 RESTRAINTS
3.3 OPPORTUNITIES
3.4 CHALLENGES
4 EXECUTIVE SUMMARY
5 PREMIUM INSIGHT
5.1 PORTERS FIVE FORCES
5.2 REGULATORY STANDARDS
5.3 TECHNOLOGICAL TRENDS
5.4 PATENT ANALYSIS
5.5 CASE STUDY
5.6 VALUE CHAIN ANALYSIS
5.7 COMPANY COMPARITIVE ANALYSIS
5.8 PRICING ANALYSIS
6 GLOBAL ELECTRONIC TRIAL MASTER FILE (ETMF) SYSTEMS MARKET, BY OFFERING
6.1 OVERVIEW
6.2 SOFTWARE
6.3 SERVICES
6.3.1 PROFESSIONAL SERVICES
6.3.1.1. TRAINING AND CONSULTING
6.3.1.2. IMPLEMENTATION
6.3.1.3. SUPPORT AND MAINTENANCE
6.3.2 MANAGED SERVICES
7 GLOBAL ELECTRONIC TRIAL MASTER FILE (ETMF) SYSTEMS MARKET, BY LEVEL OF DOCUMENTS
7.1 OVERVIEW
7.2 STUDY LEVEL DOCUMENTS
7.3 COUNTRY LEVEL DOCUMENTS
7.4 SITE LEVEL DOCUMENTS
8 GLOBAL ELECTRONIC TRIAL MASTER FILE (ETMF) SYSTEMS MARKET, BY OPERATING SYSTEM
8.1 OVERVIEW
8.2 WINDOWS
8.3 LINUX
8.4 MAC
8.5 MOBILE
8.5.1 ANDROID
8.5.2 IPHONE
8.5.3 IPAD
9 GLOBAL ELECTRONIC TRIAL MASTER FILE (ETMF) SYSTEMS MARKET, BY DEPLOYMENT MODE
9.1 OVERVIEW
9.2 ON PREMISES
9.3 CLOUD
9.3.1 PUBLIC
9.3.2 PRIVATE
9.3.3 HYBRID
10 GLOBAL ELECTRONIC TRIAL MASTER FILE (ETMF) SYSTEMS MARKET, BY FUNCTIONALITY
10.1 OVERVIEW
10.2 COMPREHENSIVE SECURITY
10.3 DOCUMENT UPLOADING/CREATION
10.4 AUDITING
10.5 METADATA
10.6 DOCUMENT CLASSIFICATION AND INDEXING
10.7 DOCUMENT STORAGE
10.8 DATA CAPTURING
10.9 SEARCH AND RETRIEVAL
10.1 OTHERS
11 GLOBAL ELECTRONIC TRIAL MASTER FILE (ETMF) SYSTEMS MARKET, BY PRICING MODEL
11.1 OVERVIEW
11.2 FREE
11.3 SUBSCRIPTION BASED
11.3.1 ANNUAL SUBSCRIPTION
11.3.2 MONTHLY SUBSCRIPTION
12 GLOBAL ELECTRONIC TRIAL MASTER FILE (ETMF) SYSTEMS MARKET, BY END USER
12.1 OVERVIEW
12.2 BIOTECH & PHARMA COMPANIES
12.2.1 BY OFFERING
12.2.1.1. SOFTWARE
12.2.1.2. SERVICES
12.2.1.2.1. PROFESSIONAL SERVICES
12.2.1.2.1.1 TRAINING AND CONSULTING
12.2.1.2.1.2 IMPLEMENTATION
12.2.1.2.1.3 SUPPORT AND MAINTENANCE
12.2.1.2.2. MANAGED SERVICES
12.3 CONTRACT RESEARCH ORGANIZATIONS
12.3.1 BY OFFERING
12.3.1.1. SOFTWARE
12.3.1.2. SERVICES
12.3.1.2.1. PROFESSIONAL SERVICES
12.3.1.2.1.1 TRAINING AND CONSULTING
12.3.1.2.1.2 IMPLEMENTATION
12.3.1.2.1.3 SUPPORT AND MAINTENANCE
12.3.1.2.2. MANAGED SERVICES
12.4 SPONSORS
12.4.1 BY OFFERING
12.4.1.1. SOFTWARE
12.4.1.2. SERVICES
12.4.1.2.1. PROFESSIONAL SERVICES
12.4.1.2.1.1 TRAINING AND CONSULTING
12.4.1.2.1.2 IMPLEMENTATION
12.4.1.2.1.3 SUPPORT AND MAINTENANCE
12.4.1.2.2. MANAGED SERVICES
12.5 OTHERS
13 GLOBAL ELECTRONIC TRIAL MASTER FILE (ETMF) SYSTEMS MARKET, BY GEOGRAPHY
13.1 GLOBAL ELECTRONIC TRIAL MASTER FILE (ETMF) SYSTEMS MARKET, (ALL SEGMENTATION PROVIDED ABOVE IS REPRESENTED IN THIS CHAPTER BY COUNTRY)
13.1.1 NORTH AMERICA
13.1.1.1. U.S.
13.1.1.2. CANADA
13.1.1.3. MEXICO
13.1.2 EUROPE
13.1.2.1. GERMANY
13.1.2.2. FRANCE
13.1.2.3. U.K.
13.1.2.4. ITALY
13.1.2.5. SPAIN
13.1.2.6. RUSSIA
13.1.2.7. TURKEY
13.1.2.8. BELGIUM
13.1.2.9. NETHERLANDS
13.1.2.10. NORWAY
13.1.2.11. FINLAND
13.1.2.12. SWITZERLAND
13.1.2.13. DENMARK
13.1.2.14. SWEDEN
13.1.2.15. POLAND
13.1.2.16. REST OF EUROPE
13.1.3 ASIA PACIFIC
13.1.3.1. JAPAN
13.1.3.2. CHINA
13.1.3.3. SOUTH KOREA
13.1.3.4. INDIA
13.1.3.5. AUSTRALIA
13.1.3.6. NEW ZEALAND
13.1.3.7. SINGAPORE
13.1.3.8. THAILAND
13.1.3.9. MALAYSIA
13.1.3.10. INDONESIA
13.1.3.11. PHILIPPINES
13.1.3.12. TAIWAN
13.1.3.13. VIETNAM
13.1.3.14. REST OF ASIA PACIFIC
13.1.4 SOUTH AMERICA
13.1.4.1. BRAZIL
13.1.4.2. ARGENTINA
13.1.4.3. REST OF SOUTH AMERICA
13.1.5 MIDDLE EAST AND AFRICA
13.1.5.1. SOUTH AFRICA
13.1.5.2. EGYPT
13.1.5.3. SAUDI ARABIA
13.1.5.4. U.A.E
13.1.5.5. OMAN
13.1.5.6. BAHRAIN
13.1.5.7. ISRAEL
13.1.5.8. KUWAIT
13.1.5.9. QATAR
13.1.5.10. REST OF MIDDLE EAST AND AFRICA
13.2 KEY PRIMARY INSIGHTS: BY MAJOR COUNTRIES
14 GLOBAL ELECTRONIC TRIAL MASTER FILE (ETMF) SYSTEMS MARKET,COMPANY LANDSCAPE
14.1 COMPANY SHARE ANALYSIS: GLOBAL
14.2 COMPANY SHARE ANALYSIS: NORTH AMERICA
14.3 COMPANY SHARE ANALYSIS: EUROPE
14.4 COMPANY SHARE ANALYSIS: ASIA PACIFIC
14.5 MERGERS & ACQUISITIONS
14.6 NEW PRODUCT DEVELOPMENT AND APPROVALS
14.7 EXPANSIONS
14.8 REGULATORY CHANGES
14.9 PARTNERSHIP AND OTHER STRATEGIC DEVELOPMENTS
15 GLOBAL ELECTRONIC TRIAL MASTER FILE (ETMF) SYSTEMS MARKET, SWOT & DBMR ANALYSIS
16 GLOBAL ELECTRONIC TRIAL MASTER FILE (ETMF) SYSTEMS MARKET, COMPANY PROFILE
16.1 ADLIB
16.1.1 COMPANY SNAPSHOT
16.1.2 REVENUE ANALYSIS
16.1.3 GEOGRAPHIC PRESENCE
16.1.4 PRODUCT PORTFOLIO
16.1.5 RECENT DEVELOPMENT
16.2 VEEVA MEDTECH(VEEVA SYSTEMS, INC)
16.2.1 COMPANY SNAPSHOT
16.2.2 REVENUE ANALYSIS
16.2.3 GEOGRAPHIC PRESENCE
16.2.4 PRODUCT PORTFOLIO
16.2.5 RECENT DEVELOPMENT
16.3 TRIAL INTERACTIVE
16.3.1 COMPANY SNAPSHOT
16.3.2 REVENUE ANALYSIS
16.3.3 GEOGRAPHIC PRESENCE
16.3.4 PRODUCT PORTFOLIO
16.3.5 RECENT DEVELOPMENT
16.4 MEDIDATA ( DASSAULT SYSTEMES)
16.4.1 COMPANY SNAPSHOT
16.4.2 REVENUE ANALYSIS
16.4.3 GEOGRAPHIC PRESENCE
16.4.4 PRODUCT PORTFOLIO
16.4.5 RECENT DEVELOPMENT
16.5 OCTALSOFT (GLORANT, LLC)
16.5.1 COMPANY SNAPSHOT
16.5.2 REVENUE ANALYSIS
16.5.3 GEOGRAPHIC PRESENCE
16.5.4 PRODUCT PORTFOLIO
16.5.5 RECENT DEVELOPMENT
16.6 MASTERCONTROL SOLUTIONS, INC
16.6.1 COMPANY SNAPSHOT
16.6.2 REVENUE ANALYSIS
16.6.3 GEOGRAPHIC PRESENCE
16.6.4 PRODUCT PORTFOLIO
16.6.5 RECENT DEVELOPMENT
16.7 IQVIA INC
16.7.1 COMPANY SNAPSHOT
16.7.2 REVENUE ANALYSIS
16.7.3 GEOGRAPHIC PRESENCE
16.7.4 PRODUCT PORTFOLIO
16.7.5 RECENT DEVELOPMENT
16.8 CLOUDBYZ
16.8.1 COMPANY SNAPSHOT
16.8.2 REVENUE ANALYSIS
16.8.3 GEOGRAPHIC PRESENCE
16.8.4 PRODUCT PORTFOLIO
16.8.5 RECENT DEVELOPMENT
16.9 CLINEVO TECHNOLOGIES
16.9.1 COMPANY SNAPSHOT
16.9.2 REVENUE ANALYSIS
16.9.3 GEOGRAPHIC PRESENCE
16.9.4 PRODUCT PORTFOLIO
16.9.5 RECENT DEVELOPMENT
16.1 FLORENCE HEALTHCARE
16.10.1 COMPANY SNAPSHOT
16.10.2 REVENUE ANALYSIS
16.10.3 GEOGRAPHIC PRESENCE
16.10.4 PRODUCT PORTFOLIO
16.10.5 RECENT DEVELOPMENT
16.11 ORACLE
16.11.1 COMPANY SNAPSHOT
16.11.2 REVENUE ANALYSIS
16.11.3 GEOGRAPHIC PRESENCE
16.11.4 PRODUCT PORTFOLIO
16.11.5 RECENT DEVELOPMENT
16.12 ARISGLOBAL LLC
16.12.1 COMPANY SNAPSHOT
16.12.2 REVENUE ANALYSIS
16.12.3 GEOGRAPHIC PRESENCE
16.12.4 PRODUCT PORTFOLIO
16.12.5 RECENT DEVELOPMENT
16.13 MONTRIUM INC
16.13.1 COMPANY SNAPSHOT
16.13.2 REVENUE ANALYSIS
16.13.3 GEOGRAPHIC PRESENCE
16.13.4 PRODUCT PORTFOLIO
16.13.5 RECENT DEVELOPMENT
16.14 CRUCIAL DATA SOLUTIONS
16.14.1 COMPANY SNAPSHOT
16.14.2 REVENUE ANALYSIS
16.14.3 GEOGRAPHIC PRESENCE
16.14.4 PRODUCT PORTFOLIO
16.14.5 RECENT DEVELOPMENT
16.15 KEY2COMPLIANCE AB (SYMBIOTEQ)
16.15.1 COMPANY SNAPSHOT
16.15.2 REVENUE ANALYSIS
16.15.3 GEOGRAPHIC PRESENCE
16.15.4 PRODUCT PORTFOLIO
16.15.5 RECENT DEVELOPMENT
16.16 DATARIVER S.R.L
16.16.1 COMPANY SNAPSHOT
16.16.2 REVENUE ANALYSIS
16.16.3 GEOGRAPHIC PRESENCE
16.16.4 PRODUCT PORTFOLIO
16.16.5 RECENT DEVELOPMENT
16.17 ETHICA CRO
16.17.1 COMPANY SNAPSHOT
16.17.2 REVENUE ANALYSIS
16.17.3 GEOGRAPHIC PRESENCE
16.17.4 PRODUCT PORTFOLIO
16.17.5 RECENT DEVELOPMENT
16.18 TRIALL (CLINBLOCKS B.V.)
16.18.1 COMPANY SNAPSHOT
16.18.2 REVENUE ANALYSIS
16.18.3 GEOGRAPHIC PRESENCE
16.18.4 PRODUCT PORTFOLIO
16.18.5 RECENT DEVELOPMENT
16.19 PREMIER CONSULTING
16.19.1 COMPANY SNAPSHOT
16.19.2 REVENUE ANALYSIS
16.19.3 GEOGRAPHIC PRESENCE
16.19.4 PRODUCT PORTFOLIO
16.19.5 RECENT DEVELOPMENT
16.2 PHLEXGLOBAL(A PHARMALEX COMPANY)
16.20.1 COMPANY SNAPSHOT
16.20.2 REVENUE ANALYSIS
16.20.3 GEOGRAPHIC PRESENCE
16.20.4 PRODUCT PORTFOLIO
16.20.5 RECENT DEVELOPMENT
16.21 SURECLINICAL INC.
16.21.1 COMPANY SNAPSHOT
16.21.2 REVENUE ANALYSIS
16.21.3 GEOGRAPHIC PRESENCE
16.21.4 PRODUCT PORTFOLIO
16.21.5 RECENT DEVELOPMENT
NOTE: THE COMPANIES PROFILED IS NOT EXHAUSTIVE LIST AND IS AS PER OUR PREVIOUS CLIENT REQUIREMENT. WE PROFILE MORE THAN 100 COMPANIES IN OUR STUDY AND HENCE THE LIST OF COMPANIES CAN BE MODIFIED OR REPLACED ON REQUEST
17 CONCLUSION
18 QUESTIONNAIRE
19 RELATED REPORTS
20 ABOUT DATA BRIDGE MARKET RESEARCH
Forschungsmethodik
Die Datenerfassung und Basisjahresanalyse werden mithilfe von Datenerfassungsmodulen mit großen Stichprobengrößen durchgeführt. Die Phase umfasst das Erhalten von Marktinformationen oder verwandten Daten aus verschiedenen Quellen und Strategien. Sie umfasst die Prüfung und Planung aller aus der Vergangenheit im Voraus erfassten Daten. Sie umfasst auch die Prüfung von Informationsinkonsistenzen, die in verschiedenen Informationsquellen auftreten. Die Marktdaten werden mithilfe von marktstatistischen und kohärenten Modellen analysiert und geschätzt. Darüber hinaus sind Marktanteilsanalyse und Schlüsseltrendanalyse die wichtigsten Erfolgsfaktoren im Marktbericht. Um mehr zu erfahren, fordern Sie bitte einen Analystenanruf an oder geben Sie Ihre Anfrage ein.
Die wichtigste Forschungsmethodik, die vom DBMR-Forschungsteam verwendet wird, ist die Datentriangulation, die Data Mining, die Analyse der Auswirkungen von Datenvariablen auf den Markt und die primäre (Branchenexperten-)Validierung umfasst. Zu den Datenmodellen gehören ein Lieferantenpositionierungsraster, eine Marktzeitlinienanalyse, ein Marktüberblick und -leitfaden, ein Firmenpositionierungsraster, eine Patentanalyse, eine Preisanalyse, eine Firmenmarktanteilsanalyse, Messstandards, eine globale versus eine regionale und Lieferantenanteilsanalyse. Um mehr über die Forschungsmethodik zu erfahren, senden Sie eine Anfrage an unsere Branchenexperten.
Anpassung möglich
Data Bridge Market Research ist ein führendes Unternehmen in der fortgeschrittenen formativen Forschung. Wir sind stolz darauf, unseren bestehenden und neuen Kunden Daten und Analysen zu bieten, die zu ihren Zielen passen. Der Bericht kann angepasst werden, um Preistrendanalysen von Zielmarken, Marktverständnis für zusätzliche Länder (fordern Sie die Länderliste an), Daten zu klinischen Studienergebnissen, Literaturübersicht, Analysen des Marktes für aufgearbeitete Produkte und Produktbasis einzuschließen. Marktanalysen von Zielkonkurrenten können von technologiebasierten Analysen bis hin zu Marktportfoliostrategien analysiert werden. Wir können so viele Wettbewerber hinzufügen, wie Sie Daten in dem von Ihnen gewünschten Format und Datenstil benötigen. Unser Analystenteam kann Ihnen auch Daten in groben Excel-Rohdateien und Pivot-Tabellen (Fact Book) bereitstellen oder Sie bei der Erstellung von Präsentationen aus den im Bericht verfügbaren Datensätzen unterstützen.