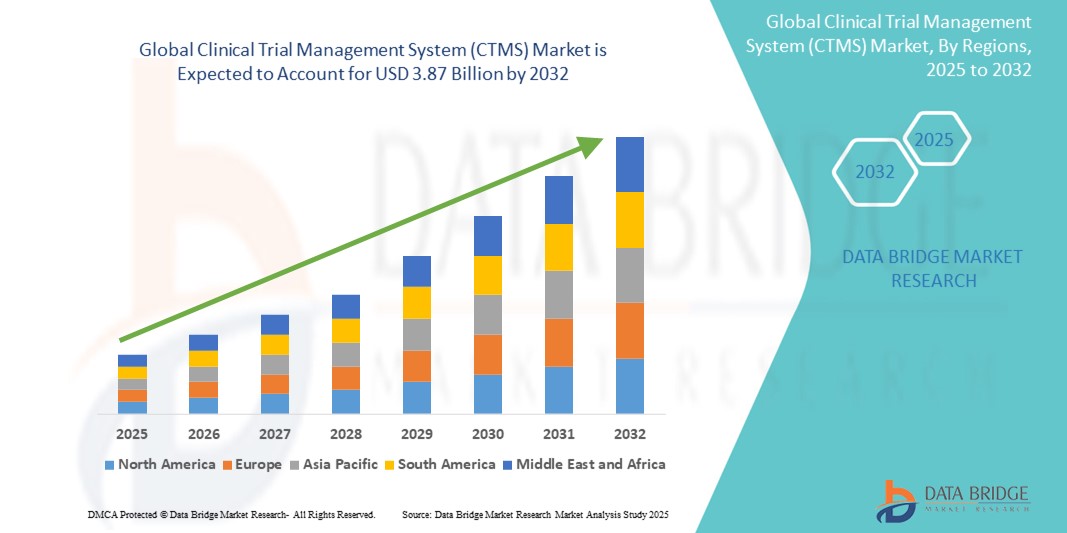
Global Clinical Trial Management System Market
Marktgröße in Milliarden USD
CAGR :
% 
 USD
1.41 Billion
USD
3.87 Billion
2024
2032
USD
1.41 Billion
USD
3.87 Billion
2024
2032
| 2025 –2032 | |
| USD 1.41 Billion | |
| USD 3.87 Billion | |
|
|
|
|
Globale Marktsegmentierung für Clinical Trial Management System (CTMS) nach Typ (Unternehmen und vor Ort), Bereitstellung (webbasiert, Cloud-basiert und vor Ort), Komponente (Software und Service), Endbenutzer (Pharma- und BiotechnologieunternehmenCROs und Medizingerätehersteller ) – Branchentrends und Prognose bis 2032
Marktgröße für klinische Studienmanagementsysteme (CTMS)
- Der globale Markt für klinische Studienmanagementsysteme (CTMS) wurde im Jahr 2024 auf 1,41 Milliarden US-Dollar geschätzt und soll bis 2032 3,87 Milliarden US-Dollar erreichen , bei einer CAGR von 13,4 % im Prognosezeitraum.
- Dieses Wachstum wird durch Faktoren wie steigende Investitionen in Forschung und Entwicklung, ein wachsendes Volumen klinischer Studien und technologische Fortschritte vorangetrieben.
Marktanalyse für klinische Studienmanagementsysteme (CTMS)
- Klinische Studienmanagementsysteme (CTMS) sind wichtige Werkzeuge in der Pharma- und Biotechnologiebranche und bieten umfassende Lösungen für die Planung, Verfolgung und Verwaltung klinischer Studien. Sie spielen eine entscheidende Rolle bei der Einhaltung gesetzlicher Vorschriften, der Verbesserung der Datengenauigkeit und der Optimierung des Studienbetriebs.
- Die Nachfrage nach CTMS-Lösungen wird maßgeblich durch das zunehmende Volumen klinischer Studien, steigende F&E-Investitionen und die zunehmende Komplexität klinischer Studien getrieben. Die Integration fortschrittlicher Technologien wie KI, maschinelles Lernen und Cloud Computing verbessert die Effizienz und Skalierbarkeit von CTMS-Plattformen weiter.
- Nordamerika wird voraussichtlich den Markt für klinische Studienmanagementsysteme (CTMS) dominieren und einen Anteil von etwa 47,6 % am Weltmarkt haben. Dies ist auf die Präsenz großer Pharma- und Biotechnologieunternehmen, eine starke Infrastruktur für die klinische Forschung und günstige staatliche Vorschriften zur Unterstützung klinischer Studien zurückzuführen.
- Der asiatisch-pazifische Raum dürfte mit einer jährlichen Wachstumsrate von 12,8 % die am schnellsten wachsende Region im Markt für klinische Studienmanagementsysteme (CTMS) sein. Grund hierfür sind die zunehmende Aktivität bei klinischen Studien, der schnelle Ausbau der Gesundheitsinfrastruktur und die Kostenvorteile bei der Durchführung klinischer Forschung in der Region.
- Das webbasierte Segment wird voraussichtlich mit einem Marktanteil von 71,7 % den größten Marktanteil einnehmen, was auf seine Skalierbarkeit, Flexibilität und Kosteneffizienz zurückzuführen ist. Cloudbasierte CTMS-Plattformen sind die bevorzugte Wahl für die Verwaltung klinischer Studien und bieten Echtzeitzugriff auf Studiendaten, verbesserte Datensicherheit und reduzierte IT-Infrastrukturkosten. Dies unterstützt ein effizientes Studienmanagement.
Berichtsumfang und Marktsegmentierung für Clinical Trial Management System (CTMS)
|
Eigenschaften |
Wichtige Markteinblicke zum Clinical Trial Management System (CTMS) |
|
Abgedeckte Segmente |
|
|
Abgedeckte Länder |
Nordamerika
Europa
Asien-Pazifik
Naher Osten und Afrika
Südamerika
|
|
Wichtige Marktteilnehmer |
|
|
Marktchancen |
|
|
Wertschöpfungsdaten-Infosets |
Zusätzlich zu den Einblicken in Marktszenarien wie Marktwert, Wachstumsrate, Segmentierung, geografische Abdeckung und wichtige Akteure enthalten die von Data Bridge Market Research kuratierten Marktberichte auch Import-Export-Analysen, eine Übersicht über die Produktionskapazität, eine Analyse des Produktionsverbrauchs, eine Preistrendanalyse, ein Szenario des Klimawandels, eine Lieferkettenanalyse, eine Wertschöpfungskettenanalyse, eine Übersicht über Rohstoffe/Verbrauchsmaterialien, Kriterien für die Lieferantenauswahl, eine PESTLE-Analyse, eine Porter-Analyse und regulatorische Rahmenbedingungen. |
Markttrends für klinische Studienmanagementsysteme (CTMS)
„Integration von KI und Advanced Analytics in CTMS“
- Ein wichtiger Trend in der Entwicklung von Systemen zur Verwaltung klinischer Studien ist die zunehmende Integration von künstlicher Intelligenz (KI), maschinellem Lernen (ML) und fortschrittlicher Analytik
- Diese Technologien ermöglichen Echtzeit-Datenanalyse, prädiktive Erkenntnisse und Prozessautomatisierung und verbessern so die Effizienz und Genauigkeit des klinischen Studienmanagements.
- Beispielsweise können KI -gestützte CTMS-Plattformen Herausforderungen bei der Patientenrekrutierung vorhersagen, die Standortauswahl optimieren und potenzielle Verzögerungen identifizieren, wodurch Studienzeiträume und -kosten deutlich reduziert werden. Diese Fähigkeit ist besonders wertvoll bei groß angelegten, multinationalen Studien, bei denen schnelle Entscheidungen entscheidend sind.
- Diese Fortschritte verändern den Ablauf klinischer Studien, verbessern die Behandlungsergebnisse der Patienten und treiben die Nachfrage nach CTMS-Plattformen der nächsten Generation mit modernster Datenanalyse und KI-Integration voran.
Marktdynamik für klinische Studienmanagementsysteme (CTMS)
Treiber
„Steigende Nachfrage nach effizientem Management klinischer Studien“
- Die zunehmende Komplexität klinischer Studien, die durch den Aufstieg der Präzisionsmedizin, personalisierter Therapien und dezentraler Studien vorangetrieben wird, trägt erheblich zur Nachfrage nach robusten Managementsystemen für klinische Studien bei.
- Da klinische Studien immer globaler und datenintensiver werden, ist der Bedarf an Echtzeit-Datenzugriff, optimierten Arbeitsabläufen und der Einhaltung gesetzlicher Vorschriften für Sponsoren, CROs und Forschungseinrichtungen von entscheidender Bedeutung.
- Fortschrittliche CTMS-Plattformen bieten integrierte Lösungen für Standortmanagement, Patientenaufnahme, Datenerfassung und Finanzverfolgung, wodurch die Studieneffizienz gesteigert und die Betriebskosten gesenkt werden.
Zum Beispiel,
- Laut einem im Journal of Clinical Research veröffentlichten Artikel wird der globale Markt für klinische Studien im Januar 2024 voraussichtlich deutlich wachsen. Bis 2028 werden voraussichtlich über 30 % der Studien dezentralisiert durchgeführt. Dieser Wandel treibt die Nachfrage nach fortschrittlichen CTMS-Lösungen voran, die komplexe Studiendesigns und Remote-Datenmanagement bewältigen können.
- Infolgedessen wird der Bedarf an effizienten Managementsystemen für klinische Studien voraussichtlich steigen und das Wachstum des CTMS-Marktes unterstützen.
Gelegenheit
„Integration von KI und Advanced Analytics in CTMS“
- KI-gestützte CTMS-Plattformen können die Effizienz von Studien steigern, indem sie Routineaufgaben automatisieren, die Patientenrekrutierung verbessern und die Datenanalyse optimieren, was eine präzisere und schnellere Entscheidungsfindung ermöglicht.
- Diese Plattformen nutzen Algorithmen des maschinellen Lernens, um Verzögerungen bei Studien vorherzusagen, die Standortauswahl zu optimieren und die Abbruchraten zu senken, wodurch die Studiendauer und -kosten deutlich reduziert werden.
- Darüber hinaus können KI-gesteuerte CTMS-Systeme Echtzeit-Einblicke in Patientendaten liefern und so personalisiertere und adaptivere Studiendesigns ermöglichen.
Zum Beispiel,
- Laut einem Bericht von Clinical Research News haben im März 2025 mehrere führende Pharmaunternehmen KI in ihre CTMS-Plattformen integriert, was zu einer bis zu 40 % schnelleren Patientenrekrutierung und einer 30-prozentigen Senkung der Studienkosten führte. Diese Fortschritte dürften das Management klinischer Studien verändern und die Nachfrage nach KI-gestützten CTMS-Lösungen steigern.
- Die Integration von KI in CTMS-Systeme kann zudem die Datengenauigkeit verbessern, die Betriebskosten senken und die Gesamtergebnisse von Studien verbessern, wodurch erhebliche Wachstumschancen für den Markt entstehen.
Einschränkung/Herausforderung
„Hohe Implementierungskosten und Bedenken hinsichtlich der Datensicherheit“
- Die hohen Kosten für die Implementierung und Wartung fortschrittlicher CTMS-Plattformen können für kleine und mittelgroße klinische Forschungsorganisationen (CROs) und Biotech-Unternehmen eine erhebliche Hürde darstellen.
- Diese Plattformen erfordern oft erhebliche Vorabinvestitionen, einschließlich Softwarelizenzen, Infrastruktur-Upgrades und Mitarbeiterschulungen, was für kleinere Organisationen unerschwinglich sein kann.
- Darüber hinaus können Bedenken hinsichtlich der Datensicherheit und der Einhaltung gesetzlicher Vorschriften die Einführung zusätzlich behindern, da bei klinischen Studien sensible Patientendaten generiert werden, die vor Verstößen und unbefugtem Zugriff geschützt werden müssen.
Zum Beispiel,
- Im September 2024 wies ein Bericht des Data Protection Journal auf die zunehmende Bedrohung durch Cyberangriffe im Gesundheitswesen hin, wobei Daten klinischer Studien zu einem Hauptziel wurden. Dies veranlasste viele Organisationen, massiv in Cybersicherheit zu investieren, was die Gesamtkosten der CTMS-Implementierung erhöhte.
- Infolgedessen können die hohen Kosten und die Herausforderungen bei der Datensicherheit, die mit CTMS-Systemen verbunden sind, deren Einführung, insbesondere bei kleineren Organisationen, einschränken und das allgemeine Marktwachstum verlangsamen.
Marktumfang für klinische Studienmanagementsysteme (CTMS)
Der Markt ist nach Typ, Lieferung, Komponenten und Endbenutzer segmentiert.
|
Segmentierung |
Untersegmentierung |
|
Nach Typ |
|
|
Per Lieferung |
|
|
Nach Komponenten |
|
|
Nach Endbenutzer |
|
Im Jahr 2025 wird erwartet, dass webbasierte Dienste den Markt dominieren und den größten Anteil im Liefersegment haben werden.
Das webbasierte Segment wird voraussichtlich den Markt für klinische Studienmanagementsysteme (CTMS) mit einem Marktanteil von 71,7 % im Jahr 2025 dominieren. Dies ist auf seine Skalierbarkeit, Flexibilität und Kosteneffizienz zurückzuführen. Cloudbasierte CTMS-Plattformen sind die bevorzugte Wahl für die Verwaltung klinischer Studien und bieten Echtzeitzugriff auf Studiendaten, verbesserte Datensicherheit und reduzierte IT-Infrastrukturkosten. Dies unterstützt ein effizientes Studienmanagement. Der anhaltende Trend zu dezentralen Studien und zur Fernüberwachung von Patienten trägt zusätzlich zur Dominanz dieses Segments bei und treibt das Marktwachstum voran.
Das Unternehmen wird voraussichtlich im Prognosezeitraum den größten Anteil am Typmarkt haben
Im Jahr 2025 wird das Enterprise-Segment voraussichtlich den Markt für klinische Studienmanagementsysteme (CTMS) mit einem Marktanteil von 65,4 % dominieren. Dies ist auf die Fähigkeit zurückzuführen, komplexe klinische Studien an mehreren Standorten zu verwalten und globale Abläufe zu unterstützen. Als erste Wahl für groß angelegte klinische Forschung bieten Enterprise-CTMS-Plattformen Echtzeit-Datenzugriff, robuste Analysen und eine nahtlose Zusammenarbeit zwischen den Beteiligten an klinischen Studien. Dies verbessert die Effizienz und die Ergebnisse der Studien. Die wachsende Nachfrage nach integrierten, skalierbaren Lösungen trägt zusätzlich zu dieser Marktdominanz bei.
Regionale Marktanalyse für klinische Studienmanagementsysteme (CTMS)
„Nordamerika hält den größten Anteil am Markt für Clinical Trial Management System (CTMS)“
- Nordamerika wird voraussichtlich den Markt für klinische Studienmanagementsysteme (CTMS) dominieren und einen Anteil von 47,6 % am Weltmarkt erreichen. Dies ist auf die Präsenz großer Pharma- und Biotechnologieunternehmen, eine starke Infrastruktur für die klinische Forschung und günstige staatliche Vorschriften zur Unterstützung klinischer Studien zurückzuführen.
- Die USA halten aufgrund der hohen Anzahl klinischer Studien, erheblicher Investitionen in Forschung und Entwicklung sowie der frühen Einführung fortschrittlicher Technologien für das Management klinischer Studien einen signifikanten Anteil von 35,3 %.
- Das gut etablierte Gesundheitsökosystem der Region, die große Patientenzahl und der Fokus auf personalisierte Medizin tragen zusätzlich zu seiner Marktführerschaft bei.
- Darüber hinaus stärken die Präsenz qualifizierter Fachkräfte, eine fortschrittliche IT-Infrastruktur und starke regulatorische Rahmenbedingungen den CTMS-Markt in Nordamerika weiter.
„Der asiatisch-pazifische Raum wird voraussichtlich die höchste durchschnittliche jährliche Wachstumsrate (CAGR) im Markt für klinische Versuchsmanagementsysteme (CTMS) verzeichnen“
- Im asiatisch-pazifischen Raum wird das höchste Wachstum im Markt für Clinical Trial Management System (CTMS) erwartet, mit einer prognostizierten jährlichen Wachstumsrate von etwa 12,8 %, getrieben durch die zunehmende Aktivität bei klinischen Studien, den schnellen Ausbau der Gesundheitsinfrastruktur und die Kostenvorteile bei der Durchführung klinischer Forschung in der Region.
- Länder wie China, Indien und Südkorea entwickeln sich aufgrund der wachsenden Pharma- und Biotechnologiebranche und der zunehmenden Patientenaufnahme in klinische Studien zu Schlüsselmärkten.
- China ist der regionale Marktführer mit erheblicher staatlicher Unterstützung für klinische Forschung, großen Patientenpopulationen und dem Ausbau biopharmazeutischer Produktionskapazitäten
- Indien wird voraussichtlich die höchste jährliche Wachstumsrate im CTMS-Markt verzeichnen, angetrieben durch kosteneffiziente klinische Studien, eine wachsende Zahl von Auftragsforschungsinstituten (CROs) und steigende ausländische Investitionen im Gesundheitssektor.
Marktanteile des Clinical Trial Management Systems (CTMS)
Die Wettbewerbslandschaft des Marktes liefert detaillierte Informationen zu den einzelnen Wettbewerbern. Zu den Details gehören Unternehmensübersicht, Unternehmensfinanzen, Umsatz, Marktpotenzial, Investitionen in Forschung und Entwicklung, neue Marktinitiativen, globale Präsenz, Produktionsstandorte und -anlagen, Produktionskapazitäten, Stärken und Schwächen des Unternehmens, Produkteinführung, Produktbreite und -umfang sowie Anwendungsdominanz. Die oben genannten Datenpunkte beziehen sich ausschließlich auf die Marktausrichtung der Unternehmen.
Die wichtigsten Marktführer auf dem Markt sind:
- Advarra (USA)
- ICON plc (Irland)
- Merative (USA)
- DSG, Inc. (USA)
- ArisGlobal (USA)
- Clario (USA)
- Oracle (USA)
- Medidata (USA)
- Fountainayn (USA)
- MedNet (USA)
- IQVIA Inc. (USA)
- SimpleTrials (USA)
- Calyx Global Inc. (USA)
- RealTime Software Solutions, LLC (USA)
- LabCorp (USA)
- Veeva Systems (USA)
- Wipro (Indien)
- PHARMASEAL (Großbritannien)
Neueste Entwicklungen auf dem globalen Markt für Clinical Trial Management System (CTMS)
- Im Februar 2025 kündigte Medidata Solutions, ein führender Anbieter von Technologie für klinische Studien, die Einführung seines neuen KI-gestützten Clinical Trial Management Systems an, das die Datenintegration und Echtzeitanalyse verbessern soll. Das System bietet verbesserte Möglichkeiten zur Studienüberwachung, automatisierte Risikobewertungen und optimierte Arbeitsabläufe zur Einhaltung gesetzlicher Vorschriften, um die Arzneimittelentwicklung zu beschleunigen und die Studieneffizienz zu verbessern.
- Im November 2024 stellte die Oracle Corporation die neueste Version ihrer CTMS-Plattform mit erweiterten Cloud-Funktionen vor, darunter erweiterte Tools zur Patientenrekrutierung, Unterstützung bei der Fernüberwachung und integrierte eConsent-Module. Diese Innovationen sollen dezentrale und hybride klinische Studien unterstützen und die Teilnehmerbeteiligung sowie die Datengenauigkeit verbessern.
- Im Oktober 2024 stellte IQVIA Inc. seine CTMS-Lösung der nächsten Generation vor. Diese nutzt maschinelle Lernalgorithmen zur Vorhersage von Studienrisiken und zur Optimierung der Ressourcenallokation. Die Plattform bietet außerdem Echtzeit-Dashboards und anpassbare Berichte, um die Entscheidungsfindung für klinische Forschungsorganisationen (CROs) und Sponsoren zu verbessern.
- Im August 2024 kündigte Clario eine Erweiterung seines CTMS-Angebots um integrierte Module für elektronische Datenerfassung (EDC) und patientenberichtete Ergebnisse (PRO) an. Dieses einheitliche System soll das Datenmanagement vereinfachen, die Compliance verbessern und patientenzentrierte Studiendesigns optimieren. Die aktualisierte Plattform zielt auf eine verbesserte Betriebseffizienz und regulatorische Bereitschaft ab.
SKU-
Erhalten Sie Online-Zugriff auf den Bericht zur weltweit ersten Market Intelligence Cloud
- Interaktives Datenanalyse-Dashboard
- Unternehmensanalyse-Dashboard für Chancen mit hohem Wachstumspotenzial
- Zugriff für Research-Analysten für Anpassungen und Abfragen
- Konkurrenzanalyse mit interaktivem Dashboard
- Aktuelle Nachrichten, Updates und Trendanalyse
- Nutzen Sie die Leistungsfähigkeit der Benchmark-Analyse für eine umfassende Konkurrenzverfolgung
Forschungsmethodik
Die Datenerfassung und Basisjahresanalyse werden mithilfe von Datenerfassungsmodulen mit großen Stichprobengrößen durchgeführt. Die Phase umfasst das Erhalten von Marktinformationen oder verwandten Daten aus verschiedenen Quellen und Strategien. Sie umfasst die Prüfung und Planung aller aus der Vergangenheit im Voraus erfassten Daten. Sie umfasst auch die Prüfung von Informationsinkonsistenzen, die in verschiedenen Informationsquellen auftreten. Die Marktdaten werden mithilfe von marktstatistischen und kohärenten Modellen analysiert und geschätzt. Darüber hinaus sind Marktanteilsanalyse und Schlüsseltrendanalyse die wichtigsten Erfolgsfaktoren im Marktbericht. Um mehr zu erfahren, fordern Sie bitte einen Analystenanruf an oder geben Sie Ihre Anfrage ein.
Die wichtigste Forschungsmethodik, die vom DBMR-Forschungsteam verwendet wird, ist die Datentriangulation, die Data Mining, die Analyse der Auswirkungen von Datenvariablen auf den Markt und die primäre (Branchenexperten-)Validierung umfasst. Zu den Datenmodellen gehören ein Lieferantenpositionierungsraster, eine Marktzeitlinienanalyse, ein Marktüberblick und -leitfaden, ein Firmenpositionierungsraster, eine Patentanalyse, eine Preisanalyse, eine Firmenmarktanteilsanalyse, Messstandards, eine globale versus eine regionale und Lieferantenanteilsanalyse. Um mehr über die Forschungsmethodik zu erfahren, senden Sie eine Anfrage an unsere Branchenexperten.
Anpassung möglich
Data Bridge Market Research ist ein führendes Unternehmen in der fortgeschrittenen formativen Forschung. Wir sind stolz darauf, unseren bestehenden und neuen Kunden Daten und Analysen zu bieten, die zu ihren Zielen passen. Der Bericht kann angepasst werden, um Preistrendanalysen von Zielmarken, Marktverständnis für zusätzliche Länder (fordern Sie die Länderliste an), Daten zu klinischen Studienergebnissen, Literaturübersicht, Analysen des Marktes für aufgearbeitete Produkte und Produktbasis einzuschließen. Marktanalysen von Zielkonkurrenten können von technologiebasierten Analysen bis hin zu Marktportfoliostrategien analysiert werden. Wir können so viele Wettbewerber hinzufügen, wie Sie Daten in dem von Ihnen gewünschten Format und Datenstil benötigen. Unser Analystenteam kann Ihnen auch Daten in groben Excel-Rohdateien und Pivot-Tabellen (Fact Book) bereitstellen oder Sie bei der Erstellung von Präsentationen aus den im Bericht verfügbaren Datensätzen unterstützen.