Saudi Arabia Turkey And Egypt In Vitro Diagnostics Ivd Quality Control Market
Tamaño del mercado en miles de millones de dólares
Tasa de crecimiento anual compuesta (CAGR) :
% 
 USD
867.09 Thousand
USD
1,260.66 Thousand
2022
2030
USD
867.09 Thousand
USD
1,260.66 Thousand
2022
2030
| 2023 –2030 | |
| USD 867.09 Thousand | |
| USD 1,260.66 Thousand | |
|
|
|
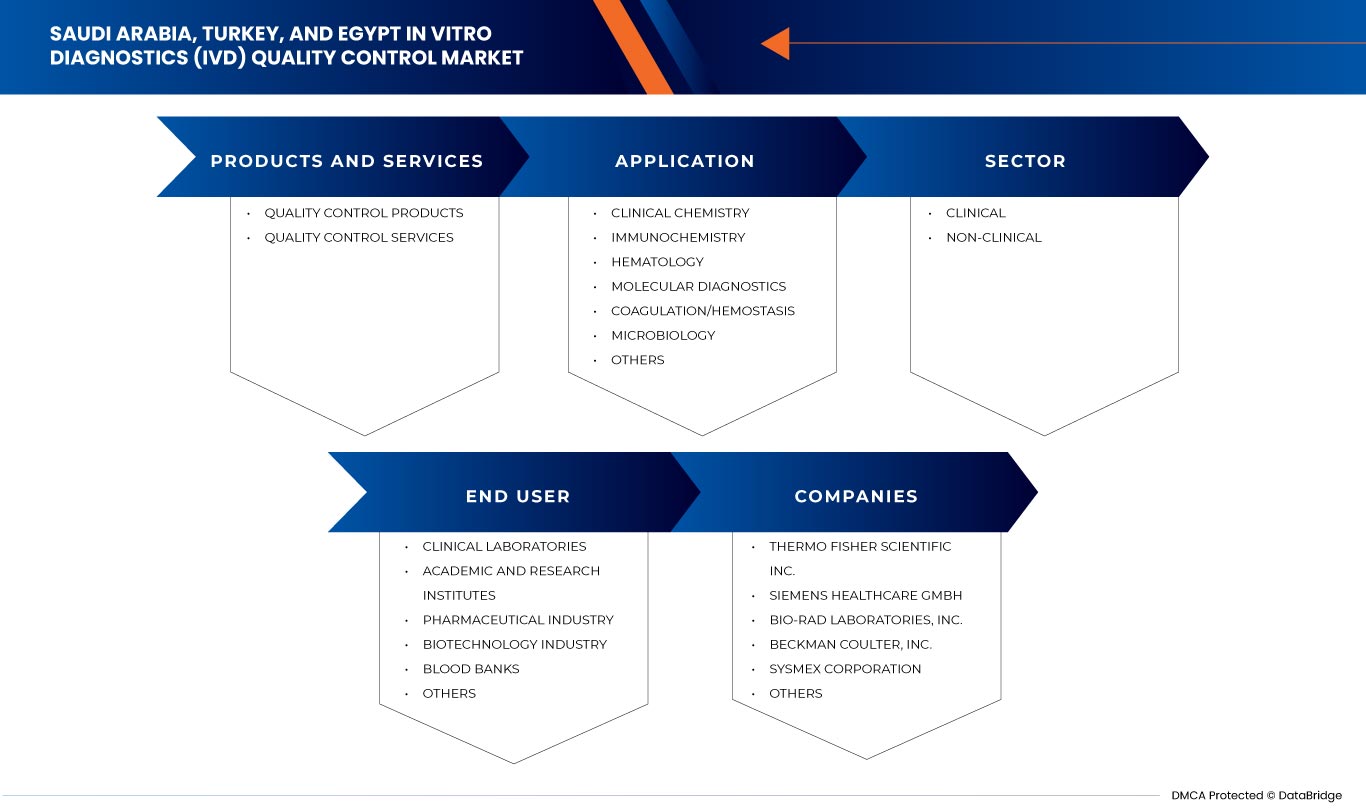
Mercado de control de calidad de diagnóstico in vitro (IVD) de Arabia Saudita, Turquía y Egipto, por producto y servicios (productos de control de calidad y servicios de control de calidad), aplicación ( química clínica , inmunoquímica, hematología, diagnóstico molecular, coagulación/hemostasia, microbiología y otros), sector (clínico y no clínico), usuario final (laboratorios clínicos, institutos académicos y de investigación, bancos de sangre, industria biotecnológica, industria farmacéutica y otros): tendencias de la industria y pronóstico hasta 2030.
Análisis y tamaño del mercado de control de calidad de diagnóstico in vitro (IVD) en Arabia Saudita, Turquía y Egipto
La creciente prevalencia de enfermedades crónicas en Arabia Saudita, Turquía y Egipto ha aumentado la demanda del mercado. El aumento del gasto sanitario para mejorar los servicios sanitarios también contribuye al crecimiento del mercado. Los principales actores del mercado se centran en diversos lanzamientos y aprobaciones de productos durante este período crucial. Además, el aumento de la mejora de los servicios de control de calidad también contribuye a la creciente demanda del mercado de control de calidad de diagnóstico in vitro.


Se espera que el mercado de control de calidad de diagnóstico in vitro (IVD) de Arabia Saudita, Turquía y Egipto gane crecimiento de mercado en el período de pronóstico de 2023 a 2030. Data Bridge Market Research analiza que el mercado está creciendo con una CAGR del 4,8% en el período de pronóstico de 2023 a 2030 y se espera que alcance los USD 1.260,66 mil para 2030 desde USD 867,09 mil en 2022.
|
Métrica del informe |
Detalles |
|
Período de pronóstico |
2023 a 2030 |
|
Año base |
2022 |
|
Años históricos |
2021 (Personalizable para 2015-2020) |
|
Unidades cuantitativas |
Ingresos en miles de USD |
|
Segmentos cubiertos |
Producto y servicios (productos de control de calidad y servicios de control de calidad), aplicación (química clínica, inmunoquímica, hematología, diagnóstico molecular, coagulación/hemostasia, microbiología y otros), sector (clínico y no clínico), usuario final (laboratorios clínicos, institutos académicos y de investigación, bancos de sangre, industria biotecnológica, industria farmacéutica y otros) |
|
Países cubiertos |
Arabia Saudita, Turquía y Egipto |
|
Actores del mercado cubiertos |
Las principales empresas que operan en el mercado son Bio-Rad Laboratories, Inc, Siemens Healthcare Private Limited, Sysmex Europe SE, Randox Laboratories Ltd., Sera Care, Thermo Fisher Scientific Inc., Beckman Coulter, Inc., Technopath Clinical Diagnostics, DiaSorin SpA, Agappe Diagnostics Ltd y Spectrum Diagnostics, entre otras. |
Definición de mercado
Los productos de diagnóstico in vitro son aquellos reactivos, instrumentos y sistemas destinados a utilizarse en el diagnóstico de enfermedades u otras afecciones, incluida la determinación del estado de salud, con el fin de curar, mitigar, tratar o prevenir enfermedades o sus secuelas. Dichos productos están destinados a utilizarse en la recolección, preparación y examen de muestras extraídas del cuerpo humano.
Los controles de calidad de diagnóstico in vitro son muestras o materiales que se utilizan para validar la fiabilidad del sistema de pruebas de diagnóstico in vitro, garantizar la precisión de los resultados de las pruebas y evaluar el impacto de factores como las condiciones ambientales y el rendimiento del operador en los resultados de las pruebas. Además, también se pueden utilizar para controlar la salud de un paciente, curar enfermedades y permitir a los profesionales médicos identificar el procedimiento o la terapia de tratamiento más eficaz para el paciente.
Dinámica del mercado de control de calidad de diagnóstico in vitro (IVD)
En esta sección se aborda la comprensión de los factores impulsores, las oportunidades, las limitaciones y los desafíos del mercado. Todo esto se analiza en detalle a continuación:
Conductores
- Aumenta la prevalencia de enfermedades crónicas en Arabia Saudita, Turquía y Egipto
Las enfermedades y afecciones crónicas están aumentando en todo el mundo. El envejecimiento de la población y el estilo de vida sedentario contribuyen a un aumento constante de los problemas de salud a largo plazo. La creciente prevalencia de enfermedades crónicas e infecciosas ha llevado al lanzamiento de herramientas de diagnóstico y prueba rápidas por parte de los principales actores del mercado. Además, la creciente adopción de dispositivos de autoprueba y de punto de atención está acelerando aún más el crecimiento de los dispositivos de diagnóstico in vitro en todo el mundo.
Por lo tanto, se espera que el creciente número de enfermedades crónicas acelere significativamente el crecimiento del mercado de control de calidad IVD en el futuro cercano.
- Creciente adopción de soluciones de control de calidad en laboratorios y hospitales
Las pruebas de laboratorio de muestras de pacientes pueden ser un procedimiento complejo, dependiendo del análisis clínico, el estudio microbiológico o las pruebas de banco de sangre, entre otras facetas del laboratorio clínico. El control de calidad (CC) es uno de los impactos más importantes en las pruebas de laboratorio: garantiza tanto la precisión como la exactitud de los resultados de las muestras de pacientes. La integridad de las muestras de control de calidad es importante tanto para la gestión de la calidad general como para cumplir con los requisitos de las pruebas de competencia.
Por lo tanto, se espera que la creciente adopción de soluciones de control de calidad en laboratorios y hospitales impulse el crecimiento del mercado.

Oportunidades
-
Aumento de las adquisiciones estratégicas y las asociaciones entre organizaciones
Recientemente, diferentes organizaciones están dando un paso adelante para asociarse y colaborar con el fin de desarrollar diagnósticos in vitro esenciales para detectar enfermedades. No solo eso, con la ayuda de asociaciones y acuerdos, ambas empresas pueden desarrollar un nuevo conjunto de tecnologías y plataformas que ayudarán a detectar enfermedades.
Con la ayuda de un acuerdo a largo plazo, ambas empresas pueden ofrecer IVD con precios dimensionales en respuesta a la demanda de los consumidores en el mercado. Esta asociación y este acuerdo mutuo no solo benefician a ambas empresas, sino que también crean muchas oportunidades para que el mercado crezca.
-
Aumento de las actividades de investigación y desarrollo
En todo el mundo, el gasto en actividades de investigación y desarrollo está aumentando debido al gasto en salud pública y a los resultados económicos. Por otra parte, el sector de la salud ocupa el segundo lugar entre todos los sectores en lo que respecta a la cantidad que gasta en investigación y desarrollo. El aumento del gasto en salud ha dado lugar además a una mejor provisión de oportunidades de investigación y desarrollo. En consecuencia, ha aumentado la demanda de servicios de externalización de asuntos regulatorios de diagnóstico in vitro en toda la región.
Restricciones/Desafíos
- Altos costos relacionados con el control de calidad y el mantenimiento del IVD
Los diagnósticos in vitro (IVD) son pruebas que se realizan en muestras, como sangre o tejido, extraídas del cuerpo humano. Los diagnósticos in vitro pueden detectar enfermedades u otras afecciones y pueden utilizarse para controlar la salud general de una persona y ayudar a curar, tratar o prevenir enfermedades.
El diagnóstico in vitro de analitos provenientes de muestras corporales, incluidas biopsias de sangre y tejidos, se utiliza solo o en combinación con investigaciones clínicas y se percibe como una herramienta importante para obtener resultados médicos de alta calidad, por lo que mantener el diagnóstico in vitro y el control de calidad de los dispositivos de diagnóstico in vitro tiene costos elevados para realizar pruebas precisas.
Por lo tanto, el aumento del coste del mantenimiento del IVD se ha convertido en un factor decisivo para las empresas en el proceso de servicio, lo que limita aún más el crecimiento del mercado hasta cierto punto.
- Normas estrictas sobre diagnóstico in vitro en Arabia Saudita, Turquía y Egipto
El uso de dispositivos de diagnóstico in vitro (IVD) en todo el mundo está aumentando rápidamente, debido al aumento de la población envejecida y a varias enfermedades crónicas que se pueden prevenir mediante un diagnóstico temprano y tratamientos oportunos. Al mismo tiempo, los actores del mercado de dispositivos de diagnóstico in vitro deben cumplir ciertas regulaciones para obtener la aprobación de las autoridades superiores para el lanzamiento del producto en una región. Estas estrictas pautas deben cumplirse y esta es una de las tareas más difíciles entre todos los pasos. La aprobación previa a la comercialización de varios dispositivos médicos varía de un país a otro.
Por lo tanto, las estrictas normas y regulaciones para la aprobación de productos actúan como restricciones para el crecimiento del mercado.
Desarrollo reciente
- En febrero de 2023, Siemens Healthineers, una empresa líder en tecnología médica, y Unilabs, un proveedor líder de servicios de diagnóstico, anunciaron un acuerdo plurianual valorado en más de 200.000 euros. Unilabs ha invertido en la tecnología de vanguardia de Siemens Healthineers y adquirirá más de 400 analizadores de laboratorio para mejorar aún más su infraestructura de laboratorio y ofrecer un servicio inigualable a sus clientes. Esta asociación ha ayudado a que la última infraestructura de pruebas de diagnóstico mejore la atención a los pacientes.
- En julio de 2021, Thermo Fisher Scientific, líder mundial al servicio de la ciencia, anunció una colaboración con Ortho Clinical Diagnostics para promover y distribuir los controles de calidad Thermo Scientific MAS y el software de garantía de calidad LabLink xL para su uso con los analizadores VITROS de Ortho Clinical Diagnostics. Esto ha ayudado a la empresa a aumentar su presencia global en el mercado.
Alcance del mercado de control de calidad de diagnóstico in vitro (IVD) en Arabia Saudita, Turquía y Egipto
El mercado de control de calidad de diagnóstico in vitro (IVD) de Arabia Saudita, Turquía y Egipto está segmentado en cuatro segmentos notables, como producto y servicios, aplicación, tipo, sector y usuario final. El crecimiento entre estos segmentos lo ayudará a analizar los segmentos de crecimiento magros en las industrias y brindará a los usuarios una valiosa descripción general del mercado y conocimientos del mercado para tomar decisiones estratégicas para identificar las principales aplicaciones del mercado.
Productos y servicios
- Productos de control de calidad
- Servicios de control de calidad
Sobre la base de productos y servicios, el mercado de control de calidad de diagnóstico in vitro (IVD) de Arabia Saudita, Turquía y Egipto está segmentado en productos de control de calidad y servicios de control de calidad.
Aplicaciones
- Química clínica
- Inmunoquímica
- Hematología
- Diagnóstico molecular
- Coagulación/Hemostasia
- Microbiología
- Otros
Según las aplicaciones, el mercado de control de calidad de diagnóstico in vitro (IVD) de Arabia Saudita, Turquía y Egipto está segmentado en química clínica, inmunoquímica, hematología, diagnóstico molecular, coagulación/hemostasia, microbiología y otros.
Sector
- Clínico
- No clínico
Según el sector, el mercado de control de calidad de diagnóstico in vitro (IVD) de Arabia Saudita, Turquía y Egipto está segmentado en clínico y no clínico.
Usuario final
- Laboratorios clínicos
- Institutos académicos y de investigación
- Bancos de sangre
- Industria de la biotecnología
- Industria farmacéutica
- Otros
Según los usuarios finales, el mercado de control de calidad de diagnóstico in vitro (IVD) de Arabia Saudita, Turquía y Egipto está segmentado en laboratorios clínicos, institutos académicos y de investigación, bancos de sangre, industria biotecnológica, industria farmacéutica y otros.
Análisis del panorama competitivo y de la cuota de mercado de control de calidad de diagnóstico in vitro (IVD)
El panorama competitivo del mercado de control de calidad de diagnóstico in vitro (IVD) proporciona detalles de los competidores. Los detalles incluidos son una descripción general de la empresa, las finanzas de la empresa, los ingresos generados, el potencial de mercado, la inversión en investigación y desarrollo, las nuevas iniciativas de mercado, la presencia global, los sitios e instalaciones de producción, las capacidades de producción, las fortalezas y debilidades de la empresa, el lanzamiento de productos, la amplitud y variedad de productos y el dominio de la aplicación. Los puntos de datos anteriores proporcionados solo están relacionados con el enfoque de las empresas en el mercado de la ataxia.
Algunos de los principales actores que operan en el mercado de control de calidad de diagnóstico in vitro (IVD) son Bio-Rad Laboratories, Inc, Siemens Healthcare Private Limited, Sysmex Europe SE, Randox Laboratories Ltd., Sera Care, Thermo Fisher Scientific Inc., Beckman Coulter, Inc., Technopath Clinical Diagnostics, DiaSorin SpA, Agappe Diagnostics Ltd y Spectrum Diagnostics, entre otros.
SKU-
Obtenga acceso en línea al informe sobre la primera nube de inteligencia de mercado del mundo
- Panel de análisis de datos interactivo
- Panel de análisis de empresas para oportunidades con alto potencial de crecimiento
- Acceso de analista de investigación para personalización y consultas
- Análisis de la competencia con panel interactivo
- Últimas noticias, actualizaciones y análisis de tendencias
- Aproveche el poder del análisis de referencia para un seguimiento integral de la competencia
Tabla de contenido
1 INTRODUCTION
1.1 OBJECTIVES OF THE STUDY
1.2 MARKET DEFINITION
1.3 OVERVIEW OF SAUDI ARABIA, TURKEY, AND EGYPT IN VITRO DIAGNOSTICS (IVD) QUALITY CONTROL MARKET
1.4 LIMITATIONS
1.5 MARKETS COVERED
2 MARKET SEGMENTATION
2.1 MARKETS COVERED
2.2 GEOGRAPHICAL SCOPE
2.3 YEARS CONSIDERED FOR THE STUDY
2.4 CURRENCY AND PRICING
2.5 DBMR TRIPOD DATA VALIDATION MODEL
2.6 MULTIVARIATE MODELLING
2.7 SAUDI ARABIA PRODUCTS AND SERVICES, LIFELINE CURVE
2.8 EGYPT PRODUCTS AND SERVICES, LIFELINE CURVE
2.9 TURKEY PRODUCTS AND SERVICES, LIFELINE CURVE
2.1 PRIMARY INTERVIEWS WITH KEY OPINION LEADERS
2.11 DBMR MARKET POSITION GRID
2.12 MARKET TESTING TYPE COVERAGE GRID
2.13 VENDOR SHARE ANALYSIS
2.14 SECONDARY SOURCES
2.15 ASSUMPTIONS
3 EXECUTIVE SUMMARY
4 PREMIUM INSIGHTS
4.1 PESTEL'S MODEL
4.2 PORTER'S 5 FORCES
4.3 INDUSTRY INSIGHTS
5 REGULATORY GUIDELINES FOR IN VITRO DIAGNOSTICS QUALITY CONTROL
5.1 REGULATIONS IN SAUDI ARABIA
5.2 REGULATIONS IN TURKEY
5.3 REGULATIONS IN EGYPT
5.3.1 MEDICAL DEVICE REGISTRATION IN EGYPT, THE PROCESS IN BRIEF:
6 MARKET OVERVIEW
6.1 DRIVERS
6.1.1 RISING PREVALENCE OF CHRONIC DISEASES ACROSS SAUDI ARABIA, TURKEY, AND EGYPT
6.1.2 RISING ADOPTION OF QUALITY CONTROL SOLUTIONS IN LABORATORIES AND HOSPITALS
6.1.3 ADVANCEMENTS IN TECHNOLOGY LEADING TO THE DEVELOPMENT OF NEW AND ADVANCED DIAGNOSTIC PRODUCTS
6.1.4 RISING USE OF QUALITY CONTROL IN MOLECULAR DIAGNOSTICS
6.2 RESTRAINTS
6.2.1 HIGH COST RELATED TO QUALITY CONTROL AND MAINTENANCE OF IVD
6.2.2 STRINGENT REGULATIONS REGARDING IVD IN SAUDI ARABIA, TURKEY, AND EGYPT
6.3 OPPORTUNITIES
6.3.1 RISE IN STRATEGIC ACQUISITION AND PARTNERSHIP AMONG ORGANIZATIONS
6.3.2 RISING RESEARCH AND DEVELOPMENT ACTIVITIES
6.4 CHALLENGES
6.4.1 LACK OF INFRASTRUCTURE IN HEALTHCARE SERVICE
6.4.2 SHORTAGE OF SKILLED PERSONNEL FOR HANDLING QUALITY CONTROL OF IN VITRO DIAGNOSTIC DEVICES.
7 SAUDI ARABIA, TURKEY, AND EGYPT IN VITRO DIAGNOSTICS (IVD) QUALITY CONTROL MARKET, BY PRODUCT AND SERVICES
7.1 OVERVIEW
7.2 QUALITY CONTROL PRODUCTS
7.2.1 SERUM/PLASMA-BASED CONTROL
7.2.2 WHOLE BLOOD-BASED CONTROLS
7.2.3 URINE-BASED CONTROLS
7.2.4 OTHER CONTROLS
7.2.5 INTERNAL QUALITY CONTROL
7.2.6 EXTERNAL QUALITY CONTROL
7.3 QUALITY CONTROL SERVICES
8 SAUDI ARABIA, TURKEY, AND EGYPT IN VITRO DIAGNOSTICS (IVD) QUALITY CONTROL MARKET, BY APPLICATION
8.1 OVERVIEW
8.2 CLINICAL CHEMISTRY
8.3 IMMUNOCHEMISTRY
8.4 HEMATOLOGY
8.5 MOLECULAR DIAGNOSTICS
8.5.1 QUALITY CONTROL PRODUCTS
8.5.1.1 INTERNAL QUALITY CONTROL
8.5.1.2 EXTERNAL QUALITY CONTROL
8.5.2 QUALITY CONTROL SERVICES
8.6 COAGULATION/HEMOSTASIS
8.7 MICROBIOLOGY
8.8 OTHERS
9 SAUDI ARABIA, TURKEY, AND EGYPT IN VITRO DIAGNOSTICS (IVD) QUALITY CONTROL MARKET, BY SECTOR
9.1 OVERVIEW
9.2 CLINICAL
9.3 NON-CLINICAL
10 SAUDI ARABIA, TURKEY, AND EGYPT IN VITRO DIAGNOSTICS (IVD) QUALITY CONTROL MARKET, BY END USER
10.1 OVERVIEW
10.2 CLINICAL LABORATORIES
10.3 ACADEMIC AND RESEARCH INSTITUTES
10.4 PHARMACEUTICAL INDUSTRY
10.5 BIOTECHNOLOGY INDUSTRY
10.6 BLOOD BANKS
10.7 OTHERS
11 SAUDI ARABIA, TURKEY, AND EGYPT IN VITRO DIAGNOSTICS (IVD) QUALITY CONTROL MARKET, COMPANY LANDSCAPE
11.1 COMPANY SHARE ANALYSIS: SAUDI ARABIA
11.2 COMPANY SHARE ANALYSIS: EGYPT
11.3 COMPANY SHARE ANALYSIS: TURKEY
12 SWOT ANALYSIS
13 TURKEY IN VITRO DIAGNOSTICS (IVD) QUALITY CONTROL MARKET, COMPANY PROFILES
13.1 THERMO FISHER SCIENTIFIC INC.
13.1.1 COMPANY SNAPSHOT
13.1.2 REVENUE ANALYSIS
13.1.3 PRODUCT PORTFOLIO
13.1.4 RECENT DEVELOPMENTS
13.2 SIEMENS HEALTHCARE GMBH
13.2.1 COMPANY SNAPSHOT
13.2.2 REVENUE ANALYSIS
13.2.3 PRODUCT PORTFOLIO
13.2.4 RECENT DEVELOPMENT
13.3 BIO-RAD LABORATORIES, INC.
13.3.1 COMPANY SNAPSHOT
13.3.2 REVENUE ANALYSIS
13.3.3 PRODUCT PORTFOLIO
13.3.4 RECENT DEVELOPMENT
13.4 BECKMAN COULTER, INC.
13.4.1 COMPANY SNAPSHOT
13.4.2 PRODUCT PORTFOLIO
13.4.3 RECENT DEVELOPMENT
13.5 SYSMEX CORPORATION
13.5.1 COMPANY SNAPSHOT
13.5.2 REVENUE ANALYSIS
13.5.3 PRODUCT PORTFOLIO
13.5.4 RECENT DEVELOPMENT
13.6 AGAPPE DIAGNOSTICS LTD
13.6.1 COMPANY SNAPSHOT
13.6.2 PRODUCT PORTFOLIO
13.6.3 RECENT DEVELOPMENT
13.7 DIASORIN MOLECULAR LLC.
13.7.1 COMPANY SNAPSHOT
13.7.2 PRODUCT PORTFOLIO
13.7.3 RECENT DEVELOPMENT
13.8 RANDOX LABORATORIES LTD.
13.8.1 COMPANY SNAPSHOT
13.8.2 PRODUCT PORTFOLIO
13.8.3 RECENT DEVELOPMENT
13.9 SERA CARE
13.9.1 COMPANY SNAPSHOT
13.9.2 PRODUCT PORTFOLIO
13.9.3 RECENT DEVELOPMENT
13.1 SPECTRUM DIAGNOSTICS
13.10.1 COMPANY SNAPSHOT
13.10.2 PRODUCT PORTFOLIO
13.10.3 RECENT DEVELOPMENT
13.11 TECHNOPATH CLINICAL DIAGNOSTICS
13.11.1 COMPANY SNAPSHOT
13.11.2 PRODUCT PORTFOLIO
13.11.3 RECENT DEVELOPMENT
14 QUESTIONNAIRE
15 RELATED REPORTS
Lista de figuras
FIGURE 1 SAUDI ARABIA, TURKEY, AND EGYPT IN VITRO DIAGNOSTICS (IVD) QUALITY CONTROL MARKET: SEGMENTATION
FIGURE 2 SAUDI ARABIA, TURKEY, AND EGYPT IN VITRO DIAGNOSTICS (IVD) QUALITY CONTROL MARKET: DATA TRIANGULATION
FIGURE 3 SAUDI ARABIA, TURKEY, AND EGYPT IN VITRO DIAGNOSTICS (IVD) QUALITY CONTROL MARKET: DROC ANALYSIS
FIGURE 4 SAUDI ARABIA IN VITRO DIAGNOSTICS (IVD) QUALITY CONTROL MARKET: COUNTRY MARKET ANALYSIS
FIGURE 5 EGYPT IN VITRO DIAGNOSTICS (IVD) QUALITY CONTROL MARKET: COUNTRY MARKET ANALYSIS
FIGURE 6 TURKEYS IN VITRO DIAGNOSTICS (IVD) QUALITY CONTROL MARKET: COUNTRY MARKET ANALYSIS
FIGURE 7 SAUDI ARABIA, TURKEY, AND EGYPT IN VITRO DIAGNOSTICS (IVD) QUALITY CONTROL MARKET: COMPANY RESEARCH ANALYSIS
FIGURE 8 SAUDI ARABIA, TURKEY, AND EGYPT IN VITRO DIAGNOSTICS (IVD) QUALITY CONTROL MARKET: INTERVIEW DEMOGRAPHICS
FIGURE 9 SAUDI ARABIA, TURKEY, AND EGYPT IN VITRO DIAGNOSTICS (IVD) QUALITY CONTROL MARKET: DBMR MARKET POSITION GRID
FIGURE 10 SAUDI ARABIA, TURKEY, AND EGYPT IN VITRO DIAGNOSTICS (IVD) QUALITY CONTROL MARKET: MARKET TESTING TYPE COVERAGE GRID
FIGURE 11 SAUDI ARABIA, TURKEY, AND EGYPT IN VITRO DIAGNOSTICS (IVD) QUALITY CONTROL MARKET: VENDOR SHARE ANALYSIS
FIGURE 12 SAUDI ARABIA, TURKEY, AND EGYPT IN VITRO DIAGNOSTICS (IVD) QUALITY CONTROL MARKET: SEGMENTATION
FIGURE 13 RISING PREVALENCE OF CHRONIC DISEASES ACROSS SAUDI ARABIA IS EXPECTED TO DRIVE THE SAUDI ARABIA IN VITRO DIAGNOSTICS (IVD) QUALITY CONTROL MARKET IN THE FORECAST PERIOD
FIGURE 14 RISING ADOPTION OF QUALITY CONTROL SOLUTIONS IN LABORATORIES AND HOSPITALS IS EXPECTED TO DRIVE THE TURKEY IN VITRO DIAGNOSTICS (IVD) QUALITY CONTROL MARKET IN THE FORECAST PERIOD IN THE FORECAST PERIOD
FIGURE 15 ADVANCEMENTS IN TECHNOLOGY LEADING TO THE DEVELOPMENT OF NEW AND ADVANCED DIAGNOSTIC PRODUCTS ARE EXPECTED TO DRIVE THE EGYPT IN VITRO DIAGNOSTICS (IVD) QUALITY CONTROL MARKET IN THE FORECAST PERIOD IN THE FORECAST PERIOD
FIGURE 16 THE PRODUCT AND SERVICES TYPE SEGMENT IS EXPECTED TO ACCOUNT FOR THE LARGEST SHARE OF THE SAUDI ARABIA IN VITRO DIAGNOSTICS (IVD) QUALITY CONTROL MARKET IN 2023 & 2030
FIGURE 17 THE PRODUCT AND SERVICES TYPE SEGMENT IS EXPECTED TO ACCOUNT FOR THE LARGEST SHARE OF THE TURKEY IN VITRO DIAGNOSTICS (IVD) QUALITY CONTROL MARKET IN 2023 & 2030
FIGURE 18 THE PRODUCT AND SERVICES TYPE SEGMENT IS EXPECTED TO ACCOUNT FOR THE LARGEST SHARE OF THE EGYPT IN VITRO DIAGNOSTICS (IVD) QUALITY CONTROL MARKET IN 2023 & 2030
FIGURE 19 DRIVERS, RESTRAINTS, OPPORTUNITIES, AND CHALLENGES OF SAUDI ARABIA, TURKEY, AND EGYPT IN VITRO DIAGNOSTICS (IVD) QUALITY CONTROL MARKET
FIGURE 20 SAUDI ARABIA, IN VITRO DIAGNOSTICS (IVD) QUALITY CONTROL MARKET, BY PRODUCTS AND SERVICES, 2022
FIGURE 21 TURKEY, IN VITRO DIAGNOSTICS (IVD) QUALITY CONTROL MARKET, BY PRODUCTS AND SERVICES, 2022
FIGURE 22 EGYPT, IN VITRO DIAGNOSTICS (IVD) QUALITY CONTROL MARKET, BY PRODUCTS AND SERVICES, 2022
FIGURE 23 SAUDI ARABIA IN VITRO DIAGNOSTICS (IVD) QUALITY CONTROL MARKET, BY PRODUCTS AND SERVICES, 2023-2030 (USD THOUSAND)
FIGURE 24 TURKEY IN VITRO DIAGNOSTICS (IVD) QUALITY CONTROL MARKET, BY PRODUCTS AND SERVICES, 2023-2030 (USD THOUSAND)
FIGURE 25 EGYPT IN VITRO DIAGNOSTICS (IVD) QUALITY CONTROL MARKET, BY PRODUCTS AND SERVICES, 2023-2030 (USD THOUSAND)
FIGURE 26 SAUDI ARABIA IN VITRO DIAGNOSTICS (IVD) QUALITY CONTROL MARKET, BY PRODUCTS AND SERVICES, CAGR (2023-2030)
FIGURE 27 TURKEY IN VITRO DIAGNOSTICS (IVD) QUALITY CONTROL MARKET, BY PRODUCTS AND SERVICES, CAGR (2023-2030)
FIGURE 28 EGYPT IN VITRO DIAGNOSTICS (IVD) QUALITY CONTROL MARKET, BY PRODUCTS AND SERVICES, CAGR (2023-2030)
FIGURE 29 SAUDI ARABIA, TURKEY AND EGYPT IN VITRO DIAGNOSTICS (IVD) QUALITY CONTROL MARKET, BY PRODUCTS AND SERVICES, LIFELINE CURVE
FIGURE 30 TURKEY IN VITRO DIAGNOSTICS (IVD) QUALITY CONTROL MARKET, BY PRODUCTS AND SERVICES, LIFELINE CURVE
FIGURE 31 EGYPT IN VITRO DIAGNOSTICS (IVD) QUALITY CONTROL MARKET, BY PRODUCTS AND SERVICES, LIFELINE CURVE
FIGURE 32 SAUDI ARABIA IN VITRO DIAGNOSTICS (IVD) QUALITY CONTROL MARKET, BY APPLICATION, 2022
FIGURE 33 TURKEY IN VITRO DIAGNOSTICS (IVD) QUALITY CONTROL MARKET, BY APPLICATION, 2022
FIGURE 34 EGYPT IN VITRO DIAGNOSTICS (IVD) QUALITY CONTROL MARKET, BY APPLICATION, 2022
FIGURE 35 SAUDI ARABIA IN VITRO DIAGNOSTICS (IVD) QUALITY CONTROL MARKET, BY APPLICATION, 2023-2030 (USD THOUSAND)
FIGURE 36 TURKEY IN VITRO DIAGNOSTICS (IVD) QUALITY CONTROL MARKET, BY APPLICATION, 2023-2030 (USD THOUSAND)
FIGURE 37 EGYPT IN VITRO DIAGNOSTICS (IVD) QUALITY CONTROL MARKET, BY APPLICATION, 2023-2030 (USD THOUSAND)
FIGURE 38 SAUDI ARABIA, IN VITRO DIAGNOSTICS (IVD) QUALITY CONTROL MARKET, BY APPLICATION, CAGR (2023-2030)
FIGURE 39 TURKEY, IN VITRO DIAGNOSTICS (IVD) QUALITY CONTROL MARKET, BY APPLICATION, CAGR (2023-2030)
FIGURE 40 EGYPT, IN VITRO DIAGNOSTICS (IVD) QUALITY CONTROL MARKET, BY APPLICATION, CAGR (2023-2030)
FIGURE 41 SAUDI ARABIA, IN VITRO DIAGNOSTICS (IVD) QUALITY CONTROL MARKET, BY APPLICATION, LIFELINE CURVE
FIGURE 42 TURKEY, IN VITRO DIAGNOSTICS (IVD) QUALITY CONTROL MARKET, BY APPLICATION, LIFELINE CURVE
FIGURE 43 EGYPT, IN VITRO DIAGNOSTICS (IVD) QUALITY CONTROL MARKET, BY APPLICATION, LIFELINE CURVE
FIGURE 44 SAUDI ARABIA, IN VITRO DIAGNOSTICS (IVD) QUALITY CONTROL MARKET, BY SECTOR, 2022
FIGURE 45 TURKEY, IN VITRO DIAGNOSTICS (IVD) QUALITY CONTROL MARKET, BY SECTOR, 2022
FIGURE 46 EGYPT, IN VITRO DIAGNOSTICS (IVD) QUALITY CONTROL MARKET, BY SECTOR, 2022
FIGURE 47 SAUDI ARABIA, IN VITRO DIAGNOSTICS (IVD) QUALITY CONTROL MARKET, BY SECTOR, 2023-2030 (USD THOUSAND)
FIGURE 48 TURKEY, IN VITRO DIAGNOSTICS (IVD) QUALITY CONTROL MARKET, BY SECTOR, 2023-2030 (USD THOUSAND)
FIGURE 49 EGYPT, IN VITRO DIAGNOSTICS (IVD) QUALITY CONTROL MARKET, BY SECTOR, 2023-2030 (USD THOUSAND)
FIGURE 50 SAUDI ARABIA IN VITRO DIAGNOSTICS (IVD) QUALITY CONTROL MARKET, BY SECTOR, CAGR (2023-2030)
FIGURE 51 TURKEY IN VITRO DIAGNOSTICS (IVD) QUALITY CONTROL MARKET, BY SECTOR, CAGR (2023-2030)
FIGURE 52 EGYPT IN VITRO DIAGNOSTICS (IVD) QUALITY CONTROL MARKET, BY SECTOR, CAGR (2023-2030)
FIGURE 53 SAUDI ARABIA, IN VITRO DIAGNOSTICS (IVD) QUALITY CONTROL MARKET, BY SECTOR, LIFELINE CURVE
FIGURE 54 TURKEY IN VITRO DIAGNOSTICS (IVD) QUALITY CONTROL MARKET, BY SECTOR, LIFELINE CURVE
FIGURE 55 EGYPT IN VITRO DIAGNOSTICS (IVD) QUALITY CONTROL MARKET, BY SECTOR, LIFELINE CURVE
FIGURE 56 SAUDI ARABIA, IN VITRO DIAGNOSTICS (IVD) QUALITY CONTROL MARKET, BY END USER, 2022
FIGURE 57 TURKEY IN VITRO DIAGNOSTICS (IVD) QUALITY CONTROL MARKET, BY END USER, 2022
FIGURE 58 EGYPT IN VITRO DIAGNOSTICS (IVD) QUALITY CONTROL MARKET, BY END USER, 2022
FIGURE 59 SAUDI ARABIA, IN VITRO DIAGNOSTICS (IVD) QUALITY CONTROL MARKET, BY END USER, 2023-2030 (USD THOUSAND)
FIGURE 60 TURKEY, IN VITRO DIAGNOSTICS (IVD) QUALITY CONTROL MARKET, BY END USER, 2023-2030 (USD THOUSAND)
FIGURE 61 EGYPT, IN VITRO DIAGNOSTICS (IVD) QUALITY CONTROL MARKET, BY END USER, 2023-2030 (USD THOUSAND)
FIGURE 62 SAUDI ARABIA IN VITRO DIAGNOSTICS (IVD) QUALITY CONTROL MARKET, BY END USER, CAGR (2023-2030)
FIGURE 63 TURKEY IN VITRO DIAGNOSTICS (IVD) QUALITY CONTROL MARKET, BY END USER, CAGR (2023-2030)
FIGURE 64 EGYPT IN VITRO DIAGNOSTICS (IVD) QUALITY CONTROL MARKET, BY END USER, CAGR (2023-2030)
FIGURE 65 SAUDI ARABIA, IN VITRO DIAGNOSTICS (IVD) QUALITY CONTROL MARKET, BY END USER, LIFELINE CURVE
FIGURE 66 TURKEY, IN VITRO DIAGNOSTICS (IVD) QUALITY CONTROL MARKET, BY END USER, LIFELINE CURVE
FIGURE 67 EGYPT, IN VITRO DIAGNOSTICS (IVD) QUALITY CONTROL MARKET, BY END USER, LIFELINE CURVE
FIGURE 68 SAUDI ARABIA IN VITRO DIAGNOSTICS (IVD) QUALITY CONTROL MARKET: COMPANY SHARE 2022 (%)
FIGURE 69 EGYPT IN VITRO DIAGNOSTICS (IVD) QUALITY CONTROL MARKET: COMPANY SHARE 2022 (%)
FIGURE 70 TURKEY IN VITRO DIAGNOSTICS (IVD) QUALITY CONTROL MARKET: COMPANY SHARE 2022 (%)
Metodología de investigación
La recopilación de datos y el análisis del año base se realizan utilizando módulos de recopilación de datos con muestras de gran tamaño. La etapa incluye la obtención de información de mercado o datos relacionados a través de varias fuentes y estrategias. Incluye el examen y la planificación de todos los datos adquiridos del pasado con antelación. Asimismo, abarca el examen de las inconsistencias de información observadas en diferentes fuentes de información. Los datos de mercado se analizan y estiman utilizando modelos estadísticos y coherentes de mercado. Además, el análisis de la participación de mercado y el análisis de tendencias clave son los principales factores de éxito en el informe de mercado. Para obtener más información, solicite una llamada de un analista o envíe su consulta.
La metodología de investigación clave utilizada por el equipo de investigación de DBMR es la triangulación de datos, que implica la extracción de datos, el análisis del impacto de las variables de datos en el mercado y la validación primaria (experto en la industria). Los modelos de datos incluyen cuadrícula de posicionamiento de proveedores, análisis de línea de tiempo de mercado, descripción general y guía del mercado, cuadrícula de posicionamiento de la empresa, análisis de patentes, análisis de precios, análisis de participación de mercado de la empresa, estándares de medición, análisis global versus regional y de participación de proveedores. Para obtener más información sobre la metodología de investigación, envíe una consulta para hablar con nuestros expertos de la industria.
Personalización disponible
Data Bridge Market Research es líder en investigación formativa avanzada. Nos enorgullecemos de brindar servicios a nuestros clientes existentes y nuevos con datos y análisis que coinciden y se adaptan a sus objetivos. El informe se puede personalizar para incluir análisis de tendencias de precios de marcas objetivo, comprensión del mercado de países adicionales (solicite la lista de países), datos de resultados de ensayos clínicos, revisión de literatura, análisis de mercado renovado y base de productos. El análisis de mercado de competidores objetivo se puede analizar desde análisis basados en tecnología hasta estrategias de cartera de mercado. Podemos agregar tantos competidores sobre los que necesite datos en el formato y estilo de datos que esté buscando. Nuestro equipo de analistas también puede proporcionarle datos en archivos de Excel sin procesar, tablas dinámicas (libro de datos) o puede ayudarlo a crear presentaciones a partir de los conjuntos de datos disponibles en el informe.














