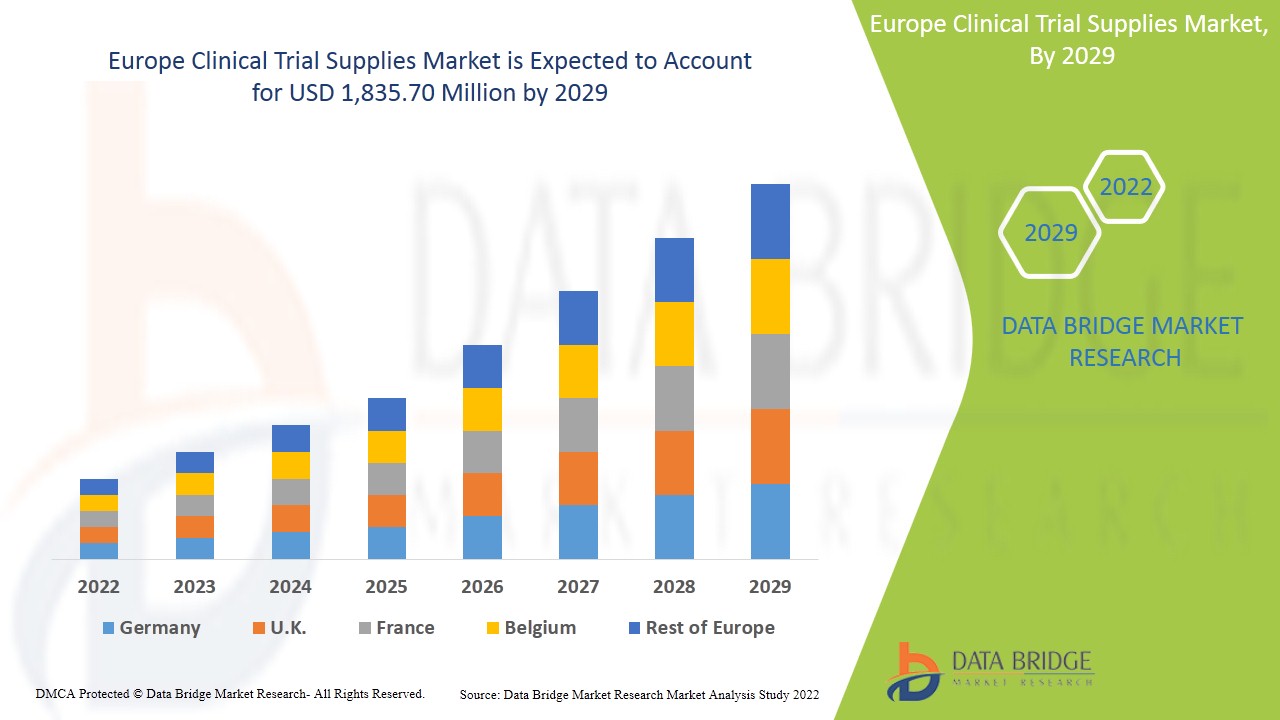
Europe Clinical Trial Supplies Market
حجم السوق بالمليار دولار أمريكي
CAGR :
% 
 1,835.70
2022
2029
1,835.70
2022
2029
| 2023 –2029 | |
| USD 1,835.70 | |
|
|
|
|
>سوق إمدادات التجارب السريرية في أوروبا، حسب الخدمات (التخزين والتصنيع والتعبئة والتغليف والتسميات)، المرحلة السريرية (المرحلة الثالثة، المرحلة الثانية، المرحلة الرابعة، المرحلة الأولى)، الاستخدامات العلاجية (علم الأورام، أمراض القلب والأوعية الدموية، الأمراض الجلدية، الاضطرابات الأيضية، الأمراض المعدية، أمراض الجهاز التنفسي ، اضطرابات الجهاز العصبي المركزي والعقلية، اضطرابات الدم، أخرى)، المستخدم النهائي (منظمات أبحاث العقود، شركات الأدوية والتكنولوجيا الحيوية)، اتجاهات الصناعة والتوقعات حتى عام 2029.
تحليل السوق والرؤى : سوق إمدادات التجارب السريرية في أوروبا
من المتوقع أن يكتسب سوق إمدادات التجارب السريرية في أوروبا نموًا في السوق في الفترة المتوقعة من 2022 إلى 2029. تحلل شركة Data Bridge Market Research أن السوق ينمو بمعدل نمو سنوي مركب بنسبة 7.8٪ في الفترة المتوقعة من 2022 إلى 2029 ومن المتوقع أن يصل إلى 1،835.70 مليون دولار أمريكي بحلول عام 2029. العامل الرئيسي الذي يدفع نمو سوق إمدادات التجارب السريرية هو ارتفاع الطلب على التجارب السريرية في جميع أنحاء العالم، وزيادة حالات الأمراض، والأموال الحكومية لاستثمارات البحث والتطوير وتطوير علاجات جديدة مثل الطب الشخصي مما يؤدي إلى نمو سوق إمدادات التجارب السريرية في المستقبل.
التجربة السريرية هي دراسة بحثية تحدد ما إذا كانت الاستراتيجية الطبية أو العلاج أو الجهاز آمنًا وفعالًا ومفيدًا للاستخدام البشري. تساعد هذه الدراسات في تحديد الأساليب الطبية التجريبية الأفضل لأمراض معينة. توفر التجربة السريرية أفضل البيانات لأغراض اتخاذ القرارات المتعلقة بالرعاية الصحية.
الغرض من التجارب السريرية هو دراسة المعايير العلمية الصارمة. هذه المعايير تحمي المرضى وتساعد في إنتاج نتائج دراسة موثوقة.
التجارب السريرية هي المرحلة الأخيرة في تطوير الأدوية في عملية بحث طويلة ودقيقة يقوم بها العلماء أو الباحثون لعلاج مرض معين، سواء كان دواءً أو جهازًا طبيًا. غالبًا ما تبدأ عملية تطوير الأدوية في المختبر، حيث يقوم العلماء أولاً بتطوير واختبار أفكار جديدة تتعلق بعلاج المرض.
يقدم تقرير سوق إمدادات التجارب السريرية في أوروبا تفاصيل عن حصة السوق والتطورات الجديدة وتحليل خط أنابيب المنتجات وتأثير اللاعبين المحليين والمحليين في السوق وتحليل الفرص من حيث جيوب الإيرادات الناشئة والتغييرات في لوائح السوق وموافقات المنتجات والقرارات الاستراتيجية وإطلاق المنتجات والتوسعات الجغرافية والابتكارات التكنولوجية في السوق. لفهم التحليل وسيناريو السوق، اتصل بنا للحصول على موجز محلل، وسيساعدك فريقنا في إنشاء حل لتأثير الإيرادات لتحقيق هدفك المنشود.
|
تقرير القياس |
تفاصيل |
|
فترة التنبؤ |
2022 إلى 2029 |
|
سنة الأساس |
2021 |
|
سنوات تاريخية |
2020 (قابلة للتخصيص حتى 2019 - 2014) |
|
وحدات كمية |
الإيرادات بالملايين من الدولارات الأمريكية، التسعير بالدولار الأمريكي |
|
القطاعات المغطاة |
حسب الخدمات (التخزين والتصنيع والتعبئة والتغليف والتسمية)، المرحلة السريرية (المرحلة الثالثة، المرحلة الثانية، المرحلة الرابعة، المرحلة الأولى)، الاستخدامات العلاجية (علم الأورام، أمراض القلب والأوعية الدموية، الأمراض الجلدية، الاضطرابات الأيضية، الأمراض المعدية، أمراض الجهاز التنفسي، اضطرابات الجهاز العصبي المركزي والعقلية، اضطرابات الدم، وغيرها)، حسب المستخدم النهائي (منظمات البحوث التعاقدية، شركات الأدوية والتكنولوجيا الحيوية) |
|
الدول المغطاة |
ألمانيا، فرنسا، المملكة المتحدة، هولندا، سويسرا، بلجيكا، روسيا، إيطاليا، إسبانيا، تركيا، بقية دول أوروبا في أوروبا |
|
الجهات الفاعلة في السوق المشمولة |
موفيانتو (الولايات المتحدة)، شارب (الولايات المتحدة)، ثيرمو فيشر ساينتيفيك إنك (الولايات المتحدة)، كاتالنت، إنك (الولايات المتحدة)، بي سي آي فارما سيرفيسز (الولايات المتحدة)، مجموعة ألماك (المملكة المتحدة)، شركة باركسيل الدولية (الولايات المتحدة)، بيونيكال المحدودة (المملكة المتحدة)، عليوم ميديكال المحدودة (المملكة المتحدة)، مايونكس (المملكة المتحدة)، كلينيجين جروب بي إل سي (المملكة المتحدة)، أنسيلاري، إل بي (الولايات المتحدة)، سيرو كلينفارم (الهند)، كلينيكال سوبليز مانجمنت هولدينجز، إنك (الولايات المتحدة)، بيوكير (المملكة المتحدة) وغيرها. |
ديناميكيات سوق لوازم التجارب السريرية
السائقين
- الطلب المتزايد على التجارب السريرية في جميع أنحاء العالم
وقد بلغ الطلب المتزايد على التجارب السريرية 82% في البلدان النامية وحدها مثل أمريكا الشمالية وأوروبا وآسيا. وتتوفر هذه الأدوية في السوق بعد التجارب السريرية، لذا فإن جميع الشركات تجري التجارب السريرية في الغالب اعتمادًا على نوع الدواء أو الجهاز. وبالتالي تعمل كمحرك رئيسي من شأنه أن يؤدي إلى توسيع معدل نمو سوق العلاج.
- ارتفاع معدل الإصابة بالأمراض المزمنة
إن انتشار الأمراض المزمنة بشكل كبير بسبب الزيادة السريعة في عدد السكان والعدوى بين الناس يمكن ملاحظته على مستوى العالم. وتساهم هذه الأمراض بدور رئيسي في مجال التجارب السريرية لتطوير الأدوية. ويتعين على الدواء أن يجتاز جميع المراحل السريرية القياسية ليكون متاحًا قبل الاستهلاك البشري. وبالتالي، لعلاج هذه الأمراض المزمنة لدى البشر، يجب أن يكون الدواء آمنًا.
- أموال الحكومة في استثمارات البحث والتطوير
تؤدي الأدوات والقوى العاملة والإدارة الطبية في حالة حدوث ضرر للباحثين والتأمين والنقل ورسوم لجنة الأخلاقيات ومعالجة البيانات والمواد الاستهلاكية الأخرى إلى تكاليف كبيرة في التجارب السريرية. التجارب السريرية هي تقييم أفكار الوقاية من الأمراض وعلاجها مما يعزز نمو سوق العلاج.
فرص
- تزايد تجارب تطوير الأدوية الجديدة في البلدان الناشئة
إن التجارب السريرية لفعالية الأدوية هي المفتاح الأساسي لتطوير الأدوية لعلاج الأمراض قبل طرحها في السوق للاستهلاك البشري. بالإضافة إلى ذلك، يجب أن تلبي الأدوية الجديدة تمديدات الترخيص والمعايير الدولية قبل البيع والتوزيع. إن زيادة انتشار الأمراض وارتفاع أعداد المرضى هي العوامل التي أدت إلى ظهور اتجاهات التجارب السريرية لتطوير الأدوية في البلدان النامية خلال الفترة الماضية.
كما تعمل الحكومات في الأسواق الناشئة (الصين والبرازيل وروسيا والهند وجنوب أفريقيا) على إصلاح الرعاية الصحية العامة ومنح المزيد من فرص الحصول على الأدوية. ويعني هذان العاملان المنسجمان معاً قدراً أعظم من الحرية لتطورات السوق وزيادة الإبداع في مجال البحوث السريرية في الأسواق الناشئة.
القيود/التحديات
التفاعلات الدوائية الضارة هي التأثيرات غير المرغوبة أو الضارة التي يمكن أن تحدث بعد تناول الدواء في ظل ظروف الاستخدام الطبيعية لدى البشر. تحدث التفاعلات الدوائية بشكل عام في اليرقان وفقر الدم والطفح الجلدي وتؤدي إلى انخفاض عدد خلايا الدم البيضاء وتلف الكلى وإصابة الأعصاب مما يؤدي إلى ضعف البصر أو السمع.
يمكن التأكد من العديد من الآثار السلبية من خلال الفحوصات الجسدية أثناء المرحلة السريرية للاختبار. وبالتالي، فإن الإبلاغ عن الآثار السلبية أثناء التجارب السريرية هو عامل التقييد الرئيسي لسوق الإمدادات. وعلى الرغم من الاستثمارات الكبيرة في الوقت والتكلفة لتطوير المواد البيولوجية والأدوية الجديدة، فمن المقدر أن انخفاض وقت الإجراء ومعدل الموافقة على الدواء يخلق أكبر تحدٍ للسوق، مما قد يعيق نمو السوق.
يقدم تقرير سوق لوازم التجارب السريرية هذا تفاصيل عن التطورات الحديثة الجديدة واللوائح التجارية وتحليل الاستيراد والتصدير وتحليل الإنتاج وتحسين سلسلة القيمة وحصة السوق وتأثير اللاعبين المحليين والمحليين في السوق وتحليل الفرص من حيث جيوب الإيرادات الناشئة والتغيرات في لوائح السوق وتحليل نمو السوق الاستراتيجي وحجم السوق ونمو سوق الفئات ومنافذ التطبيق والهيمنة وموافقات المنتجات وإطلاق المنتجات والتوسعات الجغرافية والابتكارات التكنولوجية في السوق. للحصول على مزيد من المعلومات حول سوق لوازم التجارب السريرية، اتصل بـ Data Bridge Market Research للحصول على موجز محلل ، سيساعدك فريقنا في اتخاذ قرار سوقي مستنير لتحقيق نمو السوق.
التطورات الأخيرة
- في فبراير 2022، أعلنت شركة Thermo Fisher Scientific عن شراكتها مع Medidata لتحسين اختيار موقع البحث السريري وتسريع تسجيل المرضى في التجارب السريرية. يعمل هذا على تحسين التخطيط للتجارب السريرية وتنفيذها لتسريع التجارب السريرية التي تم فيها إنشاء مجموعات البيانات من 26000 تجربة سريرية ونحو 8 ملايين مريض في أكثر من 140 دولة حول العالم
نطاق سوق لوازم التجارب السريرية في أوروبا
يتم تصنيف سوق إمدادات التجارب السريرية في أوروبا على أساس الخدمات والمرحلة السريرية والاستخدامات العلاجية والمستخدم النهائي. سيساعدك النمو بين هذه القطاعات على تحليل قطاعات النمو الضئيلة في الصناعات وتزويد المستخدمين بنظرة عامة قيمة على السوق ورؤى السوق لاتخاذ قرارات استراتيجية لتحديد تطبيقات السوق الأساسية.
خدمة
- تصنيع
- توزيع
- تخزين
- التعبئة والتغليف والوسم
على أساس الخدمات، يتم تقسيم سوق إمدادات التجارب السريرية في أوروبا إلى التصنيع والتوزيع والتخزين والتعبئة والتغليف والتسميات.
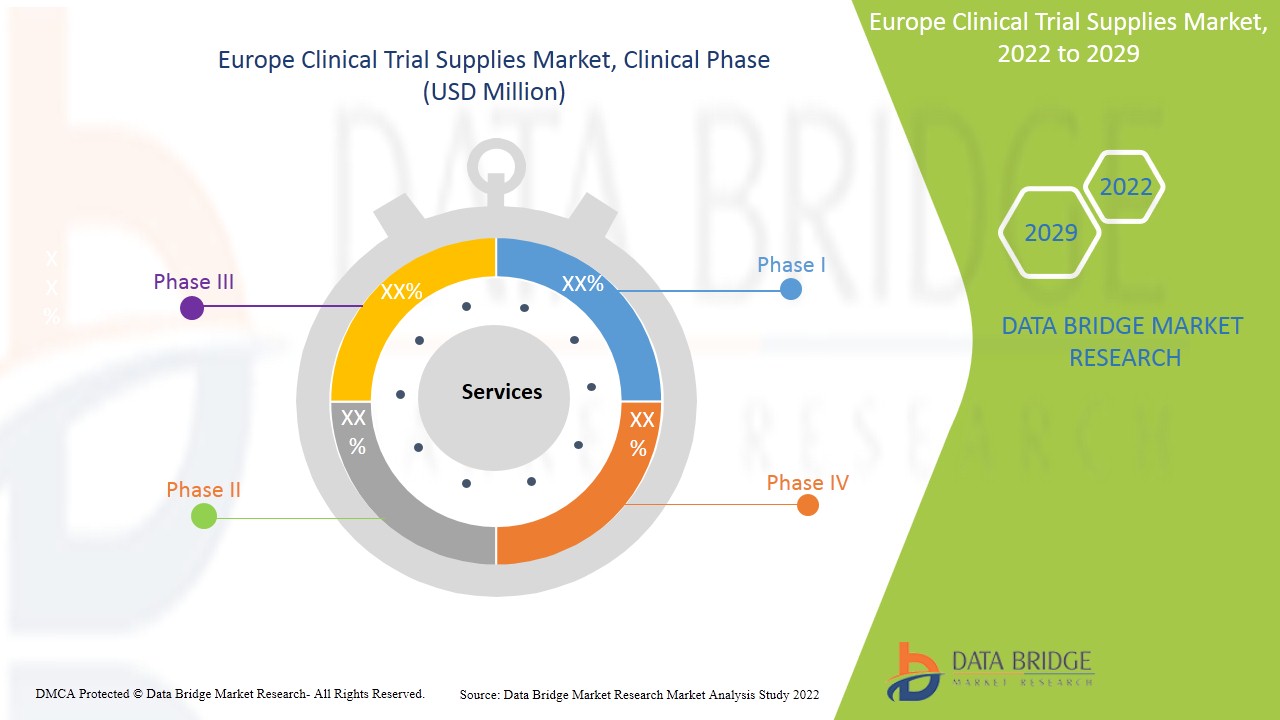
المرحلة السريرية
- المرحلة الأولى
- المرحلة الثانية
- المرحلة الثالثة
- المرحلة الرابعة
على أساس المرحلة السريرية، يتم تقسيم سوق إمدادات التجارب السريرية في أوروبا إلى المرحلة الأولى والمرحلة الثانية والمرحلة الثالثة والمرحلة الرابعة.
الاستخدامات العلاجية
- علم الأورام
- الجهاز العصبي المركزي
- الاضطرابات العقلية
- أمراض القلب والأوعية الدموية
- الأمراض المعدية
- أمراض الجهاز التنفسي
- اضطراب الدم
- طب الأمراض الجلدية
- آحرون
على أساس الاستخدامات العلاجية، يتم تقسيم سوق إمدادات التجارب السريرية في أوروبا إلى أمراض الأورام والجهاز العصبي المركزي والاضطرابات العقلية وأمراض القلب والأوعية الدموية والأمراض المعدية وأمراض الجهاز التنفسي والاضطرابات الأيضية واضطرابات الدم والأمراض الجلدية وغيرها.
المستخدم النهائي
- منظمات البحوث التعاقدية
- شركات الأدوية والتكنولوجيا الحيوية
على أساس المستخدم النهائي، يتم تقسيم سوق إمدادات التجارب السريرية في أوروبا إلى منظمات أبحاث تعاقدية وشركات الأدوية والتكنولوجيا الحيوية.
تحليل/رؤى إقليمية لسوق لوازم التجارب السريرية
يتم تقسيم سوق إمدادات التجارب السريرية في أوروبا إلى دول رئيسية مثل ألمانيا وفرنسا والمملكة المتحدة وإيطاليا وإسبانيا وروسيا وبلجيكا وتركيا وهولندا وسويسرا وبقية دول أوروبا.
تهيمن المملكة المتحدة على سوق إمدادات التجارب السريرية في أوروبا من حيث حصة السوق وإيرادات السوق وستواصل هيمنتها خلال الفترة المتوقعة 2022-2029. ويرجع هذا إلى وجود لاعبين رئيسيين رئيسيين يستثمرون في البحث والتطوير من أجل تقديم خدمة أفضل لإمدادات التجارب السريرية والبنية التحتية للرعاية الصحية المتطورة في هذه المنطقة.
كما يوفر قسم الدولة في التقرير عوامل التأثير الفردية على السوق والتغييرات في اللوائح في السوق والتي تؤثر على الاتجاهات الحالية والمستقبلية للسوق. تعد نقاط البيانات، مثل المبيعات الجديدة والاستبدالية، والتركيبة السكانية للدولة، ورسوم الاستيراد والتصدير، من بين المؤشرات الرئيسية المستخدمة للتنبؤ بسيناريو السوق للدول الفردية. بالإضافة إلى ذلك، يتم النظر في وجود العلامات التجارية العالمية وتوافرها والتحديات التي تواجهها بسبب المنافسة الشديدة من العلامات التجارية المحلية والمحلية، وتأثير قنوات المبيعات أثناء تقديم تحليل توقعات لبيانات الدولة.
تحليل المشهد التنافسي وحصة سوق إمدادات التجارب السريرية في أوروبا
يقدم المشهد التنافسي لسوق إمدادات التجارب السريرية في أوروبا تفاصيل حسب المنافس. تتضمن التفاصيل نظرة عامة على الشركة، والبيانات المالية للشركة، والإيرادات المتولدة، وإمكانات السوق، والاستثمار في البحث والتطوير، ومبادرات السوق الجديدة، ومواقع الإنتاج والمرافق، ونقاط القوة والضعف في الشركة، وإطلاق المنتج، وخطوط أنابيب تجارب المنتجات، وموافقات المنتجات، وبراءات الاختراع، وعرض المنتج ونطاقه، وهيمنة التطبيق، ومنحنى شريان الحياة التكنولوجي. ترتبط نقاط البيانات المذكورة أعلاه فقط بتركيز الشركات فيما يتعلق بسوق إمدادات التجارب السريرية.
المشاركون البارزون الرئيسيون العاملون في سوق إمدادات التجارب السريرية في أوروبا هم Movianto (الولايات المتحدة)، Sharp (الولايات المتحدة)، Thermo Fisher Scientific Inc. (الولايات المتحدة)، Catalent، Inc (الولايات المتحدة)، PCI Pharma Services (الولايات المتحدة)، Almac Group (المملكة المتحدة)، PAREXEL International Corporation (الولايات المتحدة)، Bionical Ltd. (المملكة المتحدة)، Alium Medical Limited (المملكة المتحدة)، MYODERM (المملكة المتحدة)، Clinigen Group plc (المملكة المتحدة)، Ancillare، LP (الولايات المتحدة)، SIRO Clinpharm (الهند) CLINICAL SUPPLIES MANAGEMENT HOLDINGS، INC. (الولايات المتحدة) Biocair (المملكة المتحدة) وغيرها.
منهجية البحث : سوق لوازم التجارب السريرية في أوروبا
يتم جمع البيانات وتحليل سنة الأساس باستخدام وحدات جمع البيانات ذات أحجام العينات الكبيرة. يتم تحليل بيانات السوق وتقديرها باستخدام نماذج إحصائية ومتماسكة للسوق. بالإضافة إلى ذلك، يعد تحليل حصة السوق وتحليل الاتجاهات الرئيسية من عوامل النجاح الرئيسية في تقرير السوق. منهجية البحث الرئيسية التي يستخدمها فريق بحث DBMR هي التثليث البيانات والتي تنطوي على استخراج البيانات وتحليل تأثير متغيرات البيانات على السوق والتحقق الأساسي (خبير الصناعة). وبصرف النظر عن هذا، تتضمن نماذج البيانات شبكة وضع البائعين وتحليل الخط الزمني للسوق ونظرة عامة على السوق والدليل وشبكة وضع الشركة وتحليل حصة الشركة في السوق ومعايير القياس وتحليل GlobalVsRegional وحصة البائعين. يرجى طلب مكالمة محلل في حالة وجود استفسار آخر.
SKU-
احصل على إمكانية الوصول عبر الإنترنت إلى التقرير الخاص بأول سحابة استخبارات سوقية في العالم
- لوحة معلومات تحليل البيانات التفاعلية
- لوحة معلومات تحليل الشركة للفرص ذات إمكانات النمو العالية
- إمكانية وصول محلل الأبحاث للتخصيص والاستعلامات
- تحليل المنافسين باستخدام لوحة معلومات تفاعلية
- آخر الأخبار والتحديثات وتحليل الاتجاهات
- استغل قوة تحليل المعايير لتتبع المنافسين بشكل شامل
Table of Content
1 INTRODUCTION
1.1 OBJECTIVES OF THE STUDY
1.2 MARKET DEFINITION
1.3 OVERVIEW OF EUROPE CLINICAL TRIAL SUPPLIES MARKET
1.4 LIMITATIONS
1.5 MARKETS COVERED
2 MARKET SEGMENTATION
2.1 MARKETS COVERED
2.2 GEOGRAPHICAL SCOPE
2.3 YEARS CONSIDERED FOR THE STUDY
2.4 CURRENCY AND PRICING
2.5 DBMR TRIPOD DATA VALIDATION MODEL
2.6 MULTIVARIATE MODELLING
2.7 SERVICES LIFELINE CURVE
2.8 PRIMARY INTERVIEWS WITH KEY OPINION LEADERS
2.9 DBMR MARKET POSITION GRID
2.1 VENDOR SHARE ANALYSIS
2.11 SECONDARY SOURCES
2.12 ASSUMPTIONS
3 EXECUTIVE SUMMARY
4 PREMIUM INSIGHTS
4.1 PESTEL ANALYSIS
4.2 PORTERS FIVE FORCES
5 EUROPE CLINICAL TRIAL SUPPLIES MARKET: REGULATORY SCENARIO
6 MARKET OVERVIEW
6.1 DRIVERS
6.1.1 RISING DEMAND FOR CLINICAL TRIALS WORLDWIDE
6.1.2 INCREASING INCIDENCE OF CHRONIC DISEASES
6.1.3 GOVERNMENT FUNDS IN R&D INVESTMENTS
6.1.4 ADVANCEMENT OF TECHNOLOGY IN CLINICAL TRIALS SUPPLIES
6.2 RESTRAINTS
6.2.1 ADVERSE EFFECTS OF CLINICAL TRIALS
6.2.2 TRANSPORTATION ISSUE IN CLINICAL TRIAL SUPPLIES
6.2.3 HIGH COST ASSOCIATED WITH THE CLINICAL TRIALS
6.3 OPPORTUNITIES
6.3.1 INCREASING NEW DRUG DEVELOPMENT TRIALS IN EMERGING COUNTRIES
6.3.2 INCREASING DEMAND FOR INNOVATIVE SOLUTIONS IN CLINICAL TRIALS SERVICES
6.3.3 EVOLUTION IN SUPPLY CHAIN MANAGEMENT FOR CLINICAL TRIALS
6.4 CHALLENGES
6.4.1 LOWER PROCEDURE TIME OF CLINICAL TRIALS APPROVAL
6.4.2 LACK OF SKILLED PERSON TO OPERATE DEVICES DURING CLINICAL TRIALS
7 EUROPE CLINICAL TRIAL SUPPLIES MARKET, BY SERVICES
7.1 OVERVIEW
7.2 STORAGE
7.3 MANUFACTURING
7.4 PACKAGING AND LABELLING
7.5 DISTRIBUTION
8 EUROPE CLINICAL TRIAL SUPPLIES MARKET, BY CLINICAL PHASES
8.1 OVERVIEW
8.2 PHASE III
8.3 PHASE II
8.4 PHASE IV
8.5 PHASE I
9 EUROPE CLINICAL TRIAL SUPPLIES MARKET, BY THERAPEUTIC USE
9.1 OVERVIEW
9.2 ONCOLOGY
9.3 CARDIOVASCULAR DISEASES
9.4 DERMATOLOGY
9.5 METABOLIC DISORDERS
9.6 INFECTIOUS DISEASES
9.7 RESPIRATORY DISEASES
9.8 CNS AND MENTAL DISORDERS
9.9 BLOOD DISORDERS
9.1 OTHERS
10 EUROPE CLINICAL TRIAL SUPPLIES MARKET, BY END USER
10.1 OVERVIEW
10.2 CONTRACT RESEARCH ORGANIZATIONS
10.3 PHARMACEUTICAL AND BIOTECHNOLOGY COMPANIES
11 EUROPE CLINICAL TRIAL SUPPLIES MARKET, BY REGION
11.1 EUROPE
11.1.1 GERMANY
11.1.2 FRANCE
11.1.3 U.K.
11.1.4 ITALY
11.1.5 SPAIN
11.1.6 NETHERLANDS
11.1.7 RUSSIA
11.1.8 BELGIUM
11.1.9 TURKEY
11.1.10 SWITZERLAND
11.1.11 REST OF EUROPE
12 EUROPE CLINICAL TRIAL SUPPLIES MARKET: COMPANY LANDSCAPE
12.1 COMPANY SHARE ANALYSIS: EUROPE
13 SWOT ANALYSIS
14 COMPANY PROFILE
14.1 THERMO FISHER SCIENTIFIC INC.
14.1.1 COMPANY SNAPSHOT
14.1.2 REVENUE ANALYSIS
14.1.3 COMPANY SHARE ANALYSIS
14.1.4 PRODUCT PORTFOLIO
14.1.5 RECENT DEVELOPMENT
14.1.5.1 PARTNERSHIP
14.2 ALMAC GROUP
14.2.1 COMPANY SNAPSHOT
14.2.2 COMPANY SHARE ANALYSIS
14.2.3 PRODUCT PORTFOLIO
14.2.4 RECENT DEVELOPMENTS
14.3 CATALENT INC.
14.3.1 COMPANY SNAPSHOT
14.3.2 REVENUE ANALYSIS
14.3.3 COMPANY SHARE ANALYSIS
14.3.4 SERVICE PORTFOLIO
14.3.5 RECENT DEVELOPMENT
14.3.5.1 SERVICE EXPANSION
14.4 CLINIGEN GROUP PLC
14.4.1 COMPANY SNAPSHOT
14.4.2 REVENUE ANALYSIS
14.4.3 COMPANY SHARE ANALYSIS
14.4.4 PRODUCT PORTFOLIO
14.4.5 RECENT DEVELOPMENT
14.4.5.1 PARTNERSHIP
14.5 MOVIANTO
14.5.1 COMPANY SNAPSHOT
14.5.2 COMPANY SHARE ANALYSIS
14.5.3 SERVICE PORTFOLIO
14.5.4 RECENT DEVELOPMENT
14.5.4.1 ACQUISITION
14.6 PCI PHARMA SERVICES
14.6.1 COMPANY SNAPSHOT
14.6.2 SERVICE PORTFOLIO
14.6.3 RECENT DEVELOPMENTS
14.7 SHARP
14.7.1 COMPANY SNAPSHOT
14.7.2 SERVICE PORTFOLIO
14.7.3 RECENT DEVELOPMENT
14.8 ALIUM MEDICAL LIMITED
14.8.1 COMPANY SNAPSHOT
14.8.2 SERVICE PORTFOLIO
14.8.3 RECENT DEVELOPMENT
14.9 ANCILLARE, LP
14.9.1 COMPANY SNAPSHOT
14.9.2 SERVICE PORTFOLIO
14.9.3 RECENT DEVELOPMENT
14.1 BIOCAIR
14.10.1 COMPANY SNAPSHOT
14.10.2 SERVICE PORTFOLIO
14.10.3 RECENT DEVELOPMENTS
14.11 BIONICAL LTD.
14.11.1 COMPANY SNAPSHOT
14.11.2 SERVICE PORTFOLIO
14.11.3 RECENT DEVELOPMENT
14.11.3.1 SERVICE LAUNCH
14.12 CLINICAL SUPPLIES MANAGEMENT HOLDINGS,INC
14.12.1 COMPANY SNAPSHOT
14.12.2 SERVICE PORTFOLIO
14.12.3 RECENT DEVELOPMENT
14.13 KLIFO
14.13.1 COMPANY SNAPSHOT
14.13.2 SERVICE PORTFOLIO
14.13.3 RECENT DEVELOPMENTS
14.13.3.1 ACQUISTION
14.14 MYONEX
14.14.1 COMPANY SNAPSHOT
14.14.2 SERVICE PORTFOLIO
14.14.3 RECENT DEVELOPMENT
14.15 PAREXEL INTERNATIONAL CORPORATION
14.15.1 COMPANY SNAPSHOT
14.15.2 SERVICE PORTFOLIO
14.15.3 RECENT DEVELOPMENT
14.15.3.1 COLLABORATION
14.16 SIRO CLINPHARM PRIVATE LIMITED
14.16.1 COMPANY SNAPSHOT
14.16.2 SERVICE PORTFOLIO
14.16.3 RECENT DEVELOPMENTS
15 QUESTIONNAIRE
16 RELATED REPORTS
List of Table
TABLE 1 LOCATIONS OF REGISTERED STUDIES
TABLE 2 EUROPE CLINICAL TRIAL SUPPLIES MARKET, BY SERVICES, 2020-2029 (USD MILLION)
TABLE 3 EUROPE STORAGE IN CLINICAL TRIAL SUPPLIES MARKET, BY REGION, 2020-2029 (USD MILLION)
TABLE 4 EUROPE MANUFACTURING IN CLINICAL TRIAL SUPPLIES MARKET, BY REGION, 2020-2029 (USD MILLION)
TABLE 5 EUROPE PACKAGING AND LABELLING IN CLINICAL TRIAL SUPPLIES MARKET, BY REGION, 2020-2029 (USD MILLION)
TABLE 6 EUROPE DISTRIBUTION IN CLINICAL TRIAL SUPPLIES MARKET, BY REGION, 2020-2029 (USD MILLION)
TABLE 7 EUROPE CLINICAL TRIAL SUPPLIES MARKET, BY CLINICAL PHASE, 2020-2029 (USD MILLION)
TABLE 8 EUROPE PHASE III IN CLINICAL TRIAL SUPPLIES MARKET, BY REGION, 2020-2029 (USD MILLION)
TABLE 9 EUROPE PHASE II IN CLINICAL TRIAL SUPPLIES MARKET, BY REGION, 2020-2029 (USD MILLION)
TABLE 10 EUROPE PHASE IV IN CLINICAL TRIAL SUPPLIES MARKET, BY REGION, 2020-2029 (USD MILLION)
TABLE 11 EUROPE PHASE I IN CLINICAL TRIAL SUPPLIES MARKET, BY REGION, 2020-2029 (USD MILLION)
TABLE 12 EUROPE CLINICAL TRIAL SUPPLIES MARKET, BY THERAPEUTIC USE, 2020-2029 (USD MILLION)
TABLE 13 EUROPE ONCOLOGY IN CLINICAL TRIAL SUPPLIES MARKET, BY REGION, 2020-2029 (USD MILLION)
TABLE 14 EUROPE CARDIOVASCULAR DISEASES IN CLINICAL TRIAL SUPPLIES MARKET, BY REGION, 2020-2029 (USD MILLION)
TABLE 15 EUROPE DERMATOLOGY IN CLINICAL TRIAL SUPPLIES MARKET, BY REGION, 2020-2029 (USD MILLION)
TABLE 16 EUROPE METABOLIC DISORDERS IN CLINICAL TRIAL SUPPLIES MARKET, BY REGION, 2020-2029 (USD MILLION)
TABLE 17 EUROPE INFECTIOUS DISEASES IN CLINICAL TRIAL SUPPLIES MARKET, BY REGION, 2020-2029 (USD MILLION)
TABLE 18 EUROPE RESPIRATORY DISEASES IN CLINICAL TRIAL SUPPLIES MARKET, BY REGION, 2020-2029 (USD MILLION)
TABLE 19 EUROPE CNS AND MENTAL DISORDERS IN CLINICAL TRIAL SUPPLIES MARKET, BY REGION, 2020-2029 (USD MILLION)
TABLE 20 EUROPE BLOOD DISORDERS IN CLINICAL TRIAL SUPPLIES MARKET, BY REGION, 2020-2029 (USD MILLION)
TABLE 21 EUROPE OTHERS IN CLINICAL TRIAL SUPPLIES MARKET, BY REGION, 2020-2029 (USD MILLION)
TABLE 22 EUROPE CLINICAL TRIAL SUPPLIES MARKET, BY END USER, 2020-2029 (USD MILLION)
TABLE 23 EUROPE CONTRACT RESEARCH ORGANIZATIONS IN CLINICAL TRIAL SUPPLIES MARKET, BY REGION, 2020-2029 (USD MILLION)
TABLE 24 EUROPE PHARMACEUTICAL AND BIOTECHNOLOGY COMPANIES IN CLINICAL TRIAL SUPPLIES MARKET, BY REGION, 2020-2029 (USD MILLION)
TABLE 25 EUROPE CLINICAL TRIAL SUPPLIES MARKET, BY COUNTRY, 2020-2029 (USD MILLION)
TABLE 26 EUROPE CLINICAL TRIAL SUPPLIES MARKET, BY SERVICES, 2020-2029 (USD MILLION)
TABLE 27 EUROPE CLINICAL TRIAL SUPPLIES MARKET, BY CLINICAL PHASE, 2020-2029 (USD MILLION)
TABLE 28 EUROPE CLINICAL TRIAL SUPPLIES MARKET, BY THERAPEUTIC USE, 2020-2029 (USD MILLION)
TABLE 29 EUROPE CLINICAL TRIAL SUPPLIES MARKET, BY END USER, 2020-2029 (USD MILLION)
TABLE 30 GERMANY CLINICAL TRIAL SUPPLIES MARKET, BY SERVICES, 2020-2029 (USD MILLION)
TABLE 31 GERMANY CLINICAL TRIAL SUPPLIES MARKET, BY CLINICAL PHASE, 2020-2029 (USD MILLION)
TABLE 32 GERMANY CLINICAL TRIAL SUPPLIES MARKET, BY THERAPEUTIC USE, 2020-2029 (USD MILLION)
TABLE 33 GERMANY CLINICAL TRIAL SUPPLIES MARKET, BY END USER, 2020-2029 (USD MILLION)
TABLE 34 FRANCE CLINICAL TRIAL SUPPLIES MARKET, BY SERVICES, 2020-2029 (USD MILLION)
TABLE 35 FRANCE CLINICAL TRIAL SUPPLIES MARKET, BY CLINICAL PHASE, 2020-2029 (USD MILLION)
TABLE 36 FRANCE CLINICAL TRIAL SUPPLIES MARKET, BY THERAPEUTIC USE, 2020-2029 (USD MILLION)
TABLE 37 FRANCE CLINICAL TRIAL SUPPLIES MARKET, BY END USER, 2020-2029 (USD MILLION)
TABLE 38 U.K. CLINICAL TRIAL SUPPLIES MARKET, BY SERVICES, 2020-2029 (USD MILLION)
TABLE 39 U.K. CLINICAL TRIAL SUPPLIES MARKET, BY CLINICAL PHASE, 2020-2029 (USD MILLION)
TABLE 40 U.K. CLINICAL TRIAL SUPPLIES MARKET, BY THERAPEUTIC USE, 2020-2029 (USD MILLION)
TABLE 41 U.K. CLINICAL TRIAL SUPPLIES MARKET, BY END USER, 2020-2029 (USD MILLION)
TABLE 42 ITALY CLINICAL TRIAL SUPPLIES MARKET, BY SERVICES, 2020-2029 (USD MILLION)
TABLE 43 ITALY CLINICAL TRIAL SUPPLIES MARKET, BY CLINICAL PHASE, 2020-2029 (USD MILLION)
TABLE 44 ITALY CLINICAL TRIAL SUPPLIES MARKET, BY THERAPEUTIC USE, 2020-2029 (USD MILLION)
TABLE 45 ITALY CLINICAL TRIAL SUPPLIES MARKET, BY END USER, 2020-2029 (USD MILLION)
TABLE 46 SPAIN CLINICAL TRIAL SUPPLIES MARKET, BY SERVICES, 2020-2029 (USD MILLION)
TABLE 47 SPAIN CLINICAL TRIAL SUPPLIES MARKET, BY CLINICAL PHASE, 2020-2029 (USD MILLION)
TABLE 48 SPAIN CLINICAL TRIAL SUPPLIES MARKET, BY THERAPEUTIC USE, 2020-2029 (USD MILLION)
TABLE 49 SPAIN CLINICAL TRIAL SUPPLIES MARKET, BY END USER, 2020-2029 (USD MILLION)
TABLE 50 NETHERLANDS CLINICAL TRIAL SUPPLIES MARKET, BY SERVICES, 2020-2029 (USD MILLION)
TABLE 51 NETHERLANDS CLINICAL TRIAL SUPPLIES MARKET, BY CLINICAL PHASE, 2020-2029 (USD MILLION)
TABLE 52 NETHERLANDS CLINICAL TRIAL SUPPLIES MARKET, BY THERAPEUTIC USE, 2020-2029 (USD MILLION)
TABLE 53 NETHERLANDS CLINICAL TRIAL SUPPLIES MARKET, BY END USER, 2020-2029 (USD MILLION)
TABLE 54 RUSSIA CLINICAL TRIAL SUPPLIES MARKET, BY SERVICES, 2020-2029 (USD MILLION)
TABLE 55 RUSSIA CLINICAL TRIAL SUPPLIES MARKET, BY CLINICAL PHASE, 2020-2029 (USD MILLION)
TABLE 56 RUSSIA CLINICAL TRIAL SUPPLIES MARKET, BY THERAPEUTIC USE, 2020-2029 (USD MILLION)
TABLE 57 RUSSIA CLINICAL TRIAL SUPPLIES MARKET, BY END USER, 2020-2029 (USD MILLION)
TABLE 58 BELGIUM CLINICAL TRIAL SUPPLIES MARKET, BY SERVICES, 2020-2029 (USD MILLION)
TABLE 59 BELGIUM CLINICAL TRIAL SUPPLIES MARKET, BY CLINICAL PHASE, 2020-2029 (USD MILLION)
TABLE 60 BELGIUM CLINICAL TRIAL SUPPLIES MARKET, BY THERAPEUTIC USE, 2020-2029 (USD MILLION)
TABLE 61 BELGIUM CLINICAL TRIAL SUPPLIES MARKET, BY END USER, 2020-2029 (USD MILLION)
TABLE 62 TURKEY CLINICAL TRIAL SUPPLIES MARKET, BY SERVICES, 2020-2029 (USD MILLION)
TABLE 63 TURKEY CLINICAL TRIAL SUPPLIES MARKET, BY CLINICAL PHASE, 2020-2029 (USD MILLION)
TABLE 64 TURKEY CLINICAL TRIAL SUPPLIES MARKET, BY THERAPEUTIC USE, 2020-2029 (USD MILLION)
TABLE 65 TURKEY CLINICAL TRIAL SUPPLIES MARKET, BY END USER, 2020-2029 (USD MILLION)
TABLE 66 SWITZERLAND CLINICAL TRIAL SUPPLIES MARKET, BY SERVICES, 2020-2029 (USD MILLION)
TABLE 67 SWITZERLAND CLINICAL TRIAL SUPPLIES MARKET, BY CLINICAL PHASE, 2020-2029 (USD MILLION)
TABLE 68 SWITZERLAND CLINICAL TRIAL SUPPLIES MARKET, BY THERAPEUTIC USE, 2020-2029 (USD MILLION)
TABLE 69 SWITZERLAND CLINICAL TRIAL SUPPLIES MARKET, BY END USER, 2020-2029 (USD MILLION)
TABLE 70 REST OF EUROPE CLINICAL TRIAL SUPPLIES MARKET, BY SERVICES, 2020-2029 (USD MILLION)
List of Figure
FIGURE 1 EUROPE CLINICAL TRIAL SUPLLIES MARKET: SEGMENTATION
FIGURE 2 EUROPE CLINICAL TRIAL SUPPLIES MARKET: DATA TRIANGULATION
FIGURE 3 EUROPE CLINICAL TRIAL SUPPLIES MARKET: DROC ANALYSIS
FIGURE 4 EUROPE CLINICAL TRIAL SUPPLIES MARKET: EUROPE VS REGIONAL MARKET ANALYSIS
FIGURE 5 EUROPE CLINICAL TRIAL SUPPLIES MARKET: COMPANY RESEARCH ANALYSIS
FIGURE 6 EUROPE CLINICAL TRIAL SUPLLIES MARKET: INTERVIEW DEMOGRAPHICS
FIGURE 7 EUROPE CLINICAL TRIAL SUPPLIES MARKET: DBMR MARKET POSITION GRID
FIGURE 8 EUROPE CLINICAL TRIAL SUPPLIES MARKET: DBMR VENDOR SHARE ANALYSIS
FIGURE 9 EUROPE CLINICAL TRIAL SUPPLIES MARKET: SEGMENTATION
FIGURE 10 NORTH AMERICA IS EXPECTED TO DOMINATE THE EUROPE CLINICAL TRIAL SUPPLIES MARKET IN THE FORECAST PERIOD OF 2022 TO 2029
FIGURE 11 RISING DEMAND FOR CLINICAL TRIALS WORLDWIDE AND INCREASING INCIDENCES OF DISEASES IS DRIVING THE EUROPE CLINICAL TRIAL SUPPLIES MARKET IN THE FORECAST PERIOD OF 2022 TO 2029
FIGURE 12 STORAGE SEGMENT IS EXPECTED TO ACCOUNT FOR THE LARGEST SHARE OF THE EUROPE CLINICAL TRIAL SUPPLIES MARKET IN 2022 & 2029
FIGURE 13 DRIVERS, RESTRAINTS, OPPORTUNITIES AND CHALLENGES OF EUROPE CLINICAL TRIAL SUPPLIES MARKET
FIGURE 14 EUROPE CLINICAL TRIAL SUPPLIES MARKET: BY SERVICES, 2021
FIGURE 15 EUROPE CLINICAL TRIAL SUPPLIES MARKET: BY SERVICES, 2022-2029 (USD MILLION)
FIGURE 16 EUROPE CLINICAL TRIAL SUPPLIES MARKET: BY SERVICES, CAGR (2022-2029)
FIGURE 17 EUROPE CLINICAL TRIAL SUPPLIES MARKET: BY SERVICES, LIFELINE CURVE
FIGURE 18 EUROPE CLINICAL TRIAL SUPPLIES MARKET: BY CLINICAL PHASE, 2021
FIGURE 19 EUROPE CLINICAL TRIAL SUPPLIES MARKET: BY CLINICAL PHASE, 2022-2029 (USD MILLION)
FIGURE 20 EUROPE CLINICAL TRIAL SUPPLIES MARKET: BY CLINICAL PHASE, CAGR (2022-2029)
FIGURE 21 EUROPE CLINICAL TRIAL SUPPLIES MARKET: BY CLINICAL PHASE, LIFELINE CURVE
FIGURE 22 EUROPE CLINICAL TRIAL SUPPLIES MARKET: BY THERAPEUTIC USE, 2021
FIGURE 23 EUROPE CLINICAL TRIAL SUPPLIES MARKET: BY THERAPEUTIC USE, 2022-2029 (USD MILLION)
FIGURE 24 EUROPE CLINICAL TRIAL SUPPLIES MARKET: BY THERAPEUTIC USE, CAGR (2022-2029)
FIGURE 25 EUROPE CLINICAL TRIAL SUPPLIES MARKET: BY THERAPEUTIC USE, LIFELINE CURVE
FIGURE 26 EUROPE CLINICAL TRIAL SUPPLIES MARKET: BY END USER, 2021
FIGURE 27 EUROPE CLINICAL TRIAL SUPPLIES MARKET: BY END USER, 2022-2029 (USD MILLION)
FIGURE 28 EUROPE CLINICAL TRIAL SUPPLIES MARKET: BY END USER, CAGR (2022-2029)
FIGURE 29 EUROPE CLINICAL TRIAL SUPPLIES MARKET: BY END USER, LIFELINE CURVE
FIGURE 30 EUROPE CLINICAL TRIAL SUPPLIES MARKET: SNAPSHOT (2021)
FIGURE 31 EUROPE CLINICAL TRIAL SUPPLIES MARKET: BY COUNTRY (2021)
FIGURE 32 EUROPE CLINICAL TRIAL SUPPLIES MARKET: BY COUNTRY (2022 & 2029)
FIGURE 33 EUROPE CLINICAL TRIAL SUPPLIES MARKET: BY COUNTRY (2021 & 2029)
FIGURE 34 EUROPE CLINICAL TRIAL SUPPLIES MARKET: BY SERVICES (2022-2029)
FIGURE 35 EUROPE CLINICAL TRIAL SUPPLIES MARKET: COMPANY SHARE 2021 (%)
منهجية البحث
يتم جمع البيانات وتحليل سنة الأساس باستخدام وحدات جمع البيانات ذات أحجام العينات الكبيرة. تتضمن المرحلة الحصول على معلومات السوق أو البيانات ذات الصلة من خلال مصادر واستراتيجيات مختلفة. تتضمن فحص وتخطيط جميع البيانات المكتسبة من الماضي مسبقًا. كما تتضمن فحص التناقضات في المعلومات التي شوهدت عبر مصادر المعلومات المختلفة. يتم تحليل بيانات السوق وتقديرها باستخدام نماذج إحصائية ومتماسكة للسوق. كما أن تحليل حصة السوق وتحليل الاتجاهات الرئيسية هي عوامل النجاح الرئيسية في تقرير السوق. لمعرفة المزيد، يرجى طلب مكالمة محلل أو إرسال استفسارك.
منهجية البحث الرئيسية التي يستخدمها فريق بحث DBMR هي التثليث البيانات والتي تتضمن استخراج البيانات وتحليل تأثير متغيرات البيانات على السوق والتحقق الأولي (من قبل خبراء الصناعة). تتضمن نماذج البيانات شبكة تحديد موقف البائعين، وتحليل خط زمني للسوق، ونظرة عامة على السوق ودليل، وشبكة تحديد موقف الشركة، وتحليل براءات الاختراع، وتحليل التسعير، وتحليل حصة الشركة في السوق، ومعايير القياس، وتحليل حصة البائعين على المستوى العالمي مقابل الإقليمي. لمعرفة المزيد عن منهجية البحث، أرسل استفسارًا للتحدث إلى خبراء الصناعة لدينا.
التخصيص متاح
تعد Data Bridge Market Research رائدة في مجال البحوث التكوينية المتقدمة. ونحن نفخر بخدمة عملائنا الحاليين والجدد بالبيانات والتحليلات التي تتطابق مع هدفهم. ويمكن تخصيص التقرير ليشمل تحليل اتجاه الأسعار للعلامات التجارية المستهدفة وفهم السوق في بلدان إضافية (اطلب قائمة البلدان)، وبيانات نتائج التجارب السريرية، ومراجعة الأدبيات، وتحليل السوق المجدد وقاعدة المنتج. ويمكن تحليل تحليل السوق للمنافسين المستهدفين من التحليل القائم على التكنولوجيا إلى استراتيجيات محفظة السوق. ويمكننا إضافة عدد كبير من المنافسين الذين تحتاج إلى بيانات عنهم بالتنسيق وأسلوب البيانات الذي تبحث عنه. ويمكن لفريق المحللين لدينا أيضًا تزويدك بالبيانات في ملفات Excel الخام أو جداول البيانات المحورية (كتاب الحقائق) أو مساعدتك في إنشاء عروض تقديمية من مجموعات البيانات المتوفرة في التقرير.